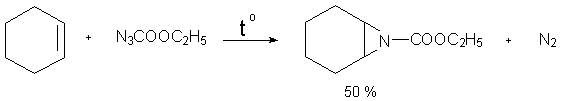
V. ЦИКЛИЧЕСКИЕ АЗОСОЕДИНЕНИЯ (ДИАЗИРИНЫ)
В конце XIX века для диазометана и других
диазоалканов было предложено две альтернативные
структурные формулы - линейная CH2 =N +=
N - (И.Тиле) и циклическая (Г. Пехман). 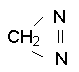
На протяжении многих лет не было строгих
аргументов в пользу какой-либо из этих структур.
Спектроскопические данные указывали на линейную
структуру диазометана и других диазоалканов, но
однозначные доказательства в ее пользу были
получены сравнительно недавно, после того как Э.
Шмитц в 1961 году получил изомерные им диазирины
общей формулы 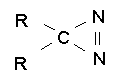
Диазирины образуются при окислении циклических гидразинов с помощью таких окислителей как оксид серебра или оксид ртути.
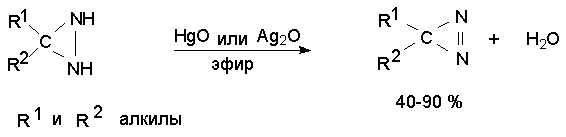
Исходные 3,3-диалкилдиазиридины получаются при взаимодействии алифатических кетонов с аммиаком и гидроксиламин-О-сульфокислотой.
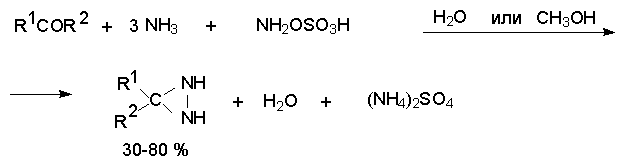
Диазирины неожиданно оказались гораздо более стабильными соединениями, чем изомерные им диазоалканы. Диазирины не расщепляются при действии растворов кислот и щелочей при 20о и довольно устойчивы при нагревании до 100о. Однако реактивы Гриньяра гладко присоединяются к двойной связи диазиринов с образованием 1-алкилдиазиридинов.
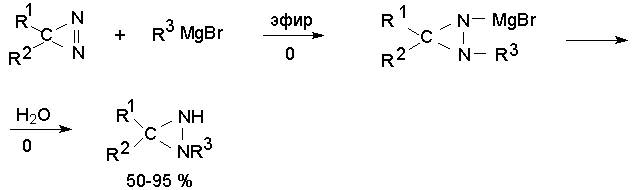
С помощью этой реакции диазирины можно легко отличить от диазоалканов, которые при действии реактивов Гриньяра дают N-алкилгидразоны.
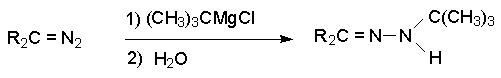
Диазирины подобно диазоалканам при фотолизе дают карбены, которые проявляют свойства типичные для синглетных карбенов.
Диазирины изомеризуются в диазоалканы при облучении в матрице из твердого азота или аргона при 20оК. Так, например, незамещенный диазирин нацело превращается в этих условиях в диазометан. Для диазирина, содержащего в качестве метки изотоп 15N, при облучении в твердой матрице немеченного азота имеет место изотопный обмен. Это указывает на то, что образование диазометана из диазирина происходит за счет отщепления и последующего присоединения азота.
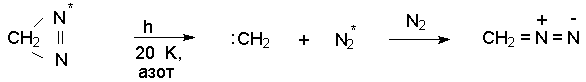
VI. АЗИДЫ.
По своей структуре органические азиды RN3, содержащие цепь из трех атомов азота, являются близкими аналогами диазосоединений. Строение азидов может быть описано с помощью двух граничных формул :
![]()
Согласно данным рентгеноструктурного анализа длины связей азот - азот в метилазиде сильно отличаются и от ординарной и от тройной связи.
![]()
VI.1. Получение азидов.
В течение длительного времени азиды оставались труднодоступным классом соединений. За последние двадцать лет положение кардинальным образом изменилось в результате внедрения в практику органического синтеза диполярных апротонных растворителей и метода межфазного катализа.
В настоящее время первичные и вторичные азиды получают с помощью обычных реакций бимолекулярного нуклеофильного замещения с участием азид - иона.
| ГМФТА, 20 | ||||
| C6H5CH2CH2Br | + NaN3 | C6H5CH2CH2N3 | + NaBr | |
| 86 % | ||||
| 18-краун-6 | ||||
| CH3(CH2)14CH2Br | + NaN3 | СH3(СH2)14CH2N3 | + NaBr | |
| CH3CN, 20 | 90 % |
Аналогичным образом из ацилгалогенидов могут быть получены ацилазиды, которые находят применение в синтезе пептидов и для получения первичных аминов с помощью перегруппировки Курциуса.
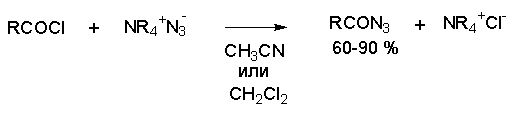
Ароматические азиды получают при обработке солей диазония азидом натрия или с помощью нитрозирования арилгидразинов.
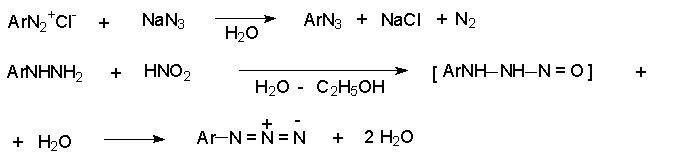
При наличии двух или более активирующих электроноакцепторных заместителей в бензольном кольце арилазиды могут быть получены также и в результате нуклеофильного замещения галогена по механизму SNAr.
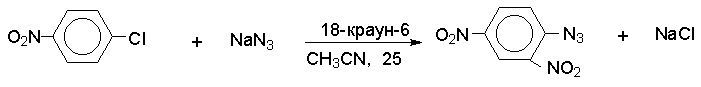
VI.2. Свойства азидов.
Термическая устойчивость азидов изменяется в ряду : алкилазиды < арилазиды < сульфонилазиды < ацилазиды. Особенно низкой термической стабильностью отличаются азиды с низкой молекулярной массой, в то время как азиды с высокой молекулярной массой сравнительно безопасны в обращении.
VI.2a. Восстановление азидов до аминов.
Алифатические азиды легко восстанавливаются до аминов с помощью алюмогидрида лития в эфире, ТГФ, ДМЭ. При этом нет никакой необходимости в выделении азидов в индивидуальном виде. Неочищенный азид сразу же восстанавливают алюмогидридом лития в эфирном растворе.
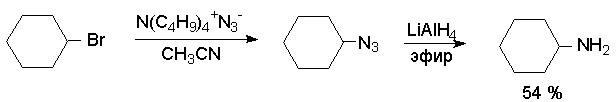
Восстановление азидов до аминов можно проводить также и каталитически на палладии и платине. Избирательное восстановление азидной группы в присутствии двойной связи может быть осуществлено с помощью катализатора Линдлара.
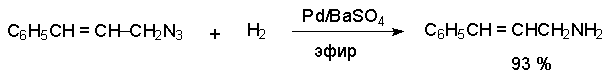
Ацилазиды перегруппировываются в изоцианаты,которые далее превращают в первичные амины. Это превращение лежит в основе перегруппировки Курциуса.
VI.2б.1,3-Диполярное циклоприсоединение азидов к алкенам и алкинам.
Алкилазиды и арилазиды относятся к многочисленному семейству 1,3-диполярофилов, которые вступают в реакции циклоприсоединения с алкенами. Особенно легко присоединяются азиды по двойной связи, сопряженной со сложноэфирной. нитрильной, нитрогрупой или с бензольным кольцом. В результате [4 + 2] - циклоприсоединения азидов к двойной связи образуются 1,2,3 - - триазолины.
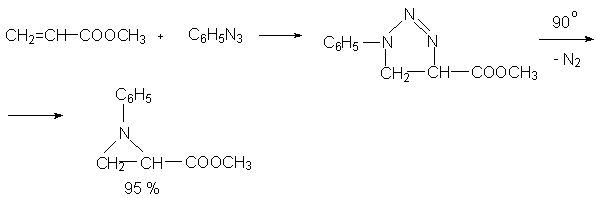
1,2,3 - - Триазолины термически нестабильны и при нагревании до 90-100о разлагаются с выделением азота.
1,3-Диполярное [4 + 2] -циклоприсоединение азидов к алкинам приводит к более устойчивым 1,2,3 - триазолам.
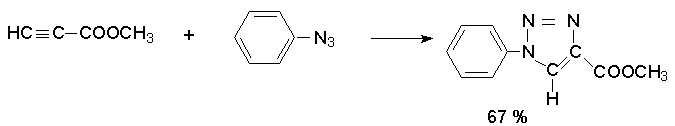
Азиды служат исходными веществами для генерирования чрезвычайно интересных реакционноспособных интермедиатов RN, называемых нитренами.
Нитрены являются азотистыми аналогами карбенов и подобно своим углеродным аналогам могут находиться в синглетной RN или триплетной форме RN . Ароматические азиды, ацилазиды и тозилазид при фотолитическом или термическом разложении при 100-150о дают синглетную форму нитрена. Синглетный нитрен легко превращается в более стабильный триплетный нитрен. Фотолиз азидов в присутствии триплетных сенсибилизаторов приводит прямо к триплетной форме нитрена. Для нитренов, в принципе, характерны те же реакции, что и для карбенов,т.е. присоединение к двойной углерод - углеродной связи и внедрение по связи С-Н. Синглетный нитрен стереоспецифически присоединяется по двойной связи алкенов с образованием производных азиридина с сохранением конфигурации алкена.