|
Учебные материалы по физической химии
Задачи по физической химии.Часть 2.Химическая кинетика. Электрохимия
4. Влияние температуры на скорость
химических реакций
Из качественных соображений понятно, что
скорость реакций должна увеличиваться с ростом
температуры, т.к. при этом возрастает энергия
сталкивающихся частиц и повышается вероятность
того, что при столкновении произойдет химическое
превращение. Для количественного описания
температурных эффектов в химической кинетике
используют два основных соотношения - правило
Вант-Гоффа и уравнение Аррениуса.
Правило Вант-Гоффа заключается в том, что
при нагревании на 10 оС скорость
большинства химических реакций увеличивается в 2 4 раза.
Математически это означает, что скорость реакции
зависит от температуры степенным образом: 4 раза.
Математически это означает, что скорость реакции
зависит от температуры степенным образом:
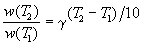 , (4.1) , (4.1)
где  -
температурный коэффициент скорости ( -
температурный коэффициент скорости ( = 2 = 2 4). Правило
Вант-Гоффа является весьма грубым и применимо
только в очень ограниченном интервале
температур. 4). Правило
Вант-Гоффа является весьма грубым и применимо
только в очень ограниченном интервале
температур.
Гораздо более точным является уравнение
Аррениуса, описывающее температурную
зависимость константы скорости:
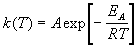 , (4.2) , (4.2)
где R - универсальная газовая постоянная; A
- предэкспоненциальный множитель, который не
зависит от температуры, а определяется только
видом реакции; EA - энергия активации,
которую можно охарактеризовать как некоторую
пороговую энергию: грубо говоря, если энергия
сталкивающихся частиц меньше EA, то при
столкновении реакция не произойдет, если энергия
превышает EA, реакция произойдет.
Энергия активации не зависит от температуры.
Графически зависимость k(T) выглядит
следующим образом:
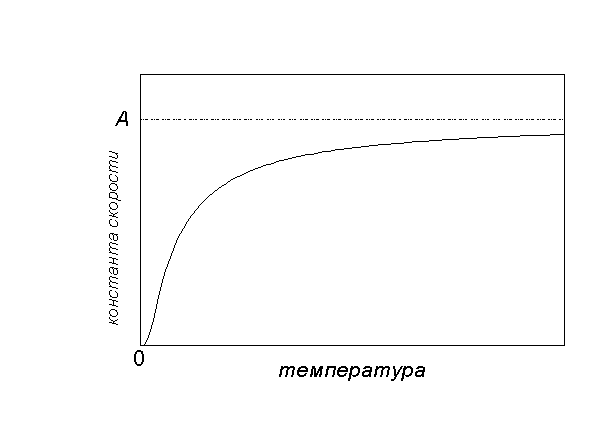
При низких температурах химические реакции
почти не протекают: k(T)  0. При очень высоких
температурах константа скорости стремится к
предельному значению: k(T) 0. При очень высоких
температурах константа скорости стремится к
предельному значению: k(T) A. Это
соответствует тому, что все молекулы являются
химически активными и каждое столкновение
приводит к реакции. A. Это
соответствует тому, что все молекулы являются
химически активными и каждое столкновение
приводит к реакции.
Энергию активации можно определить, измерив
константу скорости при двух температурах. Из
уравнения (4.2) следует:
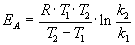 . (4.3) . (4.3)
Более точно энергию активации определяют по
значениям константы скорости при нескольких
температурах. Для этого уравнение Аррениуса (4.2)
записывают в логарифмической форме
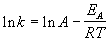
и записывают экспериментальные данные в
координатах ln k - 1/T. Тангенс угла наклона
полученной прямой равен -EA / R.
Для некоторых реакций предэкспоненциальный
множитель слабо зависит от температуры. В этом
случае определяют так называемую опытную
энергию активации:
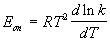 . (4.4) . (4.4)
Если предэкспоненциальный множитель -
постоянный, то опытная энергия активации равна
аррениусовской энергии активации: Eоп = EA.
ПРИМЕРЫ
Пример 4-1. Пользуясь уравнением Аррениуса,
оцените, при каких температурах и энергиях
активации справедливо правило Вант-Гоффа.
Решение. Представим правило Вант-Гоффа (4.1)
как степенную зависимость константы скорости:
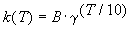 , ,
где B - постоянная величина. Сравним это
выражение с уравнением Аррениуса (4.2), приняв для
температурного коэффициента скорости значение  ~ e =
2.718: ~ e =
2.718:
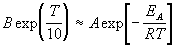 . .
Возьмем натуральный логарифм обеих частей
этого приближенного равенства:
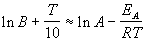 . .
Продифференцировав полученное соотношение по
температуре, найдем искомую связь связь между
энергией активации и температурой:
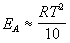 . .
Если энергия активации и температура примерно
удовлетворяют этому соотношению, то правилом
Вант-Гоффа для оценки влияния температуры на
скорость реакции пользоваться можно.
Пример 4-2. Реакция первого порядка при
температуре 70 оС завершается на 40% за 60 мин.
При какой температуре реакция завершится на 80% за
120 мин, если энергия активации равна 60 кДж/моль?
Решение. Для реакции первого порядка
константа скорости выражается через степень
превращения следующим образом:
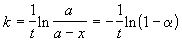 , ,
где a = x/a - степень превращения. Запишем
это уравнение при двух температурах с учетом
уравнения Аррениуса:
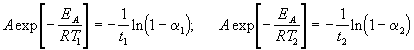 , ,
где EA = 60 кДж/моль, T1 = 343 K, t1
= 60 мин, a 1 = 0.4, t2 = 120 мин, a 2 =
0.8. Поделим одно уравнение на другое и
прологарифмируем:
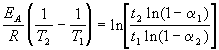
Подставляя в это выражение приведенные выше
величины, находим T2 = 333 К = 60 оС.
Пример 4-3. Скорость бактериального гидролиза
мышц рыб удваивается при переходе от температуры
-1.1о С к температуре +2.2 оС. Оцените
энергию активации этой реакции.
Решение. Увеличение скорости гидролиза в 2
раза обусловлено увеличением константы
скорости: k2 = 2k1. Энергию
активации по отношению констант скорости при
двух температурах можно определить из уравнения
(4.3) с T1 = t1 + 273.15 = 272.05 K, T2
= t2 + 273.15 = 275.35 K:
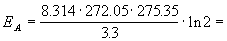 130800 Дж/моль = 130.8
кДж/моль. 130800 Дж/моль = 130.8
кДж/моль.
ЗАДАЧИ
4-1. При помощи правила Вант-Гоффа вычислите,
при какой температуре реакция закончится через 15
мин, если при 20 оС на это требуется 2 ч.
Температурный коэффициент скорости равен 3.(ответ)
4-2. Время полураспада вещества при 323 К равно
100 мин, а при 353 К - 15 мин. Определите температурный
коэффициент скорости.(ответ)
4-3. Какой должна быть энергия активации, чтобы
скорость реакции увеличивалась в 3 раза при
возрастании температуры на 10 0С а) при 300 К;
б) при 1000 К?(ответ)
4-4. Реакция первого порядка имеет энергию
активации 25 ккал/моль и предэкспоненциальный
множитель 5. 1013 сек-1. При какой
температуре время полураспада для данной
реакции составит: а) 1 мин; б) 30 дней?(ответ)
4-5. В каком из двух случаев константа скорости
реакции увеличивается в большее число раз: при
нагревании от 0 оС до 10 оС или при
нагревании от 10 оС до 20 оС? Ответ
обоснуйте с помощью уравнения Аррениуса.(ответ)
4-6. Энергия активации некоторой реакции в 1.5
раза больше, чем энергия активации другой
реакции. При нагревании от T1 до T2
константа скорости второй реакции увеличилась в a
раз. Во сколько раз увеличилась константа
скорости первой реакции при нагревании от T1
до T2?(ответ)
4-7. Константа скорости сложной реакции
выражается через константы скорости
элементарных стадий следующим образом:
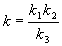
Выразите энергию активации и
предэкспоненциальный множитель сложной реакции
через соответствующие величины, относящиеся к
элементарным стадиям.(ответ)
4-8. В необратимой реакции 1-го порядка за 20 мин
при 125 оС степень превращения исходного
вещества составила 60%, а при 145 oC такая же
степень превращения была достигнута за 5.5 мин.
Найдите константы скорости и энергию активации
данной реакции .(ответ)
4-9. Реакция 1-го порядка при температуре 25 оС
завершается на 30% за 30 мин. При какой температуре
реакция завершится на 60% за 40 мин, если энергия
активации равна 30 кДж/моль?(ответ)
4-10. Реакция 1-го порядка при температуре 25 оС
завершается на 70% за 15 мин. При какой температуре
реакция завершится на 50% за 15 мин, если энергия
активации равна 50 кДж/моль?(ответ)
4-11. Константа скорости реакции первого
порядка равна 4.02.10-4 с -1 при 393 К
и 1.98. 10-3 с -1 при 413 К. Рассчитайте
предэкспоненциальный множитель для этой
реакции.(ответ)
4-12. Для реакции H2 + I2  2HI константа скорости при
температуре 683 К равна 0,0659 л/(моль. мин), а при
температуре 716 К - 0,375 л/(моль. мин). Найдите энергию
активации этой реакции и константу скорости при
температуре 700 К.(ответ) 2HI константа скорости при
температуре 683 К равна 0,0659 л/(моль. мин), а при
температуре 716 К - 0,375 л/(моль. мин). Найдите энергию
активации этой реакции и константу скорости при
температуре 700 К.(ответ)
4-13. Для реакции 2N2O  2N2 + O2 константа скорости при
температуре 986 К равна 6,72 л/(моль. мин), а при
температуре 1165 К - 977,0 л/(моль. мин). Найдите
энергию активации этой реакции и константу
скорости при температуре 1053,0 К.(ответ) 2N2 + O2 константа скорости при
температуре 986 К равна 6,72 л/(моль. мин), а при
температуре 1165 К - 977,0 л/(моль. мин). Найдите
энергию активации этой реакции и константу
скорости при температуре 1053,0 К.(ответ)
4-14. Трихлорацетат-ион в ионизирующих
растворителях, содержащих H+, разлагается
по уравнению
H+ + CCl3COO-  CO2 + CHCl3 CO2 + CHCl3
Стадией, определяющей скорость реакции,
является мономолекулярный разрыв связи C- C в
трихлорацетат-ионе. Реакция протекает по первому
порядку, и константы скорости имеют следующие
значения: k = 3.11.10-4 с-1 при 90 оС,
k = 7.62.10-5 с-1 при 80 оС.
Рассчитайте а) энергию активации, б) константу
скорости при 60 оС.(ответ)
4-15. Для реакции CH3COOC2H5 + NaOH ѕ  CH3COONa + C2H5OH
константа скорости при температуре 282,6 К равна
2,307 л/(моль. мин), а при температуре 318,1 К - 21,65
л/(моль. мин). Найдите энергию активации этой
реакции и константу скорости при температуре 343
К.(ответ) CH3COONa + C2H5OH
константа скорости при температуре 282,6 К равна
2,307 л/(моль. мин), а при температуре 318,1 К - 21,65
л/(моль. мин). Найдите энергию активации этой
реакции и константу скорости при температуре 343
К.(ответ)
4-16. Для реакции C12H22O11 + H2O
 C6H12O6 + C6H12O6
константа скорости при температуре 298,2 К равна
0,765 л/(моль. мин), а при температуре 328,2 К - 35,5
л/(моль. мин). Найдите энергию активации этой
реакции и константу скорости при температуре 313,2
К.(ответ) C6H12O6 + C6H12O6
константа скорости при температуре 298,2 К равна
0,765 л/(моль. мин), а при температуре 328,2 К - 35,5
л/(моль. мин). Найдите энергию активации этой
реакции и константу скорости при температуре 313,2
К.(ответ)
4-17. Вещество разлагается двумя параллельными
путями с константами скорости k1 и k2.
Какова разность энергий активации этих двух
реакций, если при 10 oC k1/k2
= 10, а при 40 oC k1/k2 = 0.1?(ответ)
4-18. В двух реакциях одинакового порядка
разница энергий активации составляет E2
- E1 = 40 кДж/моль. При температуре 293 К
отношение констант скорости равно k1/k2
= 2. При какой температуре константы скорости
сравняются?(ответ)
4-19. Разложение ацетондикарбоновой кислоты в
водном растворе - реакция первого порядка.
Измерены константы скорости этой реакции при
разных температурах:
T, оС |
0 |
20 |
40 |
60 |
k. 105, с-1 |
2.46 |
47.5 |
576 |
5480 |
Рассчитайте энергию активации и
предэкспоненциальный множитель. Чему равен
период полураспада при 25 оС? (ответ)
|


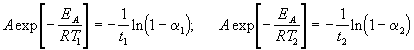 ,
,