С. Т. Жуков Химия-10/11класс
18. Окислительно-восстановительные реакции (продолжение 1)
18.5. ОВР пероксида водорода
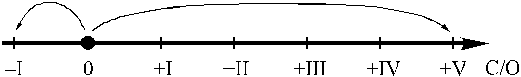
В молекулах пероксида водорода H2O2
атомы кислорода находятся в степени окисления
–I. Это промежуточная и не самая устойчивая
степень окисления атомов этого элемента, поэтому
пероксид водорода проявляет и окислительные, и
восстановительные свойства.
Окислительно-восстановительная активность
этого вещества зависит от концентрации. В обычно
используемых растворах с массовой долей 20 %
пероксид водорода довольно сильный окислитель, в
разбавленных растворах его окислительная
активность снижается. Восстановительные
свойства для пероксида водорода менее
характерны, чем окислительные, и также зависят от
концентрации.
Пероксид водорода – очень слабая кислота (см.
приложение 13), поэтому в сильнощелочных
растворах его молекулы превращаются
гидропероксид-ионы.
В зависимости от реакции среды и от того,
окислителем или восстановителем является
пероксид водорода в данной реакции, продукты
окислительно-восстановительного взаимодействия
будут разными. Уравнения полуреакций для всех
этих случаев приведены в таблице 1.
Таблица 1
Уравнения
окислительно-восстановительных полуреакций H2O2
в растворах
Рассмотрим примеры ОВР с участием пероксида
водорода.
Пример 1. Составьте уравнение реакции,
протекающей при добавлении раствора йодида
калия к раствору пероксида водорода,
подкисленному серной кислотой.
| 1 |
H2O2 + 2H3O + 2e– = 4H2O + 2e– = 4H2O |
| 1 |
2I –
2e– = I2 –
2e– = I2 |
H2O2 + 2H3O +2I
+2I =
4H2O + I2
=
4H2O + I2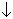
H2O2 + H2SO4 + 2KI = 2H2O + I2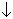 + K2SO4
+ K2SO4
Пример 2. Составьте уравнение реакции между
перманганатом калия и пероксидом водорода в
водном растворе, подкисленном серной кислотой.
| 2 |
MnO4 + 8H3O + 8H3O + 5e– = Mn2
+ 5e– = Mn2 + 12H2O + 12H2O |
| 5 |
H2O2 + 2H2O – 2e–
= O2 + 2H3O |
2MnO4 + 6H3O+ + 5H2O2 = 2Mn2
+ 6H3O+ + 5H2O2 = 2Mn2 + 14H2O + 5O2
+ 14H2O + 5O2
2KMnO4 + 3H2SO4 + 5H2O2 = 2MnSO4
+ 8H2O + 5O2 + K2SO4
+ K2SO4
Пример 3. Составьте уравнение реакции пероксида
водорода с йодидом натрия в растворе в
присутствии гидроксида натрия.
| 3 |
6 |
HO2 + H2O + 2e– = 3OH + H2O + 2e– = 3OH |
| 1 |
2 |
I +
6OH +
6OH – 6e– = IO3 – 6e– = IO3 + 3H2O + 3H2O |
3HO2 +
I
+
I = 3OH
= 3OH + IO3
+ IO3
3NaHO2 + NaI = 3NaOH + NaIO3
Без учета реакции нейтрализации между
гидроксидом натрия и пероксидом водорода это
уравнение часто записывают так:
3H2O2 + NaI = 3H2O + NaIO3
(в присутствии NaOH)
Это же уравнение получится, если сразу (на
стадии составления баланса) не принимать во
внимание образование гидропероксид-ионов.
Пример 4. Составьте уравнение реакции,
протекающей при добавлении диоксида свинца к
раствору пероксида водорода в присутствии
гидроксида калия.
Диоксид свинца PbO2 – очень сильный
окислитель, особенно в кислотной среде.
Восстанавливаясь в этих условиях, он образует
ионы Pb2 . В щелочной
среде при восстановлении PbO2 образуются
ионы [Pb(OH)3]
. В щелочной
среде при восстановлении PbO2 образуются
ионы [Pb(OH)3] .
.
| 1 |
PbO2 + 2H2O + 2e– =
[Pb(OH)3] + OH + OH |
| 1 |
HO2 + OH + OH – 2e–
= O2 + H2O – 2e–
= O2 + H2O |
PbO2 + H2O + HO2 = [Pb(OH)3]
= [Pb(OH)3] + O2
+ O2
Без учета образования гидропероксид-ионов
уравнение записывается так:
PbO2 + H2O2 + OH = [Pb(OH)3]
= [Pb(OH)3] + O2
+ O2 + 2H2O
+ 2H2O
Если по условию задания добавляемый раствор
пероксида водорода был щелочным, то молекулярное
уравнение следует записывать так:
PbO2 + H2O + KHO2 = K[Pb(OH)3]
+ O2
Если же в реакционную смесь, содержащую щелочь,
добавляется нейтральный раствор пероксида
водорода, то молекулярное уравнение может быть
записано и без учета образования гидропероксида
калия:
PbO2 + KOH + H2O2 = K[Pb(OH)3]
+ O2
18.6. ОВР дисмутации и
внутримолекулярные ОВР
Среди окислительно-восстановительных реакций
выделяют реакции дисмутации (диспропорционирования,
самоокисления-самовосстановления).
| Реакции дисмутации – ОВР, в которых
часть атомов одного и того же элемента в одной и
той же степени окисления восстанавливается, а
часть – окисляется. |
Примером известной вам реакции дисмутации
является реакция хлора с водой:
Cl2 + H2O 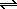 HCl + HClO
HCl + HClO
В этой реакции половина атомов хлора(0)
окисляется до степени окисления +I, а вторая
половина восстанавливается до степени окисления
–I:
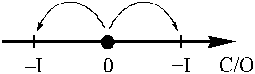
Составим методом электронно-ионного баланса
уравнение аналогичной реакции, протекающей при
пропускании хлора через холодный раствор щелочи,
например KOH:
| 1 |
Cl2 + 2e– = 2Cl |
| 1 |
Cl2 + 4OH – 2e– = 2ClO – 2e– = 2ClO + 2H2O + 2H2O |
2Cl2 + 4OH = 2Cl
= 2Cl + 2ClO
+ 2ClO + 2H2O
+ 2H2O
Все коэффициенты в этом уравнении имеют общий
делитель, следовательно:
Cl2 + 2OH = Cl
= Cl + ClO
+ ClO + H2O
+ H2O
Cl2 + 2KOH = KCl + KClO + H2O
Дисмутация хлора в горячем растворе протекает
несколько иначе:
| 5 |
10 |
Cl2 + 2e– = 2Cl |
| 1 |
2 |
Cl2 + 12OH – 10e– = 2ClO3 – 10e– = 2ClO3 + 6H2O + 6H2O |
3Cl2 + 6OH = 5Cl
= 5Cl + ClO3
+ ClO3 + 3H2O
+ 3H2O
3Cl2 + 6KOH = 5KCl + KClO3 + 3H2O
Большое практическое значение имеет
дисмутация диоксида азота при его реакции c водой
(а) и с растворами щелочей (б):
| а) |
1 |
NO2 + 3H2O – e– = NO3 + 2H3O + 2H3O |
б) |
1 |
NO2 + 2OH – e– = NO3 – e– = NO3 + H2O + H2O |
| |
1 |
NO2 + H2O + e– = HNO2
+ OH |
|
1 |
NO2 + e– = NO2 |
| |
2NO2 + 2H2O
= NO3 + H3O + H3O + HNO2 + HNO2 |
|
2NO2 + 2OH = NO3 = NO3 + NO2 + NO2 + H2O + H2O |
| |
2NO2 + H2O
= HNO3 + HNO2 |
|
2NO2 + 2NaOH = NaNO3
+ NaNO2 + H2O |
Реакции дисмутации протекают не только в
растворах, но и при нагревании твердых веществ,
например, хлората калия:
4KClO3 = KCl + 3KClO4
| 1 |
2 |
Cl+V + 6e– = Cl–I |
| 3 |
6 |
Cl+V – 2e– = Cl+VII |
Еще один тип реакций, протекающих при
нагревании твердых веществ –
внутримолекулярные ОВР.
| Внутримолекулярные ОВР – ОВР, в
которых атомы-окислители и атомы-восстановители
входят в состав одного и того же вещества. |
Характерным и очень эффектным примером
внутримолекулярной ОВР является реакция
термического разложения дихромата аммония (NH4)2Cr2O7.
В этом веществе атомы азота находятся в своей
низшей степени окисления (–III), а атомы хрома – в
высшей (+VI). При комнатной температуре это
соединение вполне устойчиво, но при нагревании
интенсивно разлагается. При этом хром(VI)
переходит в хром(III) – наиболее устойчивое
состояние хрома, а азот(–III) – в азот(0) – также
наиболее устойчивое состояние. С учетом числа
атомов в формульной единице уравнения
электронного баланса:
1 |
2Cr+VI + 6e– = 2Cr+III |
1 |
2N–III – 6e– = N2, |
а само уравнение реакции:
(NH4)2Cr2O7 = Cr2O3
+ N2 + 4H2O
+ 4H2O .
.
Другой важный пример внутримолекулярной ОВР –
термическое разложение перхлората калия KClO4.
В этой реакции хлор(VII), как и всегда, когда он
выступает в роли окислителя, переходит в хлор(–I),
окисляя кислород(–II) до простого вещества:
| 1 |
4 |
Cl+VII + 8e– = Cl–I |
| 2 |
8 |
2O–II – 4e– = O2 |
и, следовательно, уравнение реакции
KClO4 = KCl + 2O2
Аналогично разлагается при нагревании и хлорат
калия KClO3, если разложение проводить в
присутствии катализатора (MnO2): 2KClO3 =
2KCl + 3O2
В отсутствие катализатора протекает реакция
дисмутации.
К группе внутримолекулярных ОВР относятся и
реакции термического разложения нитратов.
Обычно процессы, протекающие при нагревании
нитратов довольно сложны, особенно в случае
кристаллогидратов. Если в кристаллогидрате
молекулы воды удерживаются слабо, то при слабом
нагревании происходит обезвоживание нитрата
[например, LiNO3.3H2O и Ca(NO3)2 4H2O обезвоживаются до LiNO3
и Ca(NO3)2], если же вода связана прочнее
[как, например, в Mg(NO3)2.6H2O и
Bi(NO3)3.5H2O], то происходят
своего рода реакции " внутримолекулярного
гидролиза" с образованием основных солей –
гидроксид-нитратов [Mg(NO3)OH и Bi(NO3)2OH],
которые при дальнейшем нагревании могут
переходить в оксид-нитраты {[Be4(NO3)6O]
и [Bi6O6](NO3)6}, последние при
более высокой температуре разлагаются до
оксидов.
4H2O обезвоживаются до LiNO3
и Ca(NO3)2], если же вода связана прочнее
[как, например, в Mg(NO3)2.6H2O и
Bi(NO3)3.5H2O], то происходят
своего рода реакции " внутримолекулярного
гидролиза" с образованием основных солей –
гидроксид-нитратов [Mg(NO3)OH и Bi(NO3)2OH],
которые при дальнейшем нагревании могут
переходить в оксид-нитраты {[Be4(NO3)6O]
и [Bi6O6](NO3)6}, последние при
более высокой температуре разлагаются до
оксидов.
Безводные нитраты при нагревании могут
разлагаться до нитритов (если они существуют и
при этой температуре еще устойчивы), а нитриты –
до оксидов. Если нагревание проводится до
достаточно высокой температуры, или
соответствующий оксид малоустойчив (Ag2O, HgO),
то продуктом термического разложения может быть
и металл (Cu, Cd, Ag, Hg).
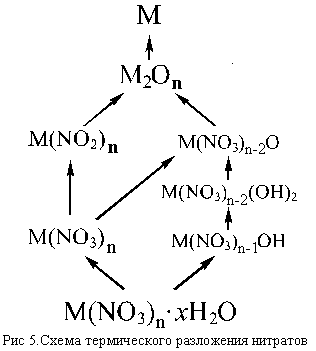
Несколько упрощенная схема термического
разложения нитратов показана на рис. 5.
Примеры последовательных превращений,
протекающих при нагревании некоторых нитратов
(температуры приведены в градусах Цельсия):
KNO3 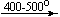 KNO2
KNO2 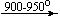 K2O;
K2O;
Ca(NO3)2.4H2O 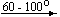 Ca(NO3)2
Ca(NO3)2 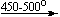 Ca(NO2)2
Ca(NO2)2 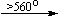 CaO;
CaO;
Mg(NO3)2.6H2O 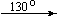 Mg(NO3)(OH)
Mg(NO3)(OH) 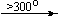 MgO;
MgO;
Cu(NO3)2.6H2O 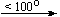 Cu(NO3)2
Cu(NO3)2  CuO
CuO 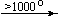 Cu2O
Cu2O 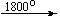 Cu;
Cu;
Bi(NO3)3.5H2O 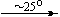 Bi(NO3)2(OH)
Bi(NO3)2(OH) 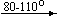 Bi(NO3)(OH)2
Bi(NO3)(OH)2 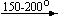 [Bi6O6](NO3)6
[Bi6O6](NO3)6 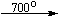 Bi2O3.
Bi2O3.
Несмотря на сложность происходящих процессов,
при ответе на вопрос, что получится при "
прокаливании" (то есть при температуре 400 – 500 oС)
соответствующего безводного нитрата, обычно
руководствуются следующими предельно
упрощенными правилами:
1) нитраты наиболее активных металлов (в ряду
напряжений – левее магния) разлагаются до
нитритов;
2) нитраты менее активных металлов (в ряду
напряжений – от магния до меди) разлагаются до
оксидов;
3) нитраты наименее активных металлов (в ряду
напряжений – правее меди) разлагаются до
металла.
Используя эти правила, следует помнить, что в
таких условиях
LiNO3 разлагается до оксида,
Be(NO3)2 разлагается до оксида при более
высокой температуре,
из Ni(NO3)2 помимо NiO может получиться и
Ni(NO2)2,
Mn(NO3)2 разлагается до Mn2O3,
Fe(NO3)2 разлагается до Fe2O3;
из Hg(NO3)2 кроме ртути может получиться
и ее оксид.
Рассмотрим типичные примеры реакций,
относящихся к этим трем типам:
18.7.
Окислительно-восстановительные реакции
конмутации
| ОВР конмутации – ОВР, в которых
происходит выравнивание степени окисления
атомов одного и того же элемента, находившихся до
реакции в разных степенях окисления. |
Эти реакции могут быть как межмолекулярными,
так и внутримолекулярными. Например,
внутримолекулярные ОВР, протекающие при
термическом разложении нитрата и нитрита
аммония, относятся к реакциям конмутации, так как
здесь происходит выравнивание степени окисления
атомов азота:
NH4NO3 = N2O + 2H2O
+ 2H2O (около 200 oС)
(около 200 oС)
NH4NO2 = N2 + 2H2O
+ 2H2O (60 – 70 oС)
(60 – 70 oС)
При более высокой температуре (250 – 300 oС)
нитрат аммония разлагается до N2 и NO, а при
еще более высокой (выше 300 oС) – до азота и
кислорода, и в том и в другом случае образуется
вода.
Примером межмолекулярной реакции конмутации
является реакция, протекающая при сливании
горячих растворов нитрита калия и хлорида
аммония:
NH4 +
NO2
+
NO2 = N2 + 2H2O
= N2 + 2H2O
NH4Cl + KNO2 = KCl + N2 + 2H2O
Если проводить аналогичную реакцию, нагревая
смесь кристаллических сульфата аммония и
нитрата кальция, то, в зависимости от условий,
реакция может протекать по-разному:
(NH4)2SO4 + Ca(NO3)2
= 2N2O + 4H2O + CaSO4 (t < 250 oC)
(NH4)2SO4 + Ca(NO3)2 = 2N2
+ O2 + 4H2O + CaSO4 (t > 250 oС)
7(NH4)2SO4 + 3Ca(NO3)2 = 8N2
+ 18H2O + 3CaSO4 + 4NH4HSO4 (t > 250 oС)
Первая и третья из этих реакций – реакции
конмутации, вторая – более сложная реакция,
включающая как конмутацию атомов азота, так и
окисление атомов кислорода. Какая из реакций
будет протекать при температуре выше 250 oС,
зависит от соотношения реагентов.
Реакции конмутации, приводящие к образованию
хлора, протекают при обработке соляной кислотой
солей кислородсодержащих кислот хлора, например:
6HCl + KClO3 = KCl + 3Cl2 + 3H2O
Также по реакции конмутации образуется сера из
газообразных сероводорода и диоксида серы:
2H2S + SO2 = 3S + 2H2O
ОВР конмутации довольно многочисленны и
разнообразны – к ним относятся даже некоторые
кислотно-основные реакции, например:
NaH + H2O = NaOH + H2.
Для составления уравнений ОВР конмутации
используется как электронно-ионный, так и
электронный баланс, в зависимости от того, в
растворе протекает данная реакция или нет.
18.8. Электролиз
Изучая главу IX, вы познакомились с электролизом
расплавов различных веществ. Так как подвижные
ионы присутствуют и в растворах, электролизу
могут быть подвергнуты также растворы различных
электролитов.
Как при электролизе расплавов, так и при
электролизе растворов, обычно используют
электроды, изготовленные из материала, не
вступающего в реакцию (графита, платины и т. п.), но
иногда электролиз проводят и с "
растворимым" анодом. " Растворимый" анод
используют в тех случаях, когда необходимо
получить электрохимическим способом соединение
элемента, из которого изготовлен анод. При
электролизе имеет большое значение разделены
анодное и катодное пространство, или электролит
в процессе реакции перемешивается – продукты
реакции в этих случаях могут оказаться разными.
Рассмотрим важнейшие случаи электролиза.
1. Электролиз расплава NaCl. Электроды инертные
(графитовые), анодное и катодное пространства
разделены. Как вы уже знаете, в этом случае на
катоде и на аноде протекают реакции:
K: Na + e–
= Na
+ e–
= Na
A: 2Cl – 2e– = Cl2
– 2e– = Cl2
Записав таким образом уравнения реакций ,
протекающих на электродах, мы получаем
полуреакции, с которыми можем поступать точно
так же, как в случае использования метода
электронно-ионного баланса:
| 2 |
K: |
Na + e–
= Na + e–
= Na |
| 1 |
A: |
2Cl – 2e– = Cl2
– 2e– = Cl2 |
Сложив эти уравнения полуреакций, получаем
ионное уравнение электролиза
2Na + 2Cl
+ 2Cl
 2Na + Cl2
2Na + Cl2
а затем и молекулярное
2NaCl  2Na + Cl2
2Na + Cl2
В этом случае катодное и анодное пространства
должны быть разделены для того, чтобы продукты
реакции не реагировали между собой. В
промышленности эта реакция используется для
получения металлического натрия.
2. Электролиз расплава K2CO3.
Электроды инертные (платиновые). Катодное и
анодное пространства разделены.
4K+ + 2CO32
 4K + 2CO2
4K + 2CO2 + O2
+ O2
2K2CO3  4K + 2CO2
4K + 2CO2
 + O2
+ O2
3. Электролиз воды (H2O). Электроды
инертные.
| 2 |
K: |
2H3O + 2e– = H2 + 2H2O + 2e– = H2 + 2H2O |
| 1 |
A: |
4OH – 4e– = O2 + 2H2O
– 4e– = O2 + 2H2O |
4H3O +
4OH
+
4OH
 2H2
2H2 + O2
+ O2 + 6H2O
+ 6H2O
2H2O  2H2
2H2 + O2
+ O2
Вода – очень слабый электролит, в ней
содержится очень мало ионов, поэтому электролиз
чистой воды протекает крайне медленно.
4. Электролиз раствора CuCl2. Электроды
графитовые. В системе присутствуют катионы Cu2 и H3O
и H3O , а также анионы Cl
, а также анионы Cl и OH
и OH .
Ионы Cu2
.
Ионы Cu2 более
сильные окислители, чем ионы H3O
более
сильные окислители, чем ионы H3O (см. ряд напряжений),
поэтому на катоде прежде всего будут разряжаться
ионы меди, и только, когда их останется очень
мало, будут разряжаться ионы оксония. Для анионов
можно руководствоваться следующим правилом:
(см. ряд напряжений),
поэтому на катоде прежде всего будут разряжаться
ионы меди, и только, когда их останется очень
мало, будут разряжаться ионы оксония. Для анионов
можно руководствоваться следующим правилом:
При электролизе растворов простые
(одноатомные) анионы разряжаются (окисляются)
раньше, чем сложные (многоатомные) ионы.
Следовательно в нашем случае на анода будут
разряжаться хлоридные ионы.
| 1 |
K: |
Cu2 +
2e– = Cu +
2e– = Cu |
| 1 |
A: |
2Cl – 2e– = Cl2
– 2e– = Cl2 |
Cu2 + 2Cl
+ 2Cl
 Cu + Cl2
Cu + Cl2
CuCl2  Cu + Cl2
Cu + Cl2
5. Электролиз раствора CuSO4. Электроды
графитовые.
В водных растворах за счет автопротолиза воды
(2H2O 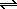 H3O
H3O + OH
+ OH )
всегда в незначительном количестве присутствуют
ионы H3O
)
всегда в незначительном количестве присутствуют
ионы H3O и OH
и OH . В случае соли,
содержащей сложный анион, вместо него
разряжаются гидроксид-ионы (4OH
. В случае соли,
содержащей сложный анион, вместо него
разряжаются гидроксид-ионы (4OH – 4e– = O2 + 2H2O),
равновесие автопротолиза воды смещается, и в
анодном пространстве накапливаются ионы
оксония. Суммарное уравнение полуреакции в
анодном пространстве: 6H2O – 4e– = O2
+ 4H3O
– 4e– = O2 + 2H2O),
равновесие автопротолиза воды смещается, и в
анодном пространстве накапливаются ионы
оксония. Суммарное уравнение полуреакции в
анодном пространстве: 6H2O – 4e– = O2
+ 4H3O . В рамках
теории электролитической диссоциации это
уравнение записывают следующим образом: 2H2O
– 4e– = O2 + 4H
. В рамках
теории электролитической диссоциации это
уравнение записывают следующим образом: 2H2O
– 4e– = O2 + 4H .
Таким образом, для нашего случая получаем (слева
– в рамках протолитической теории, справа – в
рамках теории электролитической диссоциации):
.
Таким образом, для нашего случая получаем (слева
– в рамках протолитической теории, справа – в
рамках теории электролитической диссоциации):
На катоде выделяется медь, на аноде – кислород,
а в растворе накапливается серная кислота.
Ионы металлов, стоящих в ряду напряжений правее
водорода, при электролизе растворов солей разряжаются.
В принципе ионы металлов, стоящих в ряду
напряжений левее водорода, при электролизе
водных растворов не должны разряжаться. В этих
случаях должен был бы выделяться водород.
Практически, из-за специфических особенностей
разряда ионов водорода, при электролизе
выделяются и более активные металлы.
Ионы металлов, стоящих в ряду напряжений между
алюминием и водородом при электролизе
растворов солей разряжаются вместе с водородом.
При этом, чем активнее металл, тем больше
водорода выделяется, и тем большая часть
электрической энергии расходуется бесполезно.
6. Электролиз раствора NiBr2. Электроды
графитовые. Катодное и анодное пространства
разделены.
| 1 |
K: |
Ni2 +
2e– = Ni +
2e– = Ni |
| 1 |
A: |
2Br – 2e– = Br2
– 2e– = Br2 |
Ni2 +2Br
+2Br
 Ni + Br2
Ni + Br2
NiBr2  Ni + Br2
Ni + Br2
Одновременно с этим на катоде выделяется
водород, в растворе накапливаются
гидроксид-ионы, и, как следствие, протекает
побочная реакция образования нерастворимого
гидроксида никеля.
Ионы металлов, стоящие в ряду напряжений до
алюминия при электролизе не разряжаются.
7. Электролиз раствора Na2SO4.
Электроды платиновые. Раствор перемешивается.
В этом случае на катоде разряжаются не ионы
натрия, а ионы оксония (2H3O + 2e– = H2 + 2H2O),
равновесие автопротолиза воды смещается, в
катодном пространстве накапливаются
гидроксид-ионы. Суммарное уравнение реакции в
катодном пространстве: 2H2O + 2e– = H2
+ 2OH
+ 2e– = H2 + 2H2O),
равновесие автопротолиза воды смещается, в
катодном пространстве накапливаются
гидроксид-ионы. Суммарное уравнение реакции в
катодном пространстве: 2H2O + 2e– = H2
+ 2OH .
.
| 2 |
K: |
2H2O + 2e– = H2 + 2OH |
| 1 |
A: |
6H2O – 4e– = O2 + 4H3O |
10H2O  2H2
2H2 + O2
+ O2 + 4OH
+ 4OH + 4H3O
+ 4H3O
Так как раствор перемешивается, происходит
реакция нейтрализации. В итоге получаем
2H2O  2H2
2H2 + O2
+ O2
то есть, реакцию электролиза воды. При
электролизе воды для повышения ее
электропроводности в нее специально добавляют
соли с неразряжающимися катионами и анионами,
что значительно ускоряет процесс электролиза.
8. Электролиз раствора CuSO4. Анод медный.
| 1 |
K: |
Cu2 +
2e– = Cu +
2e– = Cu |
| 1 |
A: |
Cu – 2e– = Cu2 |
В результате сложения уравнений полуреакций мы
можем прийти к ошибочному выводу, что ничего не
происходит. На самом деле эти полуреакции
описывают реальный технологический процесс
электролитического рафинирования (очистки) меди:
с катода, содержащего примеси на анод переходят
только ионы меди.




