|
Планирование многостадийных синтезов./ Органическая химия
Анализ ретронов типа II.
Расчленение ретронов типа II лучше
всего проводить на базе трансформов
алкилирования енолятов или эпоксидов
(необходима тактика FGA), Михаэля и Дильса-Альдера.
В последнем случае анализ должен включать
трансформ сочленения (R). Эти подходы
резюмированы в таблице 2.
Таблица 2.
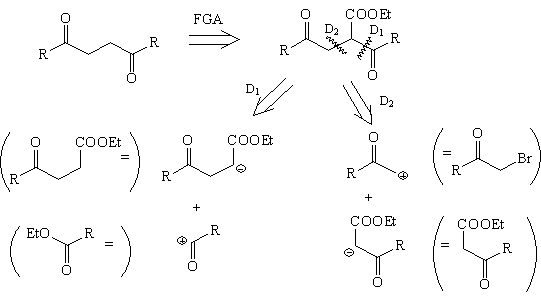
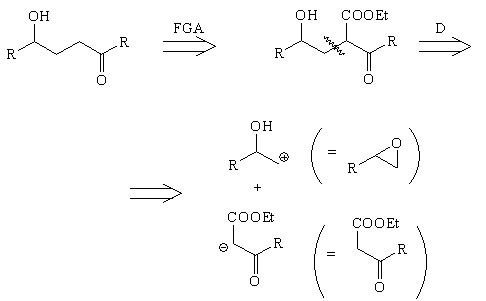
1,4-ретрон
1,5-ретрон
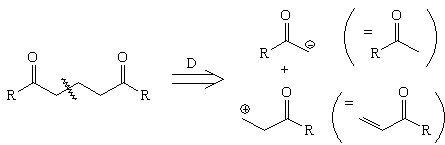
1,6-ретрон
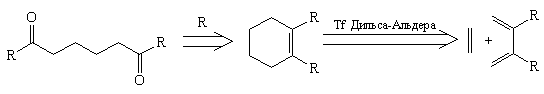
Как видно из табл.2, при анализе 1,4-ретрона
используется трансформ FGA. В результате
возникает новый 1,4-ретрон (ему соответствует
расчленение D2) и 1,3-ретрон (ему
соответствует расчленение D1).
Анализ (расчленение D1)
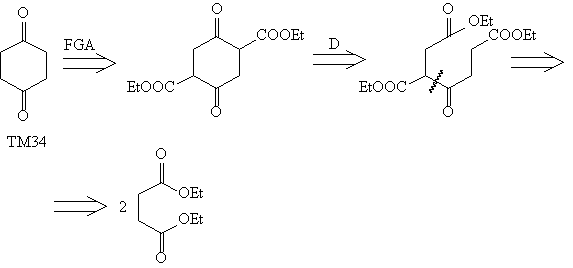
Синтез [67]
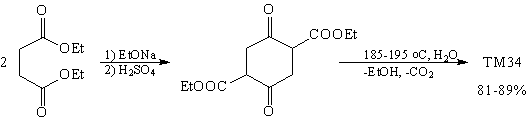
Анализ (расчленение D2)
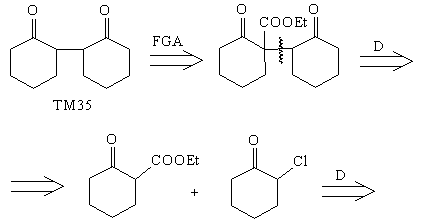
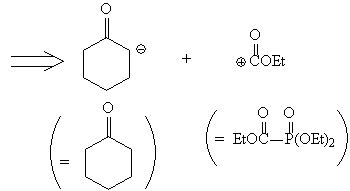
Синтез [68, 69]
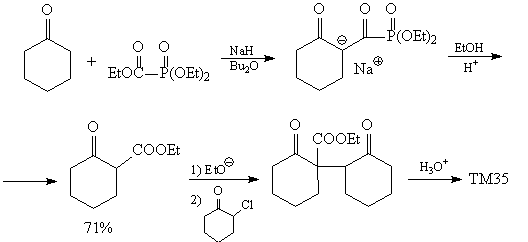
1,5-Дикарбонильный ретрон предполагает
расчленение с помощью трансформа Михаэля. Этот
ретрон появляется в анализе кетона
Виланда-Мишера (ТМ36) - важного билдинг-блока в
синтезе стероидов [70] и терпеноидов [71].
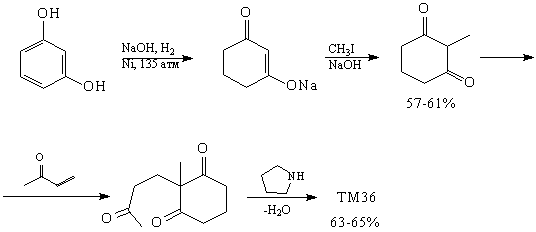
В ТМ36 присутствует ретрон альдольной
конденсации, в соответствии с которым и следует
провести первое расчленение.
Анализ
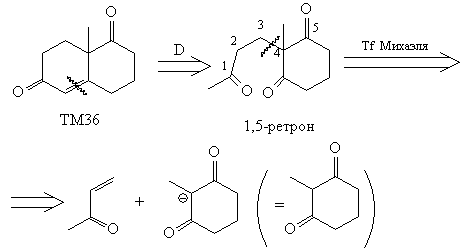
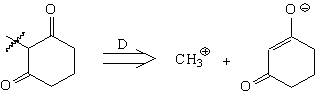
Синтез[72, 73]
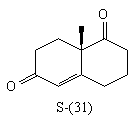
Если на стадии альдольной конденсации вместо
пирролидина использовать S-(-)-пролин, получается
в основном один (S)-стереоизомер кетона
Виланда-Мишера (31) [74]:
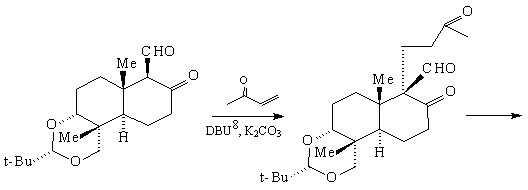
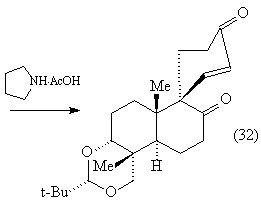
Сочетание реакции Михаэля с альдольной
конденсацией было использовано также для
спиро-аннелирования. Так было получено
соединение (32) - промежуточное вещество в синтезе
афидиколина - потенциального противовирусного и
антимитотического агента [75].
Анализ 1,6-ретрона, включающий трансформ
сочленения (R) уже встречался на примере ТМ9 (см.
выше), где решающим моментом в создании структуры
и ее стереохимии было сочетание реакции
Дильса-Альдера и озонолиза (см. с.22).
Соединение ТМ37 было использовано как
интермедиат в синтезе ювенильного гормона
мотылька cecropia.
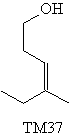
Это соединение содержит трудно создаваемый
фрагмент - двойную связь с Z-конфигурацией.
Число атомов углерода, составляющих цис-фрагмент
молекулы, равно 6, что позволяет использовать
тактику, базирующуюся на 1,6-ретроне. Анализ
становится понятным после трансформа FGA -
добавлении еще одной гидроксильной группы.
Анализ
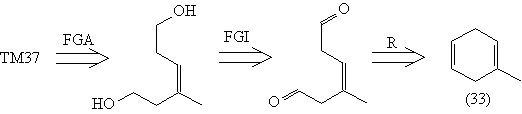
Трансформ сочленения (R) соответствует в данном
случае реакции озонолиза соединения (33). Для того,
чтобы сделать однозначным озонолиз именно
необходимой (левой) С=С связи, необходимо ввести
электронодонорную группу, облегчающую
окисление:
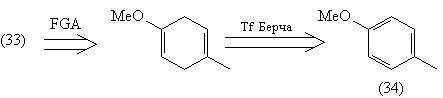
Таким бразом, анализ привел нас к доступному
соединению - метиловому эфиру п-крезола (34).
Синтез [76]
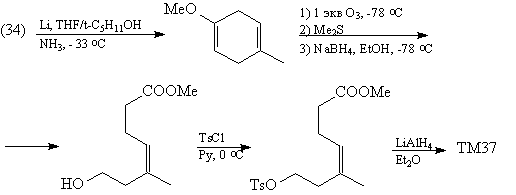
|