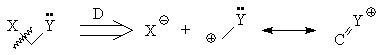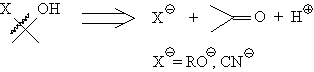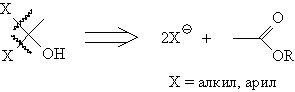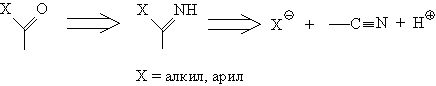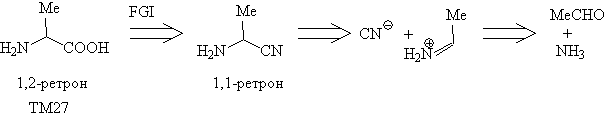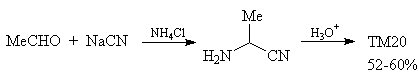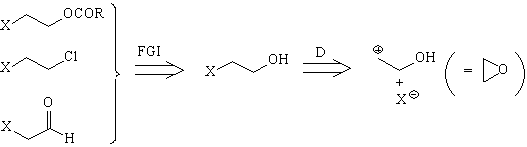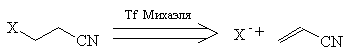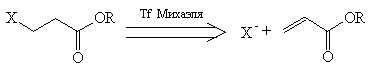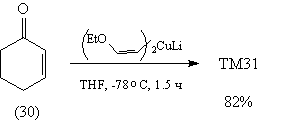|
Планирование многостадийных синтезов./ Органическая химия
Анализ ретронов типа I
Расчленение 1,1-ретрона всегда
приводит к карбонильной группе или ее аналогу:
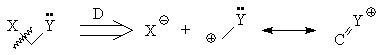
Основные случаи расчленения 1,1-ретрона приведены на схеме 2.
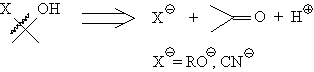
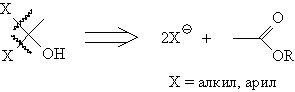
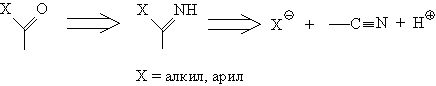
Схема 2. Расчленения 1,1-ретрона.
Иногда в анализе полезно 1,2-ретрон превратить в
1,1-ретрон с помощью трансформа FGI, как, например, в
случае ТМ26.
Анализ
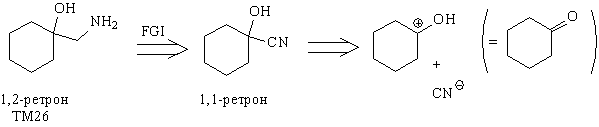
Синтез [56]
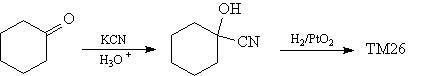
Другой аналогичный пример
1,1-ретрона, сводящегося к карбонильному
соединению - анализ  -аминокислот. -аминокислот.
Анализ
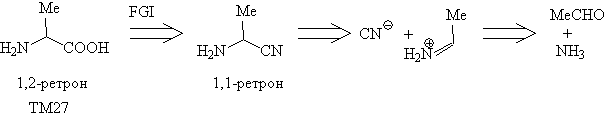
Синтез (реакция Штреккера) [57]
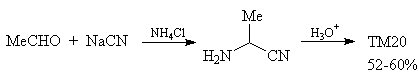
Анализ 1,2-ретрона лучше всего
базировать на спиртах. Для этого, прежде всего с
помощью трансформа FGI необходимо получить
концевую ОН-группу. Наиболее продуктивной
тактикой дальнейших расчленений является
трансформ раскрытия оксиранового (эпоксидного)
цикла. В случае  -замещенных
карбонильных соединений прибегают к тактике -замещенных
карбонильных соединений прибегают к тактике  -галогенирования или -галогенирования или  -алкилирования
кетона (схема 3). -алкилирования
кетона (схема 3).
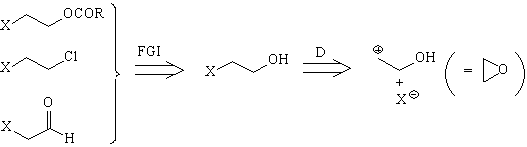
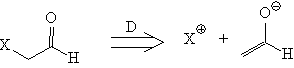
Схема 3. Расчленения 1,2-ретрона.
Структурным фрагментом многих
лекарственных препаратов являются производные
2-диалкиламиноэтанолов, например:
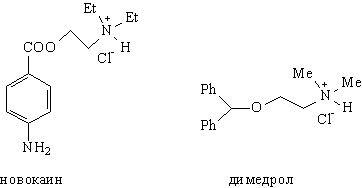
Их синтез основан именно на раскрытии цикла
окиси этилена.
Рассмотрим аналог азотистого
иприта ТМ28 - противоракового препарата, действие
которого основано на прерывании синтеза белка за
счет выраженной способности ТМ28 алкилировать
группы ОН и NH2 (анхимерное содействие атома
N). В соответствии со сказанным выше, вначале
следует применить трансформ FGI, так как в
молекуле ТМ28 присутствует 1,2-ретрон (выделенные
связи).
Анализ
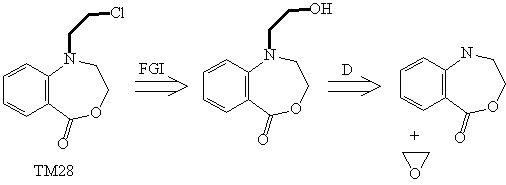
Полученное соединение также содержит 1,2-ретрон.
Для того чтобы использовать тактику,
базирующуюся на окиси этилена, следует вначале
прибегнуть к трансформу этерификации (RGD):
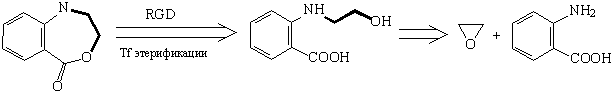
Мы пришли к
доступным соединениям - окиси этилена и
антраниловой кислоте. Теперь можно написать
схему синтеза. Удивительно, но синтез
оказывается намного проще, чем можно было
предположить, взглянув на формулу ТМ28.
Синтез [58]
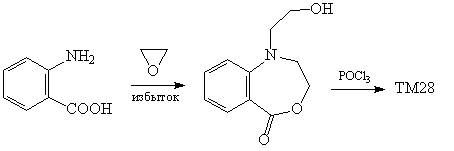
Здесь уместно сделать замечание относительно
реакций внутримолекулярной циклизации. Такие
реакции термодинамически выгодны.
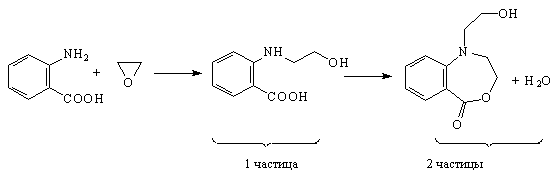
Циклизация происходит легко, поскольку этому
благоприятствует энтропийный фактор (увеличение
числа частиц).
Продуктивные расчленения
1,3-ретрона

могут быть проведены только на "карбонильном
уровне", т.е. одной из групп Х, Y должен быть
карбонильный атом О (либо атом N цианогруппы).
Основной тактикой при этом является трансформ
Михаэля.
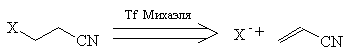
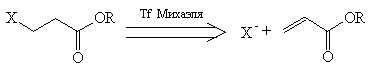
Так, при анализе соединения ТМ29 вначале следует
перейти именно на "карбонильный уровень".
Дальнейшее расчленение после этого очевидно.
Анализ
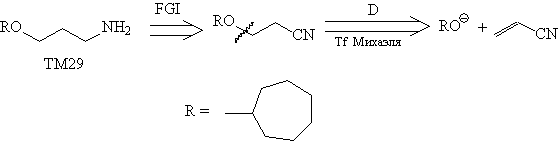
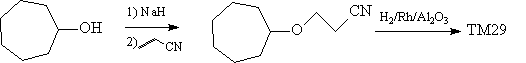
Акрилонитрил - доступное соединение, и синтез
наиболее рационально базировать на нем.
Синтез [59]
На базе производных акриловой
кислоты можно проводить расчленения и других
соединений, в которых, на первый взгляд, не виден
1,3-ретрон. Полезно помнить об эквивалентности (в
плане синтеза) таких групп:
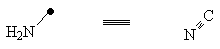
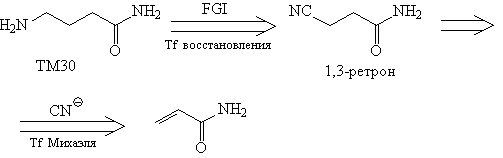
С этой точки зрения к 1,3-ретрону сводится анализ
ТМ23 - лекарственного препарата, обладающего
ноотропным действием. Если мы увидим, что
аминогруппа в ТМ30 сводится к нитрилу, то
дальнейший ход анализа становится понятным.
Анализ
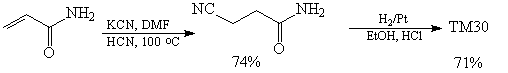
Учитывая, что акриламид - доступное
соединение, синтез ТМ30 можно представить
следующей схемой.
Синтез [60]
Большие возможности в анализе
1,3-ретрона предоставляет использование
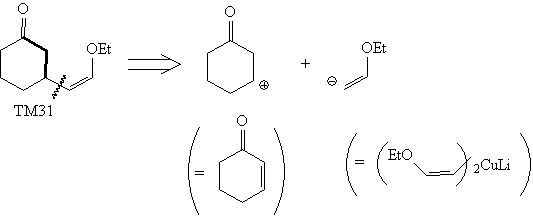
медьорганических реагентов. В соединении ТМ31
связи С-С, входящие в состав 1,3-ретрона, выделены:
Анализ
Синтез [61]
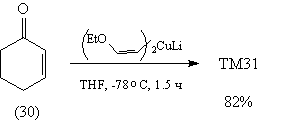
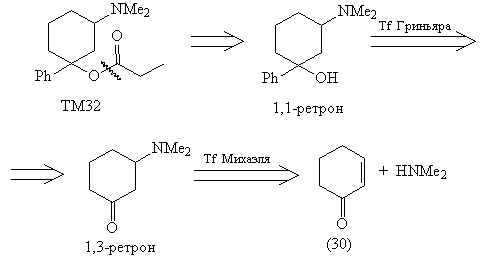
К тому же исходному соединению
приводит анализ анальгетика - соединения ТМ32.
Начиная с расчленения наиболее лабильной связи,
мы приходим к 1,1-ретрону - ретрону Гриньяра.
Расчленение этого ретрона приводит к 1,3-рeтрону.
Анализ
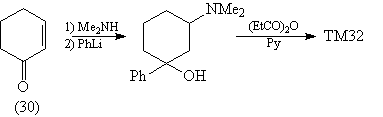
Тогда синтез ТМ32 будет выглядеть следующим
образом.
Синтез [62]
Поскольку 2-циклогексенон (30) часто
встречается как исходное соединение во многих
синтезах, полезно запомнить методы его
получения.
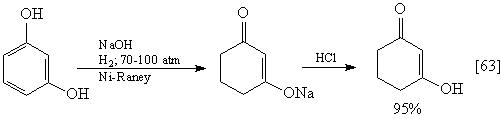
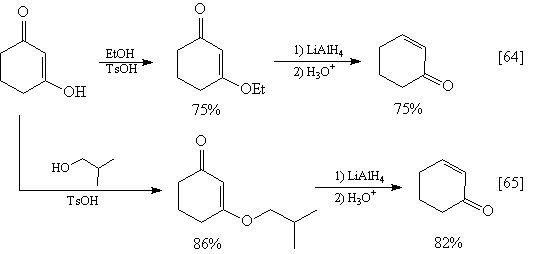
Расчленение 1,3-ретрона можно
проводить также, основываясь на реакции
карбокуприрования алкинов.
Анализ
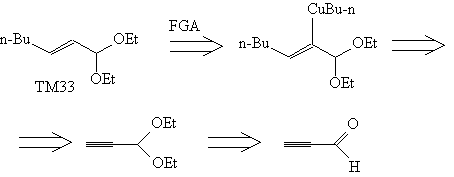
Синтез [66]
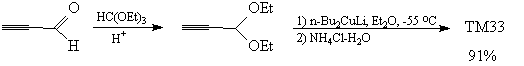
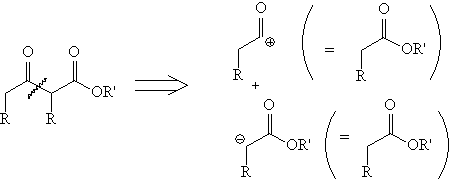
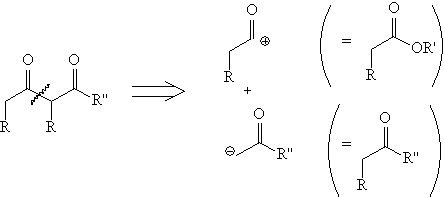
Не следует забывать и о
классическом варианте анализа
1,3-дикарбонильного ретрона, основанном на
сложноэфирной конденсации либо на конденсации
по Кляйзену:
|