|
Урок 43. Азотная кислота
Новое содержание: азотная кислота
Методические рекомендации учителю: Главное внимание на уроке следует уделить особенностям взаимодействия азотной кислоты с металлами. Следует подчернуть, что при реакциях азотной кислоты с металлами водород не выделяется, а происходит восставновление атома азота, входящего в состав кислотного остатка. Чем активнее металл и чем ниже концентрация кислоты, тем полнее протекает восстановление. (смотри схему в тексте параграфа). В качестве иллюстрации влияния концентрации азотной кислоты на состав продуктов восстановления можно привести следующие уравнения реакций:
Zn + 4HNO3 конц = Zn(NO3)2 + 2NO2 + H2O,
3Zn + 8HNO3 (40%) = 3Zn(NO3)2 + 2NO + 4H2O,
4Zn + 10HNO3 (20%) = 4Zn(NO3)2 + N2O + 5H2O,
5Zn + 12HNO3 (6%) = 4Zn(NO3)2 + N2 + 6H2O,
4Zn + 10HNO3 (0,5%) = 4Zn(NO3)2 + NH4NO3 + 3H2O.
Обычно образуются сложные смеси продуктов восстановления.
Можно отметить, что концентрированная азотная кислота реагирует практически с любым металлам с выделением оксида азота(IV). Это связано с наличием в ней катиона нитрония NO2+. Он образуется при аутодиссоциации молекулы HNO3:
2HNO3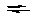 NO2+ + NO3– + H2O. Присоединяя электрон, катион нитроила превращается в оксид азота(IV). Строго говоря, некоторые металлы (магний,марганец) реагируют с разбавленной азотной кислотой с выделением водорода, об этом подробнее см. в книге И. А. Леенсон, Занимательная химия, ч. 1, М.: Дрофа, 1996, с. 116. NO2+ + NO3– + H2O. Присоединяя электрон, катион нитроила превращается в оксид азота(IV). Строго говоря, некоторые металлы (магний,марганец) реагируют с разбавленной азотной кислотой с выделением водорода, об этом подробнее см. в книге И. А. Леенсон, Занимательная химия, ч. 1, М.: Дрофа, 1996, с. 116.
Планируемые результаты обучения: знать особенности реакций азотной кислоты с металлами,
Лабораторный опыт: Изучение электропроводности растворов и движения ионов в электрическом поле
Демонстрации: Взаимодействие с медью концентрированной и разбавленной азотной кислоты, вспышка скипидара с дымящей азотной кислотой, взаимодействие угля с расплавленной селитрой, разложение нитратов свинца и серебра
Задание: §48, § 47 для дополнительного чтения
| 
