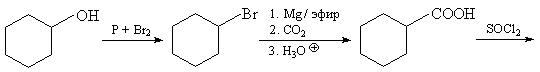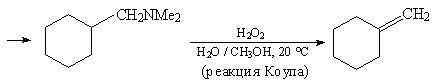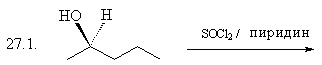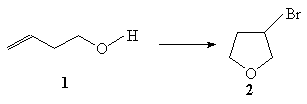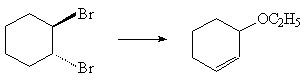И.Г.Болесов, Г.С.Зайцева
Нуклеофильное замещение и элиминирование.
Методическая разработка
Контрольная работа N6
1.Осуществите следующие превращения:
1.1. н-пропиловый спирт 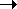 3-хлорогексан,
3-хлорогексан,
1.2. н-пропиловый спирт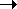 4-этилгептанол-4,
4-этилгептанол-4,
1.3. н-пропиловый спирт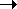 2-метил-2-хлоропентан,
2-метил-2-хлоропентан,
1.4. трет-бутиловый спирт 2,5-диметилгексанол-3,
2,5-диметилгексанол-3,
1.5. транс-3-этилциклопентанол- 1 цис-3-этил-1-хлороциклопентан,
1 цис-3-этил-1-хлороциклопентан,
1.6. н-пропиловый спирт  окись пропилена
окись пропилена 1-метоксипропанол-2,
1-метоксипропанол-2,
1.7. 1-фенилциклогексен 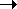 транс-2-фенилциклогексанол-1,
транс-2-фенилциклогексанол-1,
1.8. этилен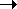 3-бутинол-1,
3-бутинол-1,
1.9. этилен 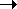 3-бутенол-1.
3-бутенол-1.
2.Определите структуры соединений X, Y и Z,
образующихся в ходе нижеприведенных
превращений. Приведите схемы механизмов их
образования.
н-амиловый спирт + горячая конц. H2SO4
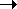 X (алкен),
X (алкен),
X + 60%-ная H2SO4 (70 oC) Y (спирт),
Y (спирт),
Y + 60%-ная H2SO4 Z (эфир серной кислоты).
Z (эфир серной кислоты).
3.Исходя из 2-метилбутанола-2 и этилена получите
3,3-диметилпентаналь-1.
4.Приведите метод синтеза ди-трет-бутилового
эфира.
5.Исходя из бромбензола, этилового спирта,
этилформиата и необходимых неорганических
реагентов, получите 1,6-дифенилпентанол-3.
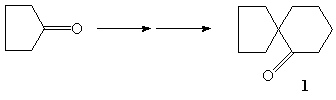
6. Осуществите в несколько стадий превращение
циклопентанона в спирокетон 1.
7.Синтезируйте из ацетилена, ацетона и
необходимых неорганических реагентов
4-бромо-2-метилбутен-2.
8.Из ацетилена, формальдегида и необходимых
неорганических реагентов получите цис-2-бутен-1,4-диол.
9.Синтезируйте из ацетилена и необходимых
неорганических реагентов цис-3-гексенол-1.
10. Исходя из бромбензола, бромциклопентана,
этилового спирта, формальдегида и необходимых
неорганических реагентов, получите
3-фенил-1-циклопентилпропанол-1.
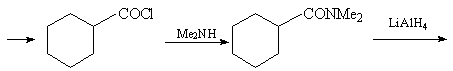
11.Исходя из метиленциклогексана и необходимых
неорганических реагентов, получите соединение 1.
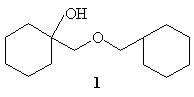
Метиленциклогексан может быть синтезирован из
циклогексанона с использованием реакции Виттига
или из доступного циклогексанола в соответствии
с нижеприведенной схемой:
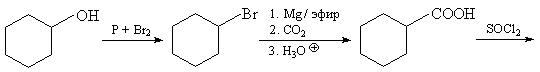
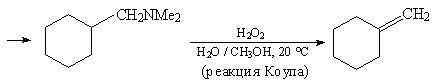
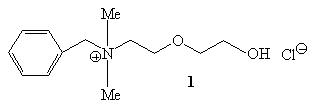
12.Исходя из диметиламина, этилового спирта,
бензальдегида и необходимых неорганических
реагентов, получите соединение 1.
13.Предложите структуры соединений 1-4 в
нижеприведенной последовательности
превращений.
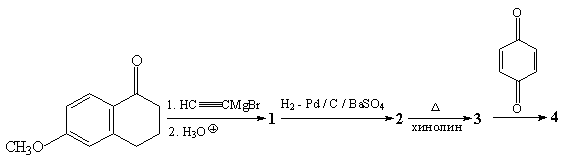
14.Исходя из ацетона, акролеина (СН2=СН-СНО)
и необходимых неорганических реагентов,
получите 1,2-диметил-4-формилциклогексен-1.
15.Синтезируйте из параформа, ацетилена, толуола
и необходимых неорганических реагентов
4-бензилокси-2-бутинол-1.
16.Приведите схему дегидратации
3-метилбутанола-2 под действием 80%серной кислоты.
Сколько алкенов образуется в результате этого
превращения. Какой из них будет, по Вашему мнению,
преобладать?
17.При нагревании 3,3-диметилбутанола-2 с 85%
фосфорной кислотой при 100 оС
образуется 80% 2,3-диметилбутена-2 и 20%
2,3-диметилбутена-1. Приведите схему механизма
образования этих продуктов. Какой тип скелетной
изомеризации осуществляется в ходе этого
протекающего по Е1 механизму превращения?
18.Приведите структуру алкена, образующегося
при нагревании (120-150 оС) гидроксида
триметил(1-метилциклогексил)аммония (1).
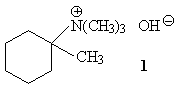
19.Укажите примерный процентный состав алкенов,
образующихся из
19.1. 2-бромо-2-метилпентана при нагревании с трет-бутилатом
калия в трет-бутиловом спирте,
19.2. 1-метил-1-хлороциклогексана при нагревании с
3-этил-пентанолятом-3 калия в 3-этилпентаноле-3.
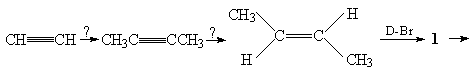
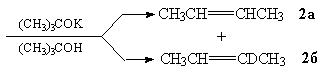
20. Укажите реагенты, необходимые для получения транс-бутена-2
из ацетилена, а также стереохимию соединений 1,
2а и 2б. Для соединения 1 приведите
формулу Фишера.
21.Приведите методы синтеза СН3-Х и (СН3)3С-Х
(где Х = F, Сl, Br, I) - важных реагентов в органическом
синтезе.
22.Исходя из ацетона, ацетилена и необходимых
неорганических реагентов, получите
2,2,5,5-тетраметилтетрагидрофуран.
23.Предложите метод синтеза мезо-4,5-октандиола,
исходя из ацетилена и пропилена.
24. Дегидробромирование 1-бромо-2-фенилэтана,
осуществляемое с помощью оснований, протекает в
7.1 раза быстрее, чем проводимое в аналогичных
условиях дегидробромирование
1-бромо-2,2-дидейтеро-2-фенилэтана.
Какие факторы, на Ваш взгляд, определяют
найденное соотношение скоростей упомянутых
реакций?
Как можно использовать эту информацию для выбора
механизма дегидробромирования, реализующегося в
приведенных выше примерах?
25. Что общего может быть между слонами и
бабочками? Оказывается, что самые крупные из
живущих на Земле животных и очень многие виды
бабочек используют один и тот же феромон. Им
оказался ацетат (Z)-7-додеценола (1). Предложите
способ получения этого интересного соединения
из ацетилена и других простых и доступных
веществ С2-С4. Как и для многих других
феромонов насекомых Z-конфигурация связи С=С
обязательна.
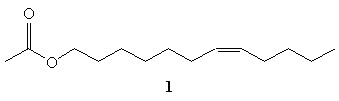
Chemistry and Biology, 1996, 3(8), 595
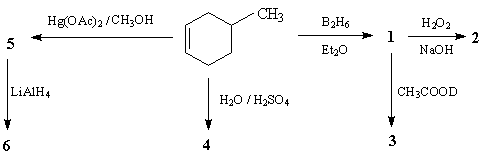
26. Напишите структурные формулы соединений,
образующихся в следующих реакциях, и укажите
относительную конфигурацию заместителей в
циклогексановом фрагменте.
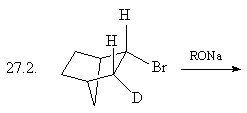
27. Какой структурный и (или) стереохимический
результат Вы ожидаете при проведении следующих
реакций? Назовите образующиеся соединения.
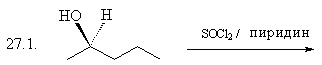
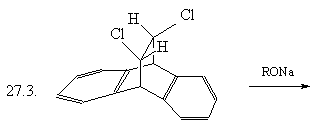
28. Бромирование непредельного спирта (1) с
помощью раствора брома в апротонном неполярном
растворителе привело монобромиду (2), а не к
ожидаемому дибромкарбинолу. Предложите
объяснение такого необычного течения реакции.
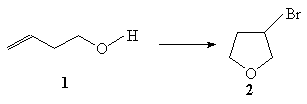
29. Известно, что вицинальные дигалогеналканы
при действии оснований отщепляют две молекулы
галогеноводорода и превращаются в алкил- или
диалкилацетилен. При этом первая стадия
дегидрогалогенирования завершается
образованием галогеналкена, в котором галоген
находится у одного из винильных атомов углерода:
RCH(Hal)-CH(Hal)R 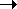 RCH=C(Hal)R
RCH=C(Hal)R
Поведение 1,2-дигалогенциклогексанов в реакциях
с основаниями резко отличается от упомянутого
выше поведения алифатических 1,2-дигалогенидов.
Так, 1,2-дибромциклогексан в реакции со спиртовым
раствором этоксида натрия дает с хорошим
препаративным выходом 3-этоксициклогексен:
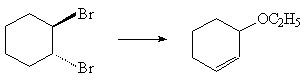
В чем, по Вашему мнению, причина такого резкого
отличия в реакциях алифатических и
алициклических 1,2-дигалогеналканов с
алкоксидами натрия?
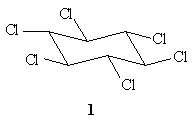
30. Соединения 1 претерпевает
однократное дегидрохлорирование при действии
основания в 104 раз медленнее, чем любой
другой 1,2,3,4,5,6-гексахлороциклогексан. Какой
фактор (какие факторы), по Вашему мнению, так
резко снижает активность гексахлорида 1?
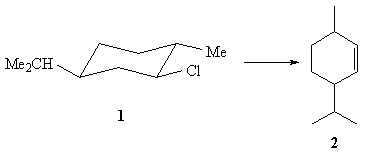
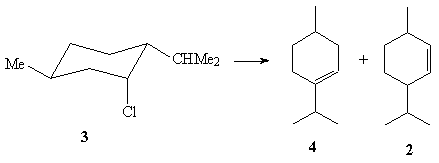
31.Дегидрохлорирование ментил хлорида (1) с
помощью этоксида натрия в этаноле завершается
образованием исключительно ментена-2 (2). В то
же время, неоментил хлорид (3) в аналогичных
условиях образует смесь ментена-3 (4) (75%) и
ментена-2 (2)(25%). В чем причина такого резкого
изменения селективности в условиях
дегидрохлорирования по Зайцеву?
Lieb.Ann.Chem. 1940. B.543. S. 191.
32. Предскажите стереохимический результат
дегидро-галогенирования трео- и эритро-1,2-дибромо-1,2-дифенилэтанов.
33.Приведите условия осуществляемых в
промышленном масштабе превращений этилена в:
33.1. этанол;
33.2. винилацетат;
33.3. этиленгликоль;
33.4. окись этилена.