|
Учебные материалы по физической химии
Задачи по физической химии.Часть 2.Химическая кинетика. Электрохимия
8. Фотохимические реакции
Многие химические реакции происходят только
под действием светового излучения. Для
возбуждения таких реакций обычно используют
видимое или УФ излучение (длина волны l = 200 ё 700 нм).
Энергия одного кванта света связана с длиной
волны соотношением:
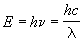 , ,
где n - частота излучения, h = 6.626.10-34
Дж. с - постоянная Планка, c = 3.108 м/с
- скорость света. Один моль квантов света иногда
называют эйнштейном.
При поглощении света происходит первичная
реакция (фотохимическая активация) и молекула
переходит в возбужденное электронное состояние:
A + h  A*. A*.
Возбужденная молекула может испытывать
последующие превращения (вторичные реакции):
1) флюоресценция, т.е. быстрое испускание
света и переход в исходное электронное
состояние:
A*  A + h A + h f. f.
Частота испускаемого света меньше или равна
частоте поглощаемого в первичном процессе света:
 f f   . .
2) Фосфоресценция - испускание света с
некоторой задержкой по времени, которая
необходима для того, чтобы молекула за счет
безызлучательных процессов перешла в другое
возбужденное состояние.
3) Дезактивация при соударении:
A* + A  A + A. A + A.
4) Диссоциация:
A*  B + C. B + C.
5) Реакция с другими молекулами:
A* + B  C. C.
Квантовый выход  фотохимической реакции равен
отношению числа прореагировавших молекул к
числу поглощенных фотонов. По закону
эквивалентности Эйнштейна-Штарка, каждый
поглощенный фотон вызывает фотохимическое
возбуждение одной молекулы. Это означает, что
теоретически первичный квантовый выход всегда
равен 1. фотохимической реакции равен
отношению числа прореагировавших молекул к
числу поглощенных фотонов. По закону
эквивалентности Эйнштейна-Штарка, каждый
поглощенный фотон вызывает фотохимическое
возбуждение одной молекулы. Это означает, что
теоретически первичный квантовый выход всегда
равен 1.
Экспериментальные значения квантового выхода
могут значительно отклоняться от 1 за счет
вторичных процессов (10-3 <  < 106). Высокие
значения квантового выхода ( < 106). Высокие
значения квантового выхода ( > 1) свидетельствуют о
протекании цепной реакции. Низкие значения > 1) свидетельствуют о
протекании цепной реакции. Низкие значения  ( ( < 1) характерны для
реакций, включающих процессы релаксации, т.е.
потери энергии возбуждения. < 1) характерны для
реакций, включающих процессы релаксации, т.е.
потери энергии возбуждения.
Кинетика фотохимических реакций описывается
обычными дифференциальными уравнениями,
выражающими закон действующих масс.
Единственное отличие от обычных реакций с
термическим возбуждением состоит в том, что
скорость фотохимических процессов не зависит от
концентрации исходного вещества, а в
соответствии с законом фотохимической
эквивалентности определяется только
интенсивностью поглощенного света.
ПРИМЕРЫ
Пример 8-1. Свет с длиной волны 436 нм проходил в
течение 900 с через раствор брома и коричной
кислоты в CCl4. Среднее количество
поглощенной энергии 1.919.10-3 Дж/с. В
результате фотохимической реакции количество
брома уменьшилось на 3,83.1019 молекул.
Чему равен квантовый выход? Предложите механизм
реакции, объясняющий квантовый выход.
Решение. В результате реакции поглотилось 1.919.10-3.
900 = 1.73 Дж световой энергии. Энергия одного
моля квантов составляет E = NAhc / l = 6.02.1023.
6.626.10-34. 3.108 / 436.10-9
= 2.74.105 Дж. Число молей поглощенных
квантов света равно n(hn ) = 1.73 / 2.74.105
= 6.29.10-6. Квантовый выход реакции равен
 = n(Br2)
/ n(hn ) = (3,83.1019/6.02.1023)
/ 6.29.10-6 = 10. = n(Br2)
/ n(hn ) = (3,83.1019/6.02.1023)
/ 6.29.10-6 = 10.
Такое значение квантового выхода характерно
для цепной реакции, механизм которой может быть
следующим:
Br2 + hn  Br + Br
(зарождение цепи), Br + Br
(зарождение цепи),
Br + C6H5CH=CHCOOH  C6H5CHBr-
CHCOOH C6H5CHBr-
CHCOOH
C6H5CHBr- CHCOOH + Br2  C6H5CHBr- CHBrCOOH + Br C6H5CHBr- CHBrCOOH + Br
Br + Br  Br2 (обрыв
цепи). Br2 (обрыв
цепи).
Пример 8-2. Фотолиз Cr(CO)6 в присутствии
вещества M может протекать по следующему
механизму:
Cr(CO)6 + hn  Cr(CO)5
+ CO, I Cr(CO)5
+ CO, I
Cr(CO)5 + CO  Cr(CO)6,
k2 Cr(CO)6,
k2
Cr(CO)5 + M  Cr(CO)5M,
k3 Cr(CO)5M,
k3
Cr(CO)5M  Cr(CO)5 +
M, k4 Cr(CO)5 +
M, k4
Предполагая, что интенсивность поглощенного
света мала: I << k4[Cr(CO)5M],
найдите фактор f в уравнении d[Cr(CO)5M]/dt
= -f[Cr(CO)5M]. Покажите, что график
зависимости 1/f от [M] - прямая линия.
Решение. Применим приближение
квазистационарных концентраций к
промежуточному продукту Cr(CO)5:
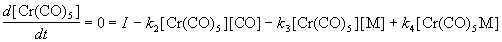
Из этого выражения можно найти
квазистационарную концентрацию [Cr(CO)5]:
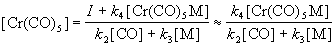
Скорость образования продукта реакции Cr(CO)5M
равна:
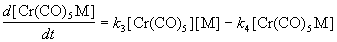
Подставляю квазистационарную концентрацию
[Cr(CO)5], находим:
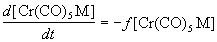 , ,
где фактор f определяется следующим
образом:
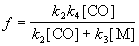 . .
Обратная величина 1/f линейно зависит от [M]:
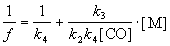 . .
ЗАДАЧИ
8-1. Энергия активации фотохимической реакции
равна 30 ккал/моль. Какова должна быть минимальная
длина волны света для того, чтобы инициировать
эту реакцию? Чему равна частота этого света?(ответ)
8-2. Энергия связи C- I в молекуле CH3I
составляет 50 ккал/моль. Чему равна кинетическая
энергия продуктов реакции
CH3I + hn  CH3.
+ I. CH3.
+ I.
при действии на CH3I УФ света с длиной волны
253.7 нм?(ответ)
8-3. Определите квантовый выход фотолиза
иодоводорода, который протекает по механизму:
HI + hn  H. + I.
, H. + I.
,
H. + HI  H2. +
I, H2. +
I,
I. + I.  I2.(ответ) I2.(ответ)
8-4. Рассчитайте квантовый выход
фотохимической реакции
(CH3)2CO  C2H6
+ CO, C2H6
+ CO,
протекающей под действием УФ света с длиной
волны 313 нм. Исходные данные: объем реакционного
сосуда 59 мл; среднее количество поглощенной
энергии 4.40.10-3 Дж/с; время облучения 7
ч; температура реакции 56.7 оС; начальное
давление 766.3 Торр; конечное давление 783.2 Торр.(ответ)
8-5. Молекулы в сетчатке глаза человека
способны передавать сигнал в зрительный нерв,
если скорость поступления излучения равна 2. 10-16
Вт. Найдите минимальное число фотонов, которое
должно за 1 с попадать на сетчатку глаза, чтобы
создать зрительное ощущение. Среднюю длину волны
света можно принять равной 550 нм.(ответ)
8-6. Вычислите максимально возможный выход
углеводов с 1 га зеленых насаждений в течение
лета. Исходные данные: солнечная энергия 1.0
кал/(см2. мин); летний день 8 ч; в область
поглощения хлорофилла (400 ё 650 нм, средняя длина
волны 550 нм) попадает 1/3 излучения; квантовый
выход 0.12 единиц H2CO на фотон.(ответ)
8-7. Аммиак разлагается УФ светом (длина волны
200 нм) с квантовым выходом 0.14. Сколько калорий
света необходимо для разложения 1 г аммиака?(ответ)
8-8. В фотохимической реакции A  2B + C квантовый выход равен 210. В
результате реакции из 0.300 моль вещества А
образовалось 2.28.10-3 моль вещества В.
Сколько фотонов поглотило вещество А? (ответ) 2B + C квантовый выход равен 210. В
результате реакции из 0.300 моль вещества А
образовалось 2.28.10-3 моль вещества В.
Сколько фотонов поглотило вещество А? (ответ)
8-9. Интенсивность флюоресценции может
изменяться в присутствии посторонних веществ.
Это явление называют тушением флуоресценции.
Простейший механизм тушения выглядит следующим
образом:
A + hn a  A*, I
(активация) A*, I
(активация)
A* + Q  A + Q, kq
(тушение) A + Q, kq
(тушение)
A*  A + hn f, kf
(флюоресценция). A + hn f, kf
(флюоресценция).
Используя приближение квазистационарных
концентраций, найдите зависимость интенсивности
флуоресценции в присутствии тушителя от
концентрации тушителя. Предложите способ
экспериментального определения констант
скорости kq и kf.
Указание: If = kf. [A*].(ответ)
8-10. Определите скорость фотохимической
реакции образования бромоводорода из простых
веществ, протекающей по следующему цепному
механизму:
Br2 + hn  2Br.
, I 2Br.
, I
Br. + H2  HBr + H.
, k1 HBr + H.
, k1
H. + Br2  HBr + Br.
, k2 HBr + Br.
, k2
H. + HBr  H2 +
Br. , k3 H2 +
Br. , k3
Br. + Br.  Br2,
k4(ответ) Br2,
k4(ответ)
*8-11. Фотохимическое хлорирование хлороформа
в газовой фазе следует закону скорости d[CCl4]/dt
= k[Cl2]1/2Ia1/2.
Предложите механизм, который приведет к этому
закону скорости при очень высоких давлениях
хлора.(ответ)
*8-12. Фотохимическое окисление фосгена,
сенсибилизированного хлором, описывается
суммарным уравнением:
2COCl2 + O2  2CO2
+ 2Cl2. 2CO2
+ 2Cl2.
Скорость этой реакции зависит от концентраций
следующим образом:
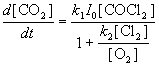 , ,
где I0 - интенсивность света. Квантовый
выход реакции - около 2. Известно, что в ходе
реакции образуются свободные радикалы ClO. и
COCl. . Предложите механизм реакции,
объясняющий эти экспериментальные данные
|

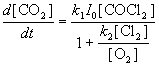 ,
,