|
Кафедра медицинской химии и тонкого органического синтеза
Лаборатория биоэлементоорганической химии

|
Зав.лабораторией
– Елена Рудольфовна Милаева
доктор
химических наук, профессор
телефон:
(495)-939-52-49
e-mail: milaeva@med.chem.msu.ru
|
ОСНОВНЫЕ НАПРАВЛЕНИЯ НАУЧНЫХ ИССЛЕДОВАНИЙ
1.
Создание новых гибридных
молекул на основе координационных и металлоорганических соединений – кандидатов
в лекарственные препараты
(Проф.
Е.Р. Милаева, с.н.с. Д.Б. Шпаковский, н.с. Т.А.Антоненко, м.н.с. Е.А. Никитин,
инженер Д.А. Берсенева. Комнаты 535, 331, 332).
Милаева
Елена Рудольфовна - e-mail: milaeva@med.chem.msu.ru
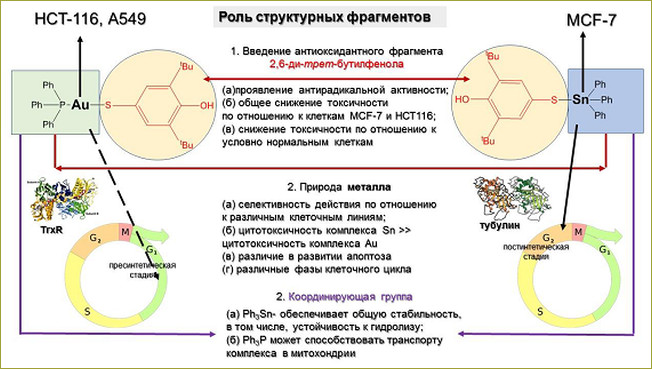
Предложена новая стратегия создания низкомолекулярных комбинированных таргетных молекул – кандидатов
лекарственных средств, базирующаяся на принципе использования
химических платформ ряда комплексов металлов, способных селективно связываться с
фармакологически значимыми мишенями.Данная методология заключается в том, что комбинирование различных
химических платформ (как органических, так и металлосодержащих) позволяет
обеспечить эффективное взаимодействие с различными мишенями, в том числе, позволит
создавать мультимодальные молекулы. Разработана
общая синтетическая стратегия конструирования новых физиологически активных
молекул на основе соединений металлов - кандидатов в противоопухолевые
средства.
Публикации
по теме:
1.
Milaeva E.R., Shpakovsky
D.B., Gracheva Yu A., Antonenko T.A., Ksenofontova T.D., Nikitin E.A.,
Berseneva D.A. Novel selective anticancer agents based on Sn and Au complexes.
Mini-review. Pure & Appl. Chem., 2020, 92, 8, 1201-1216.
2.
Antonenko T.A., Shpakovsky D.B., Berseneva D.А., Gracheva Yu A., Dubova L.G., Shevtsov P.N., Redkozubova O.M.,
Shevtsova E.F., Tafeenko V.A., Aslanov L.A., Milaeva E.R. Cytotoxic activity of
organotin carboxylates based on synthetic phenolic antioxidants and polycyclic
bile acids. J. Organomet. Chem., 2020, 909, 121089.
3.
Grin M.A., Tikhonov S.I., Petrova A.S.,
Pogorilyy V.A., Noev A.N., Tatarskiy V.V., Shpakovsky D.B., Milaeva E.R.,
Kalinina E.V., Chernov N.N., Shtil A.A., Mironov A.F., Kaprin A.D., Filonenko
E.V. New Derivatives of Bacteriopurpurin with Thiolated Au (I) Complexes: Dual
Dark- and Light Activated Antitumor Potency. Anti-cancer Agents in Medicinal
Chemistry, 2020, 20, 49-58.
4.
Antonenko T.A., Shpakovsky
D.B., Vorobyov M.A., Gracheva Yu.A., Kharitonashvili E.V., Dubova L.G., Shevtsova
E.F., Tafeenko V.A., Aslanov L.A., Iksanova A.G., Shtyrlin Yu.G., Milaeva E.R. Antioxidative
vs cytotoxic activities of organotin complexes bearing 2,6‐di‐tert‐butylphenol moieties, Appl. Organometal. Chem.,
2018, 32, e4381. (p.1-12).
5.
Milaeva E.R., Tyurin V. Yu, Shpakovsky D.B., Moiseeva A.A., Gracheva Yu.A., Antonenko T.A., Maduar V.V., Osolodkin D.I., Palyulin V.A., Shevtsova E.F. Redox-active metal complexes with 2,2΄-dipicolylamine containing ferrocenyl
moiety: synthesis, electrochemical behavior and biological activity. J. Organomet. Chem., 2017, 839, 60-70.
6.
Milaeva E.R., Shpakovsky D.B., Dyadchenko V.P., Gryzlov A.I., Gracheva Yu A., Antonenko T.A., Parulava M.J., Albov D.V., Aslanov L.A., Dubova L.G., Shevtsov P.N., Neganova M.E., Shevtsova E.F., Dubova L.G., Neganova M.E. Synthesis and biological activity of novel Au(I)
complexes with a protective antioxidant 2,6-di-tert-butylphenol group/ Polyhedron, 2017, 127, 512-519.
7.
Milaeva E.R., Tyurin V.Yu. Hybrid metal complexes with opposed
biological modes of action – promising selective drug candidates. Pure &
Applied Chemistry, 2017, 89,
8.
Korolev V.V., Lomova T.N., Maslennikova A.N., Korolev
D.V., Shpakovsky D.B., Jianwei Zhang, Milaeva E.R. Magnetocaloric properties of manganese(III)porphyrins
bearing 2,6-di-tert-butylphenolgroups. Journal of Magnetism and
Magnetic Materials, 2016, 401, 86-90.
9.
Ozturk, A. Metsios, S. Filimonova-Orlova, N. Kourkoumelis, S.
Hadjikakou, M. Manos, A. Tasiopoulos, S. Karkabounas, E. Milaeva, and N.
Hadjiliadis. Study on single crystal structure of the antimony(iii) bromide
complex with 3-methyl-2-mercaptobenzothiazole and biological activity of some
antimony(iii) bromide complexes with thioamides. Medicinal Chemistry
Research,
2012, 21, 3523–3531.
2.
Создание новых полифункциональных
антиоксидантов и протекторов
(Проф.
Е.Р. Милаева, доцент В.Ю. Тюрин, с.н.с. Д.Б. Шпаковский, н.с. Ю.А. Грачева.
Комнаты 530А, 331, 332).
Шпаковский
Дмитрий Борисович - e-mail: dmshpak@mail.ru
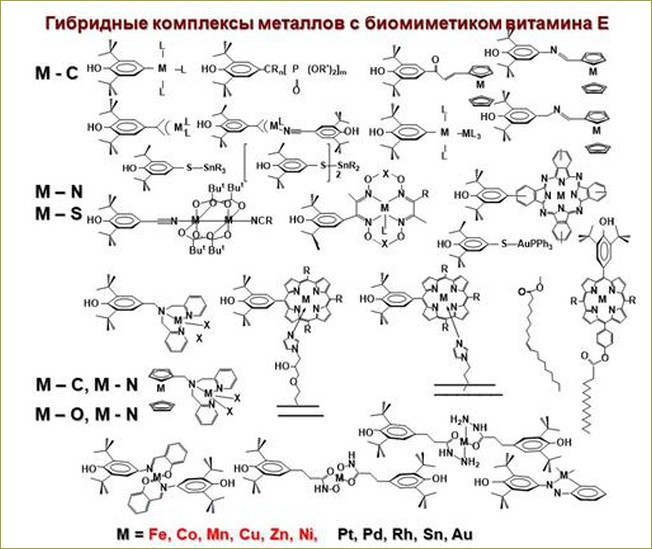
Проблема направленного синтеза соединений, обладающих
активностью в условиях нарушения окислительного и пролиферативного статуса
организма, связана с участием окислительного стресса в патогенезе ряда
патологий. Известно, что окислительная деградация биологических субстратов
происходит при нарушении баланса содержания кислорода и его активных
метаболитов (АМК) (O2-•, O22-•, O21, O2-, OH•, H2O2, HO2•), которые являются высоко реакционноспособными
радикальными частицами и индуцируют окислительный стресс организма
Новая предлагаемая стратегия позволяет получать
соединения, способные оказывать влияние на клеточный гомеостаз, что основано на
их участии в биохимических процессах, протекающих по редокс-маршруту. Направленный
синтез соединений – биомиметиков мексидола и токоферолов, с
широким спектром редокс-активности на основе 2,6-диалкилфенолов и их комплексов
биогенных металлов (либо металлов с доказанной фармакологической активностью),
а также комплексное изучение их физиологической активности является новым подходом
к созданию модуляторов гомеостаза.
В качестве таких агентов получены серии не просто
органических производных известных синтетических редокс-агентов, а их комплексов
с биометаллами с целью отбора соединений-лидеров, которые могут быть
использованы в качестве антиоксидантов, митопротекторов, апоптомодуляторов,
цитостатиков, ингибиторов радикальных процессов.
Публикации по теме:
1.
Nikitin E.A., Shpakovsky D.B., Pryakhin A.D., Antonenko
T.A., Tyurin Vl.Yu, Kazak A.A., Ulyanov A.N., Tafeenko V.A., Aslanov L.A., Dubova
L.G., Lysova E.A., Shevtsova E.F., Milaeva E.R. Antioxidant activity of modified
2,6-Di-tert- butylphenols with pyridine moiety. Pharmacy &
Pharmacology Int. J., 2020, 8, 122-134.
2.
Kolyada M.N., Osipova
V.P., Berberova N.T., Milaeva E.R., Ponomareva E.N., Belaya M.M. Cryoprotective
activity of phosphorus-containing phenol. Cryobiology, 2020, 96, 61-67.
3.
Milaeva E.R., Shpakovsky
D.B., Maklakova I.A., Rufanov K.A., Neganova M.E., Shevtsova E.F., Churakov A.V.,
Babkova V.A., Babkov D.A., Kosolapov V.A., Spasov A.A. Novel antioxidants based
on diphenylsulfimide containing a 2,6-di-tert-butylphenol moiety. RussianChemicalBulletin, 2018, 67, № 11, 2025-2034.
4.
E.B. Averina, D.A. Vasilenko, Y.A.
Gracheva, Y.K. Grishin, E.V. Radchenko, V.V. Burmistrov, G.M. Butov, M.E. Neganova,
T.P. Serkova, O.M. Redkozubova, E.F. Shevtsova, E.R. Milaeva, T.S. Kuznetsova, N.S.
Zefirov. Synthesis and
biological evaluation of novel 5-hydroxylaminoisoxazole derivatives as
lipoxygenase inhibitors and metabolism enhancing agents. Bioorg. Med. Chem. 2016, 24(4), 712-720;
5.
Osipova V.P., Kolyada
M.N., Berberova N.T., Milaeva E.R., Ponomareva E.N., Belaya M.M. Cryoprotective
effect of phosphorous-containing phenolic anti-oxidantfor the cryopreservation
of beluga sperm. Cryobiology, 2014, 69, с. 467-472.
6.
D. B. Shpakovsky, C. N. Banti, E. M. Mukhatova, Yu. A. Gracheva, V. P. Osipova, N. T. Berberova, D. V. Albov, T. A. Antonenko, L. A. Aslanov, E. R. Milaeva, S. K. Hadjikakou. Synthesis, antiradical activity and in
vitro cytotoxicity of novel organotin complexes based on
2,6-di-tert-butyl-4-mercaptophenol. Dalton Trans., 2014, 43, 6880–6890.
7.
А. И. Стрельников, И. К.
Томилова, Б. Г. Сафронов, В. В. Криштоп, Е. Л. Алексахина, Д. Б. Шпаковский, Е.
Р. Милаева. Сравнительная характеристика in vivo действия водорастворимой
и липофильной форм дипиколиламина, содержащего фрагмент 2,6-ди-трет-бутилфенола,
на окислительный статус тканей крыс. Известия РАН, Серия химическая.
2014, №5, с.1238.
8.
T.K. Rocheva, V.YuTyurin, D.V. Belykh, А.А.Moiseeva, JingweiZhang, Е.V. Buravlev, I.Yu. Chukicheva, E.R. Milaeva, А.V.Kutchin.. Biogenic metal porphyrins
with bulky 3,5-diisobornyl-4-hydroxyphenyl moieties. Synthesis, redox-properties
and antioxidative activity. American Journal
of Analytical Chemistry, 2014, №5, p. 1028-1036.
9.
Milaeva E. R., Shpakovsky D. B., Gracheva Y. A., Orlova S. I.,
Maduar V. V., Tarasevich B. N., Meleshonkova N. N., Dubova L. G., Shevtsova E.
F. Metal complexes with functionalised 2,2'-dipicolylamine ligand containing an
antioxidant 2,6-di-tert-butylphenol moiety: synthesis and biological studie. Dalton
Transactions, 2013, 42, 6817–6828.
10.
Milaeva E. Metal-based antioxidants - potential therapeutic candidates
for prevention the oxidative stress-related carcinogenesis. Current Topics in
Medicinal Chemistry, 2011, 11, 2703–2713.
3.
Создание кандидатов в
лекарственные препараты методом комбинирования
металлоцентров Pt(IV), Ru(III) и Ru(II) и мишень-ориентированных лигандов
(Доцент
А.А. Назаров, н.с. Ю.А. Грачева, м.н.с. И.А. Шутков, инженер М.Р. Гончар. Комнаты
530А, 424, 332).
Назаров
Алексей Анатольевич - e-mail: al@me.com
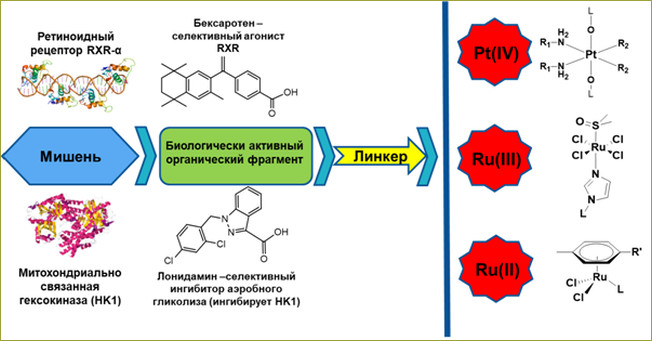
Предложен новый подход к конструированию
металлосодержащих противоопухолевых средств, заключающийся в комбинации в одной
молекуле атомов Pt(IV), Ru(III) и Ru(II) и мишень-ориентированных лигандов,
которые воздействуют на клеточные механизмы, специфичные для злокачественных
опухолей. Полученные соединения показывают высокую активность на широком
спектре раковых клеточных культур в экспериментах in vitro. Выявлены соединения
лидеры комплексов Pt(IV) и Ru(III) с фрагментами специфичного ингибитора
гликолиза и агониста ретиноидного рецептора.
Разработаны синтетические подходы к получению нового
класса противоопухолевых соединений рутения и платины, содержащих в своем
составе цитотоксичный компонент в форме пролекарства, который будет
активироваться в условиях раковой клетки. Общую идею можно описать следующим
образом: создается субстанция, которая будет лбладать цитотоксичностью за счет
активации более чем одного пролекарственного металлосодержащего центра,
входящего в ее состав. В результате соединение оказывается токсичным по
отношению к раковым клеткам, но менее токсичным для здоровых. Наличие двух
различных металлов в молекулах этих соединений позволяет контролировать
взаимодействие с биологическими мишенями, такими как геномная ДНК за счет
специфического взаимодействия с ее фрагментами.
Публикации по теме:
1.
Gonchar M.R., Matnurov E.M., Burdina T.A., Zava
O., Ridel Tina, Milaeva E.R., Dyson P.J., Nazarov A.A. Ruthenium(II)–arene and
triruthenium-carbonyl cluster complexes with new water-soluble phopsphites based
on glucose: Synthesis, characterization and antiproliferative activity. J. Organomet.
Chem., 2020, 919, 121312.
2.
Okulova Y.N., Zenin
I.V., Shutkov I.A., Kirsanov K.I., Kovaleva O.N., Lesovaya E.A., Fetisov T.I.,
Milaeva E.R., Nazarov A.A. Antiproliferative activity of Pt(IV) complexes with
lonidamine and bexarotene ligands attached via succinate-ethylenediamine linker.
Inorganica Chimica Acta, 2019, 495, 119010.
3.
Nazarov A.A.,
Mendoza-Ferri M.-G., Hanif M., Keppler B.K., Dyson P.J., Hartinger C.G. Understanding
the interactions of diruthenium anticancer agents with amino acids. Journal
of Biological Chemistry, 2018, 23, 1159–1164.
4.
Bolotin D.S., Demakova
M.Ya, Legin A.A., Suslonov V.V., Nazarov A.A., Jakupec M.A., Keppler B.K.,
Kukushkin V.Yu. Amidoxime Platinum(II) Complexes: pH-Dependent Highly Selective
Generation and Cytotoxic Activity. New Journal of Chemistry, 2017, 41, №
14, 6840-6848.
5.
Nosova Yu.N., Foteeva
L.S., Zenin I.V., Fetisov T.I., Kirsanov K.I., Yakubovskaya M.G., Antonenko T.A.,
Tafeenko V.A., Aslanov L.A., Lobas A.A., Gorshkov M.V., Markus Galanski,
Keppler B.K., Timerbaev A.R., Milaeva E.R., Nazarov A.A. Enhancing the
cytotoxic activity of anticancer Pt(IV) complexes by introduction of lonidamine
as an axial ligand, European Journal of Inorganic Chemistry, 2017, № 12,
1785-1791.
6.
Nosova Yulia N., Zenin
Ilia V., Maximova Varvara P., Zhidkova Ekaterina M., Kirsanov Kirill I.,
Lesovaya Ekaterina A., Lobas Anna A., Gorshkov Mikhail V., Kovaleva Оlga
N., Milaeva Elena R., Markus Galanski, Keppler Bernhard K., Nazarov Alexey A. Influence
of the number of axial bexarotene ligands on the cytotoxicity of Pt(IV) analogs
of oxaliplatin. Bioinorganic Chemistry & Applications, 2017, 2017,
1-6.
7.
Nosova Yulia N.,
Karlov Dmitry S., Pisarev Sergey A., Shutkov Ilya A., Palyulin Vladimir A.,
Mathurin Baquié, Milaeva Elena R., Dyson Paul J., Nazarov Alexey A. New
highly cytotoxic organic and organometallic bexarotene derivatives. Journal
of Organometallic Chemistry, 2017, 839, 91-97.
8.
Nazarov A.A., Nosova
Yu N., Mikhalev O.V., Kovaleva O.N., Dyson P.J., Milaevaa E.R. Antiproliferative
activity of ruthenium and osmium clusters with phosphine. Russian Chemical Bulletin, 2016, 65, № 2, 546-549.
9.
Nazarov A., Meier
Samuel M., Olivier Zava, Nosova Yu., Milaeva E.R., Hartinger C., Dyson P. Protein
Ruthenation and DNA Alkylation: Chlorambucil-functionalized RAPTA Complexes and
Their Anticancer Activity. Dalton Transactions, 2015, 44, 3614-3623.
10.
Zenita A., Davey G.E.,
Pablo Campomanes, Groessl M., Clavel C.M., Haojie Yu, Nazarov A.A., Charmian
Hui Fang Yeo, Wee Han Ang, Dröge P., Rothlisberger U., Dyson P.J., Davey C.A.
Ligand substitutions between ruthenium–cymene compounds can control protein
versus DNA targeting and anticancer activity. Nature communications, 2014,
5, № Article number: 3462.
4.
Изучение молекулярного
механизма новых кандидатов в лекарственные препараты
(д.м.н.
А.А.Штиль, проф. Е.Р. Милаева, доцент А.А. Назаров, н.с. Ю.А. Грачева, м.н.с.
И.А. Шутков, инженер М.Р. Гончар. Комнаты 530А, 408А).
Милаева
Елена Рудольфовна - e-mail: milaeva@med.chem.msu.ru

Курсы лекций, читаемые сотрудниками лаборатории:
Неорганическая медицинская химия (для студентов химического
факультета) - профессор Милаева Е.Р.
Современнная бионеорганическая химия (для студентов химического
факультета) – профессор Милаева Е.Р.
Бионеорганическая химия (для студентов факультета
фундаментальной физико-химической инженерии) – профессор Милаева Е.Р.
Бионеорганическая химия (для студентов факультета
фундаментальной медицины) – доцент Назаров А.А.
|





