|
Кафедра неорганической химии
Учебные материалы по неорганической химии
[предыдущий раздел] [содержание] [следующий
раздел]
§ 6. Физические свойства гидридов Н2Э.
Некоторые физические свойства водородных
соединений халькогенов представлены в табл.5.
Таблица 5.Физические свойства
гидридов ЭН2 элементов VI группы.
Гидрид
Свойство |
H2O |
H2S |
H2Se |
H2Te |
Длина связей Э-Н, 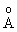 |
0.957 |
1.336 |
1.46 |
1.69 |
Энергия связи Э-Н,
кДж/моль |
463 |
347 |
276 |
238 |
Валентный угол Н-Э-Н, о |
104.5 |
92.1 |
91 |
90 |
Дипольный момент, D |
1.844 |
0.92 |
0.24 |
|
 fGo, кДж/моль fGo, кДж/моль
|
-237.24 (ж) |
-33.8 (г) |
19.7 (г) |
85,07 (г) |
Т.пл., оС |
0.0 |
-85.6 |
-65.7 |
-51 |
Т.кип., оС |
100.0 |
-60.3 |
-41.4 |
-2 |
К дисс.
К1 (до НЭ- )
К2 (до Э2- ) |
1.8. 10-16 * )
- |
1.05 . 10-7
1.23. 10-13 |
1.55. 10-4
1.00. 10-11 |
2.29. 10-3
6.76. 10-13 |
* ) Константа автопротолиза.
По мере увеличения размера атомов халькогенов
длина связи Н-Э увеличивается, а ее энергия, а,
следовательно, энергия Гиббса образования ( fGo) и
термодинамическая стабильность Н2Э,
уменьшаются. Понижение устойчивости молекул H2S
, H2Se, H2Te по сравнению с Н2О
объясняется ростом размеров np-орбиталей и
уменьшением их перекрывания с 1s-орбиталями
атомов водорода. fGo) и
термодинамическая стабильность Н2Э,
уменьшаются. Понижение устойчивости молекул H2S
, H2Se, H2Te по сравнению с Н2О
объясняется ростом размеров np-орбиталей и
уменьшением их перекрывания с 1s-орбиталями
атомов водорода.
Изменение угла Н- Э- Н в ряду Н2О- H2S- H2Se-
H2Te с точки зрения МВС можно объяснить тем,
что с ростом размеров атомов халькогенов
отталкивание между атомами водорода, а значит, и
величина угла Н- Э- Н уменьшаются.
В стандартных условиях гидриды Н2Э
являются газами. С ростом массы и размеров
молекул Н2Э усиливается межмолекулярное
взаимодействие и, как следствие, повышаются
температуры и энтальпии плавления и кипения
(табл.5). Аномально высокие температуры фазовых
переходов у воды объясняются усилением
межмолекулярного взаимодействия за счет
образования водородных связей.
[предыдущий раздел] [содержание] [следующий
раздел]
§ 7. Химические свойства Н2Э.
Газообразные гидриды Н2Э растворимы в
воде примерно одинаково: насыщенный раствор Н2S
при атмосферном давлении и 25оС имеет
концентрацию 0.1 моль/л. В водных растворах Н2Э
ведут себя как слабые двухосновные кислоты.
Сила кислот возрастает от серы к теллуру
благодаря понижению энергии связи Э- Н и
облегчению протолитического взаимодействия с
водой (табл.5):
Н2Э + Н2О  Н3О+ + HЭ- . Н3О+ + HЭ- .
Средние соли этих кислот, то есть сульфиды,
селениды и теллуриды, встречаются в природе как
минералы и руды металлов и служат источником их
получения. На различной растворимости сульфидов
в растворах с регулируемой кислотностью
основаны методы разделения и аналитического
определения металлов.
Рассмотрим в первом приближении процесс
осаждения труднорастворимых сульфидов
двухвалентных металлов из растворов их солей при
действии газообразного H2S.
В насыщенном водном растворе H2S
концентрация протонов определяется
растворимостью сероводорода и его константами
диссоциации:
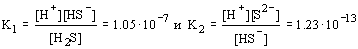
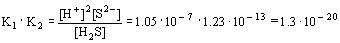
Отсюда следует, что [H+]2[S2- ] = 1.3.
10- 20. [H2S] = 1.3. 10- 21.
Поскольку К2 меньше К1 на 6 порядков,
то основной вклад в концентрацию [H+] в
растворе H2S вносит К1. Таким образом, [H+]=[HS-
]= 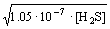  10-4. 10-4.
При подстановке этого значения в соотношение [H+]2[S2-
] = 1.3. 10- 21 получаем, что
концентрация ионов S2- в насыщенном
растворе H2S равна ~1.3. 10- 13.
Учитывая эту величину, оцените: 1) Будет ли
осаждаться CuS при действии H2S на раствор 0.01
М CuSO4 (ПР = 1.4. 10-36)? 2) Будет ли
осаждаться MnS при действии H2S на раствор 0.01
М MnSO4 (ПР =1.1. 10- 13)? (1. Ионное
произведение, [Cu2+][S2- ] = 10-2. 1.3.
10-13 =1.3. 10-15, превышает ПР, и
осадок выпадает. 2) Ионное произведение, [Mn2+][S2-]=
10-2. 1.3. 10-13 = =1.3. 10- 15,
не достигает ПР, и осадок не образуется.)
Халькогеноводороды сгорают на воздухе с
образованием диоксидов: Н2Э + 3/2 О2  ЭО2 + Н2О.
В кислых растворах Н2Э ведут себя как
мягкие восстановители. Восстановительные
свойства Н2Э усиливаются при переходе
от Н2О к Н2Ро, о чем
свидетельствуют значения стандартных
окислительно-восстановительных потенциалов
(табл.6). Кислород, галогены, кислоты-окислители,
перманганат-ион быстро и количественно
взаимодействуют с водными растворами
халькогеноводородов, выделяя халькоген в форме
простых веществ Э. Сероводород в зависимости от
условий проведения реакции может окисляться до
серы, SO2, тиосульфата, политионатов, H2SO4.
Для сероводорода характерна реакция с диоксидом
серы: SO2(г) + 2H2S(г) ЭО2 + Н2О.
В кислых растворах Н2Э ведут себя как
мягкие восстановители. Восстановительные
свойства Н2Э усиливаются при переходе
от Н2О к Н2Ро, о чем
свидетельствуют значения стандартных
окислительно-восстановительных потенциалов
(табл.6). Кислород, галогены, кислоты-окислители,
перманганат-ион быстро и количественно
взаимодействуют с водными растворами
халькогеноводородов, выделяя халькоген в форме
простых веществ Э. Сероводород в зависимости от
условий проведения реакции может окисляться до
серы, SO2, тиосульфата, политионатов, H2SO4.
Для сероводорода характерна реакция с диоксидом
серы: SO2(г) + 2H2S(г)  3S(тв.) + +2Н2О(г).
При проведении этой реакции в водных растворах (жидкость
Вакенродера) в продуктах найдены сера,
тиосульфат-ион, политионовые кислоты и другие
частицы. 3S(тв.) + +2Н2О(г).
При проведении этой реакции в водных растворах (жидкость
Вакенродера) в продуктах найдены сера,
тиосульфат-ион, политионовые кислоты и другие
частицы.
Таблица 6.Стандартные
окислительно-восстановительные потенциалы (В).
Реакция |
Ео |
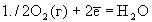 |
+1.229 |
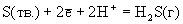 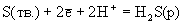
|
+0.174
+0.144 |
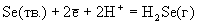 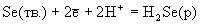
|
-0.082
-0.155 |
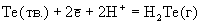 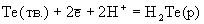
|
-0.441
-0.464 |
 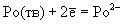 |
-1.400 |
Для серы свойственно образование полисульфанов
H2Sn. Соединения с n = 2-8 выделены в
индивидуальном состоянии, более высокие
гомологи - пока только в виде смесей. У селена и
теллура в результате окисления селенидов и
теллуридов в растворах осаждающиеся простые
вещества взаимодействуют с халькогенидами,
образуя полиселениды и полителлуриды (Na2Sе4,
Na2Te6). Однако отвечающие им водородные
соединения не выделены.
Полисульфаны синтезируют различными путями:
Na2S n (р) + 2HCl (p) = 2NaCl (p) +H2S
n (р) (n = 4-6)
S nCl2 (ж) +2H2S (ж) =2НCl (г)
+ H2S n+2(ж)
Молекулы полисульфанов образованы
неразветвленными цепочками из атомов серы. Они
неустойчивы, легко диспропорционируют на H2S
и свободную серу. Бесцветный дисульфан H2S2
является аналогом пероксида водорода H2O2,
он имеет аналогичное строение и проявляет
окислительные свойства. С помощью H2S2
окисляют сульфиды GeS и SnS до
тиопроизводных Gе(IV) и Sn(IV), а сульфиды As2S3
и Sb2S3 - до тиопроизводных As(V) и
Sb(V):
GeS + (NH4)2S2  (NH4)2GeS3 (NH4)2GeS3
As2S3 + 2(NH4)2S2 = 2 NH4 AsS3
+ (NH4)2S .
[предыдущий раздел] [содержание] [следующий
раздел]
§ 8. Получение гидридов Н2Э
Среди гидридов халькогенов единственным
термодинамически стабильным оказывается
сероводород Н2S (табл.5). Необходимо отметить
его сильную токсичность и опасность для
человека, сравнимую с синильной кислотой HCN .
Н2S и до некоторой степени Н2Se могут
быть получены непосредственно из простых
веществ, тогда как Н2Te и Н2Ро
синтезировать таким образом невозможно из-за их
термической нестойкости. Н2Те выше 0оС
распадается во влажном воздухе и на свету. Н2Ро
еще менее устойчив и может быть получен лишь в
следовых количествах.
Гидриды халькогенов легко синтезируют,
обрабатывая халькогениды металлов водой или
кислотами:
FeS +2HCl  H2S H2S + FeCl2 + FeCl2
Al2Se3 + 6H2O  H2Se H2Se + 2Al(OH)3
Ї + 2Al(OH)3
Ї
Al2Te3 + 6HCl  2 H2Te
2 H2Te + 2AlCl3
. + 2AlCl3
.
H2Te удобно также получать катодным
восстановлением теллура при 0оС. Анодом
служит платиновый электрод, а электролитом 50%-ная
серная кислота
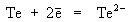 (катод) (катод)
[предыдущий раздел] [содержание] [следующий
раздел]
§ 9. Сульфиды металлов.
Процессы получения многих металлов сводятся к
переработке их сульфидов.
При обработке сульфидов на воздухе возможны 3
пути:
1.превращение в оксид;
2.образование водорастворимых сульфатов для
использования в процессах гидрометаллургии;
3.окисление до металлов (HgS + O2  Hg + SO2). Hg + SO2).
Эти возможности могут быть оценены с помощью
фазовой диаграммы трехкомпонентной системы M- S- O2,
построенной в логарифмических координатах
давлений SO2 и О2.
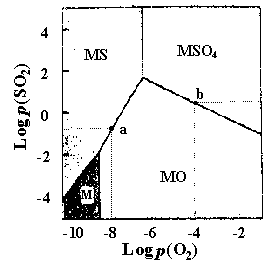
Рис.5. Изотермическая диаграмма 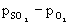 для
системы M(II)-S-O2. для
системы M(II)-S-O2.
Согласно правилу Гиббса с = k + 2 -  (с - число степеней
свободы, (с - число степеней
свободы,  - число фаз, k
- число компонентов), в системе металл- сера-
кислород при заданных температуре и давлении
газовой фазы в равновесии сосуществуют
максимально 3 фазы. На рис.5 изображена фазовая
диаграмма для системы М(II)- S- O2. - число фаз, k
- число компонентов), в системе металл- сера-
кислород при заданных температуре и давлении
газовой фазы в равновесии сосуществуют
максимально 3 фазы. На рис.5 изображена фазовая
диаграмма для системы М(II)- S- O2.
Границы между фазовыми полями - прямые линии.
Границы между фазами М/МО и MS/MSO4
вертикальные, границы между другими фазами
наклонные: у М/МS наклон равен 1.0, у МS/МО наклон
равен 1.5 и у МО/ MSO4 наклон составляет - 0.5. В
условиях постоянных температур на границе М/МО
происходит процесс МО = М + 1/2О2(г), константа
равновесия которого равна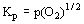 . Отсюда следует р(О2)
= =2logKр = константа и, таким образом, величина
р(О2) не зависит от р(SO2). На границе MS/MSO4
протекает процесс MSO4 = МS + 2О2(г),
константа равновесия которого равна . Отсюда следует р(О2)
= =2logKр = константа и, таким образом, величина
р(О2) не зависит от р(SO2). На границе MS/MSO4
протекает процесс MSO4 = МS + 2О2(г),
константа равновесия которого равна 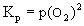 . Отсюда вытекает, что log
p(О2) = 1/2 log Kp = константа и величина р(О2)
также не зависит от р(SO2). На границе М/МS в
равновесии MSтв+О2(г) = Мтв + SO2(г)
участвуют 2 газа. Константа равновесия Кр =
р(SO2) / p(О2). Из этого следует, что log p(SO2)
= log Kр + log р(О2), и наклон граничной
линии М/МS равен 1.0. . Отсюда вытекает, что log
p(О2) = 1/2 log Kp = константа и величина р(О2)
также не зависит от р(SO2). На границе М/МS в
равновесии MSтв+О2(г) = Мтв + SO2(г)
участвуют 2 газа. Константа равновесия Кр =
р(SO2) / p(О2). Из этого следует, что log p(SO2)
= log Kр + log р(О2), и наклон граничной
линии М/МS равен 1.0.
На границе МS/МО в равновесии также участвуют 2
газа, но в других мольных соотношениях: MS + 3/2O2(г)
= МО + SO2(г) . 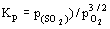 .
Следовательно, .
Следовательно, 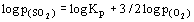 , и
наклон равен 1.5. На границе МО/ MSO4 2 газа
появляются в качестве продуктов распада: MSO4 =
MO + SO2(г) + +1/2O2(г). Константа равновесия , и
наклон равен 1.5. На границе МО/ MSO4 2 газа
появляются в качестве продуктов распада: MSO4 =
MO + SO2(г) + +1/2O2(г). Константа равновесия 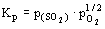 . Отсюда . Отсюда 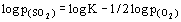 , то есть наклон равен - 0.5. , то есть наклон равен - 0.5.
Используя диаграмму р(SO2) - p(О2)
(рис.5), можно оценить состав продуктов окисления
сульфидов M(II) в различных условиях. Например, при
давлении p(О2) ~ 10-8 атм и р(SO2) ~ 2.
10-2 атм (точка а на рис.5) сульфид металла MS
окисляется до оксида МО, а при p(О2) ~ 10-4
атм и р(SO2) ~ 1.7 атм (точка b на рис.5) - до
сульфата MSO4.
[предыдущий раздел] [содержание] [следующий
раздел]
|