|
Кафедра неорганической химии
Учебные материалы по неорганической химии
[предыдущий раздел] [содержание] [следующий
раздел]
§ 10. Оксиды халькогенов.
Наиболее важными являются ди- (ЭО2) и
триоксиды (ЭО3) халькогенов. Для серы же
известен и ряд других нестабильных оксидов.
Оксид S2O получают пропусканием
тионилхлорида над сульфидом серебра
SOCl2 + Ag2S  S2O + 2AgCl.
S2O + 2AgCl.
Оксид S8O получают из H2S7 и SOCl2:
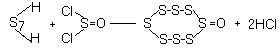 или
окислением S8 трифторуксусной кислотой. или
окислением S8 трифторуксусной кислотой.
[предыдущий раздел] [содержание] [следующий
раздел]
§ 10.1. Диоксиды халькогенов: получение,
строение и физические свойства.
Диоксид серы синтезируют непосредственным
сжиганием серы на воздухе или длительным отжигом
сульфидов: 4FeS2 + 11O2 = 2Fe2O3 +
8SО2 .
Диоксиды селена и теллура образуются при
обработке простых веществ диоксидом азота,
концентрированной HNO3:
Se + NO2  SeO2
+ NO SeO2
+ NO
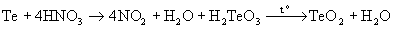
Однако в результате такой же обработки серы
образуются производные S(VI):
SO2 + NO2  SO3
+ NO и S + 6HNO3 SO3
+ NO и S + 6HNO3  H2SO4
+ 6NO2 + 2H2O. H2SO4
+ 6NO2 + 2H2O.
PoO2 можно получить слабым нагреванием
(250оС) металла на воздухе.
Физические свойства диоксидов халькогенов ЭО2
представлены в табл.7. С увеличением размера
атома Э халькогена возрастает длина связи Э-О и
усиливается межмолекулярное взаимодействие: при
стандартных условиях SО2 - газ, а SеО2 ,
TeО2 и РоО2 - твердые вещества.
Диоксид серы SО2 - бесцветный газ с резким
запахом, угнетающе действующий на растения.
Молекула SО2 изоэлектронна молекуле озона и
имеет угловую форму: валентный угол O- S- O равен 119о.
Кратность связи S- O составляет 1.5.
Таблица 7.Свойства диоксидов ЭО2
.
Свойства |
SО2 |
SеО2 |
TeО2 |
РоО2 |
r(Э-О), 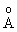 |
1.431 |
1.61 |
1.83 |
|
| Валентный угол О-Э-О, о |
119.3 |
125 |
110 |
|
| Дипольный момент, D |
1.67 |
2.70 |
|
|
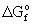 ,
кДж/моль ,
кДж/моль |
-300.4 |
-172(тв) |
-265(тв) |
-192 (тв) |
| Т.пл., оС |
-75.46 |
возг.315
340(давл.) |
733 |
552 |
| Т.кип., оС |
-10.01 |
337 |
1257 |
разл. |
Наличие неподеленной электронной пары
(электронной плотности) вблизи атома серы
объясняет полярность и высокую реакционную
способность молекулы SО2.
Увеличение размера атомов в ряду S- Se- Te- Po
отражается в строении твердых диоксидов.
Кристалл диоксида серы содержит дискретные
молекулы SО2. Твердый SеО2 построен из
бесконечных цепочек, в которых атомы Sе окружены
тремя атомами О в виде пирамиды { SeO3} с
концевым атомом кислорода. В двух полиморфных
модификациях  - и - и  -TeO2 содержатся
группы {ТeO4 } типа искаженных тригональных
бипирамид, соединенные ребрами или вершинами. TeО2
и особенно РоО2 со структурой типа CaF2
по существу ионные соединения. -TeO2 содержатся
группы {ТeO4 } типа искаженных тригональных
бипирамид, соединенные ребрами или вершинами. TeО2
и особенно РоО2 со структурой типа CaF2
по существу ионные соединения.
С ростом радиуса увеличиваются и
координационные числа атомов халькогенов в
диоксидах от 2 (SО2) до 3 (SеО2), 4 (TeО2)
и 8 (РоО2).
[предыдущий раздел] [содержание] [следующий
раздел]
§ 10.2. Химические свойства диоксидов ЭО2.
SО2 хорошо растворяется в воде (39.3 объема в
1 объеме Н2О при 20оС, то есть около 10%
по массе) с образованием гидратов SО2 .
nH2O. Раствор имеет кислую реакцию, но в
индивидуальном виде H2SO3 не выделена
из-за ее термодинамической неустойчивости.
Твердый диоксид селена также хорошо растворим
в воде, и при этом образуется селенистая кислота
SeO2 + H2O = H2SeO3. TeО2 и
РоО2 в воде не растворяются в силу высокой
энергии кристаллической решетки. В щелочной
среде TeО2 образует теллуриты металлов TeО2
+ 2OH  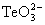 + H2O. TeО2 легко
растворяется в разбавленной HCl: TeO2+ 6HCl + H2O. TeО2 легко
растворяется в разбавленной HCl: TeO2+ 6HCl  H2TeCl6 +2H2O.
Аналогичные соединения известны и у других
элементов: H2PbCl6, H2TiCl6, H2PtCl6. H2TeCl6 +2H2O.
Аналогичные соединения известны и у других
элементов: H2PbCl6, H2TiCl6, H2PtCl6.
РоО2 с щелочами взаимодействует лишь при
сплавлении, а в реакциях с кислотами проявляет
основные свойства: РоО2 + 2H2SO4  Po(SO4)2 + 2 H2O
. Po(SO4)2 + 2 H2O
.
Восстановительные свойства SО2 обусловлены
присутствием в его молекуле неподеленной
электронной пары (см. § 10.1). SО2
взаимодействует с окислителями различной силы
(свободные галогены, хлорная, бромная и иодная
вода; растворы KMnO4, H2SeO3 и др.),
образуя различные производные S(VI):
I2 + SO2 + 2H2O = 2HI +H2SO4 ,
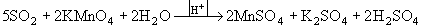
H2SeO3 + 2SO2 + H2O  Se Se + 2H2SO4 . + 2H2SO4 .
Реакция с F2 начинается около 200оС с
образованием SF6: SO2 + 5F2  SF6 + 2ОF2. При
повышении температуры (300-500оС) протекает
вторичный процесс: 2SO2+ 2OF2 SF6 + 2ОF2. При
повышении температуры (300-500оС) протекает
вторичный процесс: 2SO2+ 2OF2  SO2F2 + SOF2.
В зависимости от соотношений реагентов возможно
образование ряда оксофторидов серы: SOF2, SOF4
и SF5OF. SO2F2 + SOF2.
В зависимости от соотношений реагентов возможно
образование ряда оксофторидов серы: SOF2, SOF4
и SF5OF.
Диоксид серы фотохимически реагирует с Cl2:
SO2 + Cl2 + h  SO2Cl2.
Первичным процессом служит фотохимическая
диссоциация молекулы Cl2 на два радикала Cl.
. SO2Cl2.
Первичным процессом служит фотохимическая
диссоциация молекулы Cl2 на два радикала Cl.
.
Важнейший процесс для химической
промышленности и экологии - окисление SO2кислородом
до SO3: SO2+1/2O2 SO3, в технике осуществляется
при повышенной температуре с использованием
катализатора V2O5+ К2O. SO3, в технике осуществляется
при повышенной температуре с использованием
катализатора V2O5+ К2O.
При отсутствии воды выше 210оС диоксид
серы реагирует с NO2 с образованием
нитрозилдисерной кислоты (NO)2S2O7:
2NO2  2NO +
О2 , 2NO +
О2 ,
2SO2 + О2  2SO3,
2SO3,
2SO3 + NO2 + NO  (NO)2S2O7. (NO)2S2O7.
В присутствии следов воды на стенках колбы
обнаруживаются Н2SO4 и NOНSO4:
3NO2 + 2SO2 + H2O  2NOHSO4 + NO . 2NOHSO4 + NO .
Нитрозилсерная кислота разлагается : 2NOHSO4
+ Н2О  2H2SO4
+ NO + NO2. Ранее этот процесс использовался
для получения серной кислоты. 2H2SO4
+ NO + NO2. Ранее этот процесс использовался
для получения серной кислоты.
При взаимодействии с более слабыми
окислителями SО2 может окисляться до других
степеней окисления. Например, при пропускании SО2
через взвесь MnO2 в воде
2SO2 + MnO2 = MnS2O6 ,
образуется дитионат MnS2O6,
производное серы(V).
Окислительные свойства SО2 проявляются
при взаимодействии с сильными восстановителями,
например, H2S : 2 H2S(г) + SО2(г)
=3S + 2H2O(г).
С этим процессом связано образование свободной
серы при вулканических процессах. + 2H2O(г).
С этим процессом связано образование свободной
серы при вулканических процессах.
Взвесь пыли металлического цинка в воде
восстанавливает SO2 до производных серы (III) -
дитионитов и дитионистой кислоты: Zn + 2SO2 = ZnS2O4
или
2NaHSO3 + SO2 + Zn =  ZnSO3 + Na2S2O4 + H2O. ZnSO3 + Na2S2O4 + H2O.
Наличие неподеленной электронной пары в
молекуле SO2 обусловливает не только
восстановительные, но и комплексообразующие
свойства, в частности, образование гидратов.
Молекула SO2 служит нейтральным лигандом в
многочисленных комплексах с переходными
металлами, например:
[Fe2(CO)8( - SO2)], [{ Fe(C5H5)(CO)2}
2 SO2] и [RuCl(NH3)4(SO2)]Cl. - SO2)], [{ Fe(C5H5)(CO)2}
2 SO2] и [RuCl(NH3)4(SO2)]Cl.
Их образование протекает по
донорно-акцепторному механизму, при этом
молекула SO2 может присоединяться
(координироваться) к атому металла через атом
серы или атом кислорода и действовать как
концевой (однодентатный) или мостиковый
(бидентатный) лиганды.
Диоксид SеO2 менее термодинамически
стабилен, чем SO2 и ТеO2. Он легко
восстанавливается аммиаком, гидразином, водным
раствором SO2 до красного Sе.
Сравнить восстановительные свойства SeO2 и
TeO2, более слабые по сравнению с SO2,
можно с помощью диаграммы Фроста (см. § 11).
РоО2 легко растворяется в
галогеноводородных кислотах НХ, образуя соли РоХ4
, и не участвует в
окислительно-восстановительных реакциях с НХ.
[предыдущий раздел] [содержание] [следующий
раздел]
§ 10.3. Получение и свойства триоксидов
ЭО3 .
Среди триоксидов ЭО3 наиболее важен триоксид
серы SО3 , который производится
каталитическим окислением SO2 при 500оС
для получения H2SO4. Он выделяется
также при термическом распаде сульфатов
металлов: 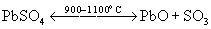 или
дисульфатов: или
дисульфатов: 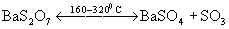 . При этом
SО3 частично диссоциирует на SО2 и О2.
В лаборатории чистый SО3 получают
пропусканием его над P2O5.
Образующийся продукт присоединения (аддукт) P2O5.
SО3 при нагревании выделяет чистый SО3. . При этом
SО3 частично диссоциирует на SО2 и О2.
В лаборатории чистый SО3 получают
пропусканием его над P2O5.
Образующийся продукт присоединения (аддукт) P2O5.
SО3 при нагревании выделяет чистый SО3.
Кристаллический триоксид SО3 плавится при
16оС. Мономерная газообразная молекула SО3
имеет форму симметричного плоского треугольника
с длиной связи S- O 1.43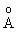 и не обладает дипольным моментом. Различные
полиморфные модификации твердого оксида SО3 построены
из тетраэдров SО4 (рис.6).
и не обладает дипольным моментом. Различные
полиморфные модификации твердого оксида SО3 построены
из тетраэдров SО4 (рис.6).
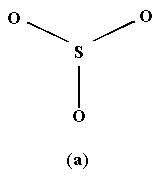
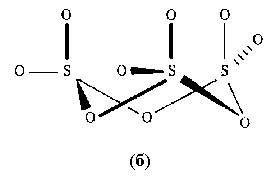
Рис.6. Строение газообразной молекулы SO3 (a)
и конденсированного тримера S3O9 (б).
Они связаны общими вершинами в циклические
тримеры S3О9, напоминающие
циклические метаполифосфаты и силикаты, или
бесконечные спиральные цепи.
Триоксид SО3 - одно из самых
реакционноспособных соединений. Проявляет
окислительные свойства. Серой и углеродом SО3
восстанавливается до SO2: 2SO3 + C  2SO2 + CO2.
Выше 500оС SО3 восстанавливается
моноксидом СО: SО3 + СО 2SO2 + CO2.
Выше 500оС SО3 восстанавливается
моноксидом СО: SО3 + СО  SO2 + СО2 . Сульфидами металлов SО3
восстанавливается до SО2 или свободной
серы. SO2 + СО2 . Сульфидами металлов SО3
восстанавливается до SО2 или свободной
серы.
Особенности взаимодействия SО3 с
галогеноводородами связаны с ростом
восстановительных свойств в ряду HCl- HBr- HI.
Окислительные свойства SО3 усиливаются с
температурой. При нагревании SО3 реагирует
с газообразным HCl, образуя хлорсерную
кислоту HSO3Cl. При дальнейшем повышении
температуры HCl восстанавливает SО3 до SO2
с одновременным выделением Cl2. При
взаимодействии с HBr триоксид серы уже при 0оС
восстанавливается до SO2: 2SO3+2HBr SO2+Br2+Н2SO4.
В жидком HI при -51оС немедленно выделяет I2,
а SO3 восстанавливается до Н2 S. SO2+Br2+Н2SO4.
В жидком HI при -51оС немедленно выделяет I2,
а SO3 восстанавливается до Н2 S.
Взаимодействие SО3 с газообразным Н2S
протекает с образованием SO2, Н2О, S. Но
при ~ - 78оС получается твердый аддукт SO3.
Н2S - изомер тиосерной кислоты. При
проведении этой реакции в сухом эфире образуется
свободная тиосерная кислота: 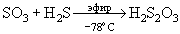 . SО3 действует как сильнейшая
кислота Льюиса, образуя с оксидами металлов
соответствующие сульфаты, например, Fe2O3
+ 3SO3 . SО3 действует как сильнейшая
кислота Льюиса, образуя с оксидами металлов
соответствующие сульфаты, например, Fe2O3
+ 3SO3 Fe2(SO4)3
. Fe2(SO4)3
.
При 1700С SО3 с газообразным F2
образует пероксодисульфурилдифторид: 2SO3+
F2 S2O6F2. S2O6F2.
SеО3 получают дегидратацией селеновой
кислоты при 150оС с помощью фосфорного
ангидрида с последующей отгонкой SеО3 в
вакууме. TeО3 синтезируют дегидратацией
ортотеллуровой кислоты H6TeO6 при 350оС.
SеО3 и TeО3 при нагревании легко
отщепляют кислород и образуют диоксиды. SеО3 хорошо
растворяется в воде с образованием Н2SеО4.
Твердый SeO3 состоит из тетраэдров 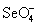 , объединенных в
циклические тетрамеры , объединенных в
циклические тетрамеры 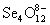 .
Твердый триоксид теллура построен из октаэдров
ТеО6, объединенных общими вершинами в цепи.
В противоположность SО3 и SеО3, ТеО3
водой гидратируется слабо. .
Твердый триоксид теллура построен из октаэдров
ТеО6, объединенных общими вершинами в цепи.
В противоположность SО3 и SеО3, ТеО3
водой гидратируется слабо.
SеО3 обладает сильными окислительными
свойствами, окисляя охлажденную соляную кислоту:
SеО3 + 2HCl 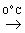 H2SeO3
+ H2SeO3
+  Cl2, фосфор
до Р2О5. SеО3 с органическими
веществами взрывается. Cl2, фосфор
до Р2О5. SеО3 с органическими
веществами взрывается.
Окислительные свойства триоксида теллура
выражены гораздо слабее, он вытесняет хлор из
соляной кислоты только при нагревании.
[предыдущий раздел] [содержание] [следующий
раздел]
|

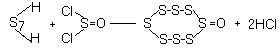 или
окислением S8 трифторуксусной кислотой.
или
окислением S8 трифторуксусной кислотой.