|
Учебные материалы по физической химии
Задачи по физической химии.Часть 1.Химическая термодинамика
Биологический факультет.
Досрочный экзамен по физической химии (3-й семестр).Задачи
1. Один моль водяных паров обратимо и
изотермически сконденсировали в жидкость при 100 оС.
Рассчитайте работу, теплоту, изменение
внутренней энергии и энтальпии в этом процессе.
Удельная теплота испарения воды при 100 оС
равна 2260 Дж/г.
2. Для некоторого вещества зависимость
теплоемкости от температуры имеет вид: CV
= aT 3 при температуре 0 – 10 К. Найдите
зависимость энергии Гельмгольца, энтропии и
внутренней энергии от температуры в этом
диапазоне.
3. Рассчитайте изменение энтропии 1000 г воды в
результате ее замерзания при –5 ОС. Теплота
плавления льда при 0 оС равна 6008 Дж/моль.
Теплоемкости льда и воды равны 34.7 и 75.3 Дж/(моль.
К), соответственно. Объясните, почему энтропия
при замерзании уменьшается, хотя процесс -
самопроизвольный.
4. Давление пара над твердым UF6 равно 2956 Па
при 2oC и 10280 Па при 19oC, а давление пара
над жидким UF6 равно 47817 Па при 30oC и 74030
Па при 42oC. Определите координаты тройной
точки и  плH (UF6). плH (UF6).
5. При 1273 К и общем давлении 30 атм в равновесной
смеси
CO2(газ) + C(тв) = 2CO(газ)
содержится 17% CO2. Сколько процентов CO2
будет содержаться в газе при общем давлении 20
атм? При каком давлении в газе будет содержаться
25% CO2?
6. Раствор, содержащий 0.81 г углеводорода H(CH2)nH
и 190 г бромистого этила, замерзает при 9.47 oC.
Температура замерзания бромистого этила 10.00 oC,
криоскопическая константа 12.5 град. моль–1.
Сколько атомов углерода содержит молекула
углеводорода?
7. При нагревании любой термодинамической
системы заселенность одних уровней
увеличивается, а других уменьшается. Используя
закон распределения Больцмана, определите,
какова должна быть энергия уровня для того, чтобы
его заселенность увеличивалась с ростом
температуры.
Биологический факультет
Досрочный экзамен по физической химии (3-й
семестр)
1. Четыре моля кислорода, находящиеся в объеме 20
л при температуре 270 К, адиабатически расширили
против внешнего давления 600 торр до утроения
объема. Рассчитайте конечную температуру,
совершенную работу, изменение внутренней
энергии и энтальпии.
2. Зависимость теплового эффекта реакции CH3OH(г)
+ 3/2O2 = CO2 + 2H2O(г) от
температуры выражается уравнением:
 rHT (Дж)
= rHT (Дж)
=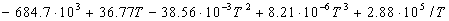
Рассчитайте изменение теплоемкости  Cp и Cp и  CV
для этой реакции при 500 К. CV
для этой реакции при 500 К.
3. Вычислите изменение энергии Гиббса при
сжатии от 1 атм до 3 атм при 298 К: а) одного моля
жидкой воды; б) одного моля водяного пара
(идеальный газ).
4. Давление пара над твердым Cl2 равно 352 Па
при –112oC и 35 Па при –126.5oC, а давление
пара над жидким Cl2 равно 1590 Па при –100oC
и 7830 Па при –80oC. Определите координаты
тройной точки и  плH(Cl2). плH(Cl2).
5. Для реакции
2HI(г) = H2 (г) + I2(г)
при 698.6 K константа равновесия равна KP
= 1.83 10–2. Сколько граммов HI
образуется, если 10 г I2 и 0.2 г H2 нагреть
до этой температуры в 3-литровом сосуде? 10–2. Сколько граммов HI
образуется, если 10 г I2 и 0.2 г H2 нагреть
до этой температуры в 3-литровом сосуде?
6. Рассчитать состав (в мольных долях) раствора
бензол–толуол, который при нормальном давлении
кипит при температуре 100o C, а также состав
образующегося пара. Раствор считать идеальным.
Давления пара чистых бензола и толуола при 100o
C равны 1350 Торр и 556 Торр, соответственно.
7. Для некоторой термодинамической системы (не
идеального газа) известна сумма по состояниям, Z(T,V).
Найдите работу, которую выполняет эта система
при обратимом изотермическом расширении от V1
до V2.
|
