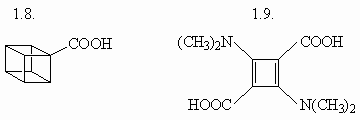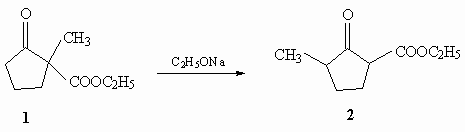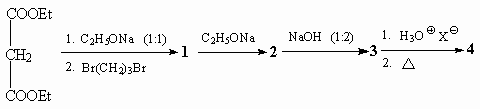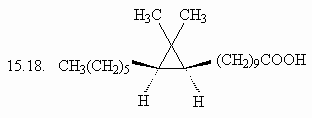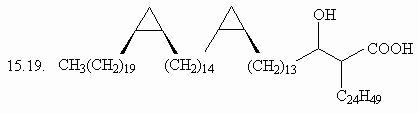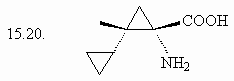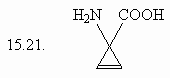|
Учебные материалы/ Органическая химия / Карбоновые кислоты и их производные
И.Г.Болесов, Г.С.Зайцева
карбоновые кислоты и их производные
(синтез, реакционная способность, применение в органическом синтезе)
КОНТРОЛЬНАЯ РАБОТА N 2 (вопросы с 1-17)
1. Назовите следующие соединения по
номенклатуре IUPAC:
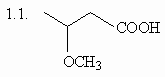
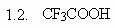
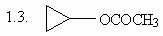


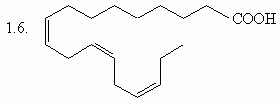
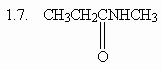
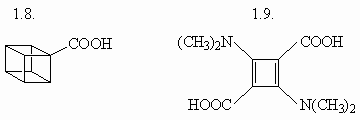
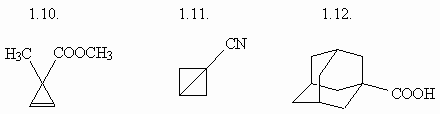
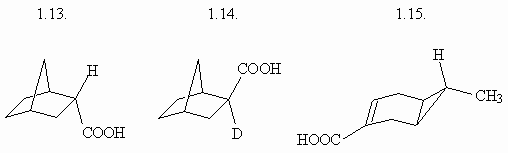 (ответ) (ответ)
2. В каждой из указанных ниже пар анионов
укажите наиболее сильное основание. Укажите
также наиболее сильную кислоту в парах
соответствующих сопряженных кислот:
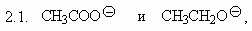
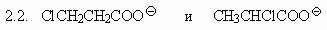
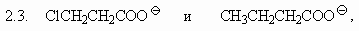

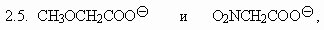
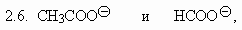
 (ответ) (ответ)
3. Укажите, какая из карбоксильных
групп в молекуле 3-хлоргександиовой кислоты
имеет меньшую константу диссоциации.
4. При кипячении в растворе D2O,
содержащем сильную протонную кислоту,
пропановая кислота постепенно обменивает три
атома водорода на дейтерий. Предложите возможный
механизм дейтерообмена.
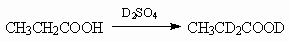 (ответ) (ответ)
5. Тщательный анализ состава реакционной
смеси, образующейся при взаимодействии
1-бромобутана с магнием в эфире и далее с СО2
показал, что наряду с ожидаемой пентановой
кислотой образуются также н-бутан, 1-бутен и н-октан.
Выскажите Ваши соображения о возможных путях
образования этих углеводородов.
6. Предскажите результат реакций
этилмагнийбромида:
6.1. с двуокисью углерода,
6.2. с нитрилом изомасляной кислоты,
6.3. с этилацетатом.
7. Предскажите кратчайший путь (одно-
или двухстадийный) получения следующих веществ,
используя для этого любые производные С1 - С3
и необходимые металлоорганические соедлинения:
СН3СН2СН(ОН)СН2СООСН3,
(СH3)2C=CHCOOCH2CH3 (ответ)
8. Сложный эфир С5H10O2
в реакции с изопропилмагнийбромидом образует
третичный спирт, дегидратация которого приводит
лишь к одному алкену С10H20. Предложите
структуру сложного эфира и синтезированного из
него алкена С10Н20. Дополнительные
данные: алкен С10Н20 при
озонировании и восстановительном разложении
озонида образует ацетон и симметричный кетон, не
образующий бензилиденового производного при
смешении с бензальдегидом и не дающий
хлороформной реакции.(ответ)
9. Предложите методы и реагенты, с
помощью которых 3-метилбутановую кислоту можно
превратить в следующие соединения:
(СН3)2С=СНСООСН3,
(СН3)2СНСН2СН2СООН,
(СН3)2СНСН2Br,
9.4. (СН3)2СНСН2СОNH2.(ответ)
10. Предложите последовательность реакций,
с помощью которых из малонового эфира можно
получить следующие соединения:
10.1. (СН3)2СНСН2СН2СООН,
10.2. СН2=СНСН2СН2СООН,
10.3. НООССН2СН2СООН,
10.4. НООССН2СН(СН3)СООН
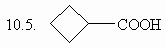 (ответ) (ответ)
11. Предложите последовательность реакций, с
помощью которых из ацетоуксусного эфира можно
получить указанные ниже соединения:
11.1. СН2=СНСН2СН2СОСН3,
11.2. СН3СОСН2СН2СОСН3,
11.3. СН3СОСН2СН2СООН,
11.4. СН3СОСН2СН2СН2СООН. (ответ)
12. Продолжительное нагревание кетоэфира 1
в присутствии этоксида натрия приводит к
образованию изомерного ему соединения 2.
Предложите схему интересной скелетной
перегруппировки.
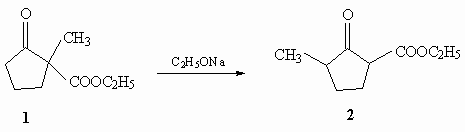 (ответ) (ответ)
13. Особенность спектра ЯМР 1Н
N,N-диметилформамида (ДМФА), зарегистрированного
при комнатной температуре, состоит в том, что в
нем присутствуют два сигнала протонов метильных
групп. Предложите объяснение неэквивалентности
протонов метильных групп ДМФА в наблюдаемых
условиях. (ответ)
14. Расшифруйте последовательность
превращений:
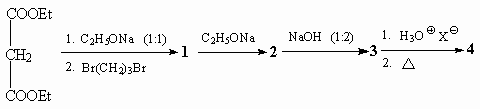 (ответ) (ответ)
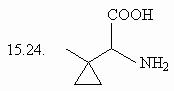
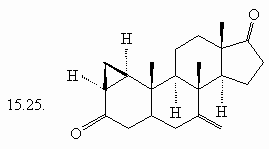
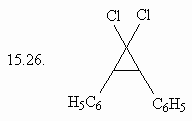
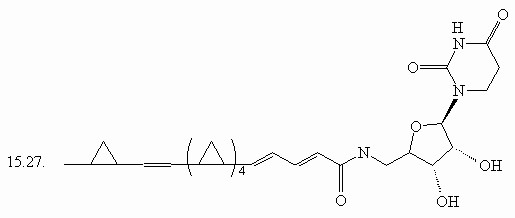
15. Сколько изомеров
3,4-дигидроксигексановой кислоты (15.1.) Вы можете
нарисовать, если будете варьировать только
пространственное расположение заместителей?
Какие типы изомерных отношений Вы встретите
среди предложенных Вами соединений?
Оцените число изомеров и для серии приведенных
ниже соединений, учитывая, что новые изомеры Вы
будете получать, лишь варьируя пространственное
расположение заместителей в каждом случае.
15.2. HOCH2-CH(OH)-COOH;
15.3. CH3-CH(NH2)-COOH;
15.4. C6H5-CH2-CH(NH2)-COOH;
15.5. СH3-CH(OH)-CH(NH2)-COOH;
15.6. H2N-CH2-CH2-CH2-CH2-CH(NH2)COOH;
15.7. CH3-CH2-CH(CH3)-CH(NH2)-COOH;
15.8. HOOC-CH(NH2)-CH2-CH2-COOH;
15.9. CH3-CH(CH3)-CH(NH2)-COOH;
15.10. H2N-CO-CH2-CH2-CH(NH2)-COOH;
15.11. HS-CH2-CH(NH2)-COOH;
15.12. HOOC-CH(OH)-CH(OH)-COOH;
15.13. HO-CH2-CH(OH)-CH(OH)-COOH;
15.14. HC(=O)-CH(OH)-CH(OH)-COOH;
15.15. HO-CH2-CH(OH)-CH(OH)-CH(OH)-COOH.
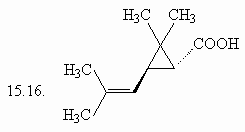
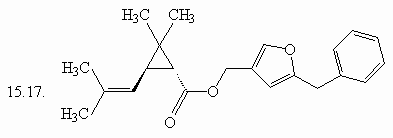
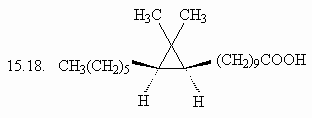
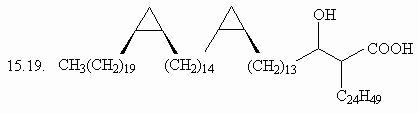
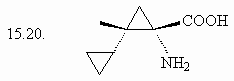
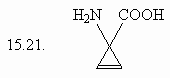
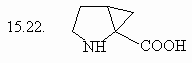
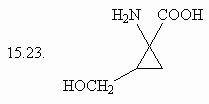
 (ответ) (ответ)
16. Этиловый эфир муравьиной кислоты
кипит при 54.5 oC. В то же время, каждый из
компонентов, из которых образован указанный
эфир, имеет более высокую температуру кипения:
муравьиная кислота кипит при 100.5 oC, а
этиловый спирт - при 78 oC. Найденное
соотношение температур кипения карбоновой
кислоты, спирта и образованного из них сложного
эфира сохраняется и для многих других сочетаний
кислота - спирт - сложный эфир (например, для
метиловых и этиловых эфиров карбоновых кислот и
соответствующих спиртов и карбоновых кислот). В
чем, по Вашему мнению, причина (или причины)
упомянутого снижения температур кипения сложных
эфиров по сравнению с исходными карбоновыми
кислотами?
17. Какие факторы контролируют
кислотность карбоновых кислот? В каких пределах
может меняться их рКа ? Приведите примеры,
иллюстрирующие Ваши соображения.
|