|
Учебные материалы по неорганической химии
Неорганические синтезы. Практикум для студентов 1-го курса (сборник методик)
СИНТЕЗ ТЕТРАИОДИДА ОЛОВА
Ознакомиться по любому доступному Вам
справочнику с физическими и физико-химическими
свойствами используемых и синтезируемых Вами
веществ. Напишите уравнения реакций.
 В
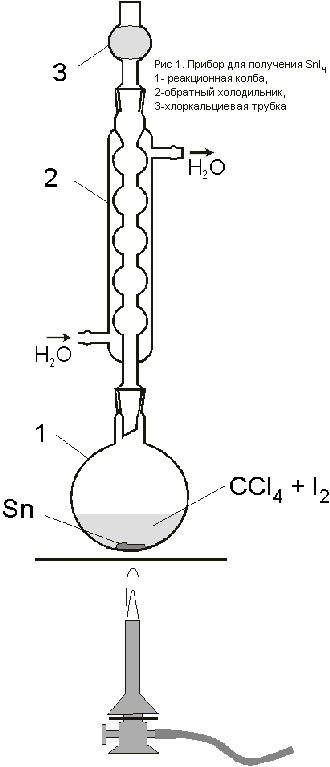
колбу прибора (рис.1), состоящего из одногорлой
колбы 1, шарикового холодильника 2 с
хлоркальциевой трубкой 3, поместить 1 г
измельченного олова и свежевозогнанный иод
(недостаток 10% от стехиометрического количества).
Туда же прилить 50 мл сухого тетрахлорида
углерода. Следует помнить, что тетрахлорид
углерода ядовит и впитывается через кожу. В
колбу прибора (рис.1), состоящего из одногорлой
колбы 1, шарикового холодильника 2 с
хлоркальциевой трубкой 3, поместить 1 г
измельченного олова и свежевозогнанный иод
(недостаток 10% от стехиометрического количества).
Туда же прилить 50 мл сухого тетрахлорида
углерода. Следует помнить, что тетрахлорид
углерода ядовит и впитывается через кожу.
Нагреть смесь в реакционной колбе 1 газовой
горелкой через асбестовую сетку до кипения.
Нагревание смеси проводить в течение 1,5-2 часов,
следя за тем, чтобы кипение растворителя не было
очень бурным. Конец реакции характеризуется
исчезновением малиновой и появлением
соломенно-желтой окраски раствора. Оставить
раствор с осадком на ночь.
На следующий день нагреть раствор до кипения и
декантировать в стакан (под тягой! Пары CCl4
ядовиты, ПДК в рабочей зоне 20 мг/м3).
Стакан с раствором охладить в бане со льдом. При
охлаждении выпадают кристаллы SnI4. Если
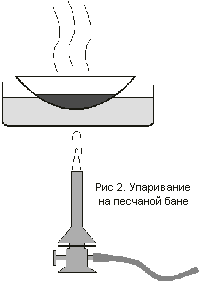
кристаллов выпало мало, раствор перенести в
фарфоровую чашку и упарить на песчаной бане до
половины объема (рис.2.). Раствор охладить в бане
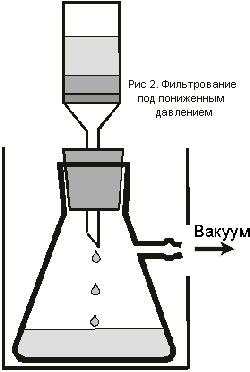
со льдом. Выпавшие кристаллы отфильтровать при
пониженном давлении (рис.3.) на стеклянном фильтре
N 2 (очки!). Промыть осадок на фильтре 5 мл
сухого, охлажденного во льду CСl4.
Вещество высушить на воздухе и перенести в
бюкс, определить его массу и рассчитать выход.
(Непрореагировавшим оловом пренебречь.)
К небольшой части препарата в пробирке
добавить несколько капель воды и нагреть. Что
происходит? Как меняется цвет осадка? Определите
pH раствора. К части раствора над осадком добавить
1-2 капли раствора азотнокислого серебра.
Отметить цвет выпавшего осадка. Объяснить
наблюдаемые явления, написать уравнения реакций.
Реактивы: 1. Иод,. 2. Олово - 1 г. 3.
Четырехлористый углерод - 50 мл.
Оборудование: 1. Колба одногорлая. 2.
Холодильник. 3. Стакан. 4. Воронка со стеклянным
фильтрующим дном N 2.
Рекомендованная литература: 1. Практикум по
неорганической химии /ред В.П.Зломанов, М.: МГУ, 1994.
2. Руководство по неорганическому синтезу /Ред
Г.Брауэр, М.: Мир, 1985, Т.3.
|

 В
колбу прибора (рис.1), состоящего из одногорлой
колбы 1, шарикового холодильника 2 с
хлоркальциевой трубкой 3, поместить 1 г
измельченного олова и свежевозогнанный иод
(недостаток 10% от стехиометрического количества).
Туда же прилить 50 мл сухого тетрахлорида
углерода. Следует помнить, что тетрахлорид
углерода ядовит и впитывается через кожу.
В
колбу прибора (рис.1), состоящего из одногорлой
колбы 1, шарикового холодильника 2 с
хлоркальциевой трубкой 3, поместить 1 г
измельченного олова и свежевозогнанный иод
(недостаток 10% от стехиометрического количества).
Туда же прилить 50 мл сухого тетрахлорида
углерода. Следует помнить, что тетрахлорид
углерода ядовит и впитывается через кожу. 
