Определение скорости химической реакции. Дополнительный материал.
Нюанс 1:
Это выражение
v = Dc/Dt
позволяет определить лишь среднюю скорость реакции за выбранный отрезок времени.
Ученых же, как правило, интересует скорость в выбранный момент времени, т.е. так называемая
мгновенная скорость реакции. Она определяется как производная функции c(t):
v = dc/dt
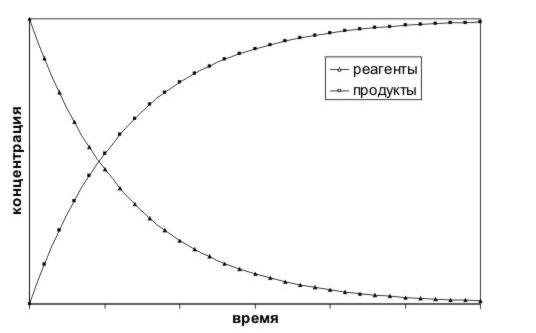
Если мы определяем скорость реакции по одному из реагентов, то знак производной c(t) отрицателен,
т.к. концентрации реагентов убывают. Но по физическому смыслу скорость не может быть
отрицательной величиной. Поэтому при использовании концентраций реагентов:
v = -dc/dt
Нюанс 2:
Определим скорость этой же реакции
H2 + I2 = 2HI
не по уменьшению концентрации реагента, а по увеличению концентрации продукта:
v(HI) = dc(HI)/dt
У нас получилось, что v(H2) = v(I2), но не равно v(HI)! Ведь при уменьшении
концентраций водорода и иода, например, в 3 раза концентрация иодоводорода возрастает в 9 раз
(это видно по коэффициентам в уравнении реакции). Чтобы скорости стали равными (и можно было говорить
о единой скорости реакции), изменение концентрации HI в единицу времени следует поделить на
стехиометрический коэффициент при HI:
v(HI) = dc(HI)/2dt
В общем случае для реакции
aA + bB = eE + fF
значение скорости определяется как:
v = -dc(A)/adt = -dc(B)/bdt = dc(E)/edt = dc(F)/fdt
Приложения
| 






