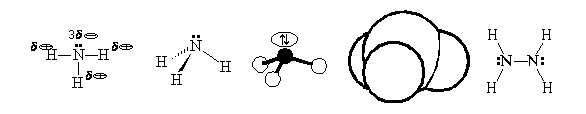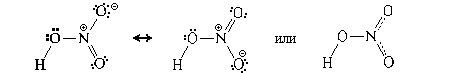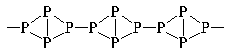С. Т. Жуков Химия 8-9 класс
Глава 16. Элементы IIIA, IVA и VA групп
16.1. Общая характеристика элементов
IIIA, IVA и VA групп
IIIA |
IVA |
VA |
B
Бор
0,776 |
C
Углерод
0,620 |
N
Азот
0,521 |
Al
Алюминий
1,312 |
Si
Кремний
1,068 |
P
Фосфор
0,919 |
Ga
Галлий
1,254 |
Ge
Германий
1,090 |
As
Мышьяк
1,001 |
In
Индий
1,382 |
Sn
Олово
1,240 |
Sb
Сурьма
1,193 |
Tl
Таллий
1,319 |
Pb
Свинец
1,215 |
Bi
Висмут
1,295 |
Состав этих трех групп естественной
системы элементов показан на рисунке 16.1. Здесь же
приведены значения орбитальных радиусов атомов
(в ангстремах). Именно в этих группах наиболее
четко прослеживается граница между элементами,
образующими металлы (орбитальный радиус больше
1,1 ангстрема), и элементами, образующими
неметаллы (орбитальный радиус меньше 1,1
ангстрема). На рисунке эта граница показана
двойной линией. Не следует забывать, что граница
эта все же условна: алюминий, галлий, олово,
свинец и сурьма безусловно амфотерные металлы,
но и бор, германий, мышьяк проявляют некоторые
признаки амфотерности.
Из атомов элементов этих трех групп в земной коре
чаще всего встречаются следующие: Si (w = 25,8
%), Al (w = 7,57 %), P (w = 0,090 %), C (w = 0,087 %) и N (w = 0,030 %).
Именно с ними вы и познакомитесь в этой главе.
Общие валентные электронные формулы атомов
элементов IIIA группы – ns2np1, IVA
группы – ns2np2, VA группы – ns2np3.
Высшие степени окисления равны номеру группы.
Промежуточные на 2 меньше.
Все простые вещества, образуемые атомами этих
элементов (за исключением азота) – твердые. Для
многих элементов характерна аллотропия (B, C, Sn, P,
As). Устойчивых молекулярных веществ всего три:
азот N2, белый фосфор P4 и желтый мышьяк
As4.
Элементы-неметаллы этих трех групп
склонны образовывать молекулярные водородные
соединения с ковалентными связями. Причем у
углерода их так много, что углеводороды и их
производные изучает отдельная наука –
органическая химия. Второй по количеству
водородных соединений среди этих элементов –
бор. Бороводороды (бораны) весьма многочисленны и
сложны по строению, поэтому химия бороводородов
также выделилась в отдельный раздел химии.
Кремний образует всего 8 водородных соединений
(силанов), азот и фосфор – по два, остальные – по
одному водородному соединению. Молекулярные
формулы простейших водородных соединений и их
названия:
B2H6 –
диборан; |
CH4 – метан; |
NH3 – аммиак; |
|
SiH4 – силан; |
PH3 – фосфин; |
|
GeH4 – герман; |
AsH3 – арсин. |
Состав высших оксидов соответствует
высшей степени окисления, равной номеру группы.
Тип высших оксидов в каждой из групп с
увеличением порядкового номера постепенно
меняется от кислотного к амфотерному или
основному.
Кислотно-основный характер
гидроксидов весьма разнообразен. Так, HNO3 –
сильная кислота, а TlOH – щелочь.
 1.Составьте сокращенные электронные формулы и
энергетические диаграммы атомов элементов IIIA, IVA
и VA групп. Укажите внешние и валентные электроны.
1.Составьте сокращенные электронные формулы и
энергетические диаграммы атомов элементов IIIA, IVA
и VA групп. Укажите внешние и валентные электроны.
16.2. Азот
У атома азота есть три неспаренных
электрона, поэтому по обменному механизму он
может образовать три ковалентных связи. Еще одну
ковалентную связь он может образовать по
донорно-акцепторному механизму, при этом атом
азота приобретает положительный формальный
заряд +1 е. Таким образом, максимально азот
пятивалентен, но его максимальная ковалентность
равна четырем.(Именно этим объясняется часто
свтречающееся утверждение о том, что азот не
может быть пятивалентным)
Почти весь земной азот находится в атмосфере
нашей планеты. Существенно меньшая часть азота
присутствует в литосфере в виде нитратов. Азот
входит в состав органических соединений,
содержащихся во всех организмах и в продуктах их
разложения.
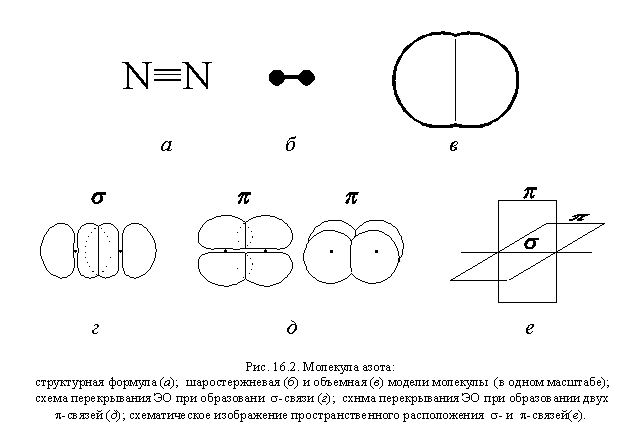
Азот образует единственное простое
молекулярное вещество N2 с тройной
связью двухатомной в молекуле (рис. 16.2). Энергия
этой связи равна 945 кДж/моль, что превышает
значения других энергий связи (см. таблицу 21).
Этим объясняется инертность азота при обычных
температурах. По физическим характеристикам
азот – бесцветный газ без запаха, хорошо
знакомый нам с рождения (земная атмосфера на три
четверти состоит из азота). В воде азот
малорастворим.
Азот образует два водородных
соединения: аммиак NH3 и гидразин N2H6:
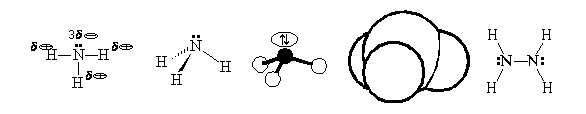
Аммиак – бесцветный газ с резким
удушающим запахом. Неосторожное вдыхание
концентрированных паров аммиака может привести
к спазму и удушью. Аммиак очень хорошо растворим
в воде, что объясняется образованием каждой
молекулой аммиака четырех водородных связей с
молекулами воды.
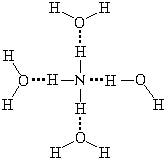
Молекула аммиака – частица-основание
(см. приложение 14). Принимая протон она
превращается в ион аммония. Реакция может
протекать как в водном растворе, так и в газовой
фазе:
NH3 + H2O 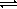 NH4
NH4 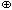 + OH
+ OH 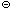 (в растворе);
(в растворе);
NH3 + H3O B = NH4 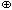 + H2O (в растворе);
+ H2O (в растворе);
NH3г + HClг = NH4Clкр (в газовой
фазе).
Водные растворы аммиака достаточно
щелочные для осаждения нерастворимых
гидроксидов, но недостаточно щелочные для того,
чтобы амфотерные гидроксиды растворялись в них с
образованием гидроксокомплексов. Поэтому
раствор аммиака удобно использовать для
получения амфотерных гидроксидов p-элементов:
Al(OH)3, Be(OH)2, Pb(OH)2 и т. п., например:
Pb2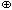 + 2NH3
+ 2H2O = Pb(OH)2 + 2NH4
+ 2NH3
+ 2H2O = Pb(OH)2 + 2NH4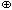 .
.
При поджигании на воздухе аммиак
сгорает, образуя азот и воду; при взаимодействии
с кислородом в присутствии катализатора (Pt)
обратимо окисляется до монооксида азота:
4NH3 + 3O2 = 2N2 + 6H2O
(без катализатора),
4NH3 + 5O2 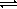 4NO + 6H2O (с катализатором).
4NO + 6H2O (с катализатором).
При нагревании аммиак может
восстанавливать оксиды не очень активных
металлов, например, меди:
3CuO + 2NH3 = 3Cu + N2 + 3H2O
Соли аммония по своим свойствам
(кроме термической устойчивости) похожи на соли
щелочных металлов. как и последние, почти все они
растворимы в воде, но, так как ион аммония
является слабой кислотой, гидролизованы по
катиону. При нагревании соли аммония
разлагаются:
NH4Cl = NH3  + HCl
+ HCl  ;
;
(NH4)2SO4 = NH4HSO4 + NH3 ;
;
(NH4)2CO3 = 2NH3 + CO2
+ CO2 + H2O
+ H2O
 ;
;
NH4HS = NH3 + H2S
+ H2S ;
;
NH4NO3 = N2O + 2H2O
+ 2H2O ;
;
NH4NO2 = N2 + 2H2O
+ 2H2O ;
;
(NH4)2HPO4 = NH3 + (NH4)H2PO4;
+ (NH4)H2PO4;
(NH4)H2PO4 = NH4PO3 + H2O .
.
Азот в различных степенях окисления
образует с кислородом пять оксидов: N2O,
NO, N2O3, NO2 и N2O5.
Наиболее устойчив из них диоксид азота. Это бурый
ядовитый газ с неприятным запахом. Реагирует с
водой:
2NO2 + H2O = HNO2 + HNO3.
С раствором щелочи реакция идет с
образованием нитрата и нитрита.
N2O и NO – несолеобразующие оксиды.
N2O3 и N2O5 – кислотные
оксиды. Реагируя с водой, они соответственно
образуют растворы азотистой и азотной кислот.
Оксокислота азота в степени
окисления +III – азотистая кислота HNO2. Это
слабая кислота, молекулы которой существуют
только в водном растворе. Ее соли – нитриты. Азот
в азотистой кислоте и нитритах легко окисляется
до степени окисления +V.
В отличие от азотистой, азотная
кислота HNO3 – сильная кислота. Строение ее
молекулы может быть выражено двумя способами:
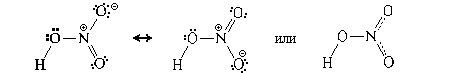
С водой азотная кислота смешивается во
всех отношениях, в разбавленных растворах нацело
с ней реагируя:
HNO3 + H2O = H3O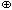 + NO3
+ NO3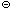
Азотная кислота и ее растворы –
сильные окислители. При разбавлении азотной
кислоты ее окислительная активность снижается. В
растворах азотной кислоты любой концентрации
атомами окислителями являются прежде всего
атомы азота, а не водорода. Поэтому при окислении
азотной кислотой различных веществ водород если
и выделяется, то только как побочный продукт. В
зависимости от концентрации кислоты и
восстановительной активности другого реагента,
продуктами реакции могут быть NO2, NO, N2O,
N2 и даже NH4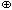 . Чаще всего образуется смесь газов, но в случае
концентрированной азотной кислоты выделяется
только диоксид азота:
. Чаще всего образуется смесь газов, но в случае
концентрированной азотной кислоты выделяется
только диоксид азота:
Cu + 4HNO3 = Cu(NO3)2 + 2NO2 +
2H2O
3FeS + 30HNO3 = Fe2(SO4)3 + Fe(NO3)3
+ 27NO2 + 15H2O
+ 15H2O
В случае разбавленной азотной кислоты
чаще всего выделяется монооксид азота:
Fe + 4HNO3 = Fe(NO3)3 + NO + 2H2O
3H2S + 2HNO3 = 2NO + 4H2O + 3S
В случае очень разбавленной азотной
кислоты, реагирующей с сильным восстановителем
(Mg, Al, Zn), образуются ионы аммония:
4Mg + 10HNO3 = 4Mg(NO3)2 + NH4NO3
+ 3H2O
Те металлы, которые пассивируются
концентрированной серной кислотой,
пассивируются и концентрированной азотной
кислотой.
Соли азотной кислоты – нитраты – термически
неустойчивые соединения. При нагревании они
разлагаются:
2KNO3 = 2KNO2 + O2 ;
;
2Zn(NO3)2 = 2ZnO + 4NO2 + O2
+ O2 ;
;
2AgNO3 = 2Ag + 2NO2 + O2
+ O2 .
.
 1.Составьте уравнения реакций, данных в тексте
параграфа описательно.
1.Составьте уравнения реакций, данных в тексте
параграфа описательно.
2.Составьте уравнения реакций, характеризующих
химические свойства а) аммиака, б) азотной
кислоты, в) нитрата цинка.
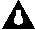 Химические свойства аммиака и азотной кислоты.
Химические свойства аммиака и азотной кислоты.
16.3. Фосфор
В отличие от атома азота, атом
фосфора может образовывать пять ковалентных
связей по обменному механизму. Традиционное
объяснение этого сводится к возможности
возбуждения одного из 3s-электронов и переход
его на 3d-подуровень.
Элемент фосфор образует довольно много аллотропных
модификаций. Из них наиболее устойчивы три
модификации: белый фосфор, красный фосфор и
черный фосфор. Белый фосфор – воскообразное
ядовитое склонное к самовозгоранию на воздухе
вещество, состоящее из молекул P4. Красный
фосфор – немолекулярное менее активное вещество
темно-красного цвета с довольно сложным
строением. Обычно красный фосфор всегда содержит
примесь белого, поэтому и белый, и красный фосфор
всегда хранят под слоем воды. Черный фосфор –
также немолекулярное вещество со сложным
каркасным строением.
Молекулы белого фосфора тетраэдрические, атом
фосфора в них трехвалентен. Шаростержневая
модель и структурная формула молекулы белого
фосфора:
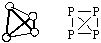
Строение красного фосфора может быть
выражено структурной формулой:
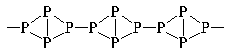
Получают фосфор из фосфата кальция при
нагревании с песком и коксом:
Ca3(PO4)2 + 3SiO2 + 5C =
3CaSiO3 + 2P + 5CO.
Для фосфора наиболее характерны
соединения со степенью окисления +V. При
взаимодействии с избытком хлора фосфор образует
пентахлорид. При сгорании любой аллотропной
модификации фосфора в избытке кислорода
образуется оксид фосфора(V):
4Р + 5O2 = 2P2O5.
Существует две модификации оксида
фосфора(V): немолекулярная (с простейшей формулой
P2O5) и молекулярная (с молекулярной
формулой P4O10). Обычно оксид фосфора
представляет собой смесь этих веществ.
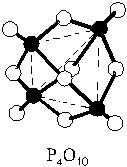
Этот очень гигроскопичный кислотный оксид,
реагируя с водой, образует последовательно
метафосфорную, дифосфорную и ортофосфорную
кислоты:
P2O5 + H2O = 2HPO3, 2HPO3
+ H2O = H4P2O7, H4P2O7
+ H2O = 2H3PO4.
Ортофосфорная кислота (обычно ее
называют просто фосфорной) – трехосновная
слабая кислота (см. приложение 13). Это бесцветное
кристаллическое вещество, очень хорошо
растворимое в воде. При реакции с сильными
основаниями в зависимости от соотношения
реагентов образует три ряда солей
(ортофосфаты, гидроортофосфаты и
дигидроортофосфаты – обычно в их названиях
приставку "орто" опускают):
H3PO4 + OH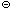 = H2PO4
= H2PO4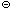 + H2O,
+ H2O,
H3PO4 + 2OH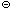 =
HPO42
=
HPO42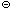 + 2H2O,
+ 2H2O,
H3PO4 + 3OH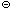 =
PO43
=
PO43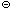 + 3H2O.
+ 3H2O.
Большинство средних фосфатов
(исключение – соли щелочных элементов кроме
лития) нерастворимы в воде. Растворимых кислых
фосфатов существенно больше.
Фосфорную кислоту получают из природного
фосфата кальция, обрабатывая его избытком серной
кислоты. При другом соотношении фосфата кальция
и серной кислоты образуется смесь
дигидрофосфата и сульфата кальция, используемая
в сельском хозяйстве в качестве минерального
удобрения под названием "простой
суперфосфат":
Ca3(PO4)2 + 3H2SO4 = 2H3PO4
+ 3CaSO4;
Ca3(PO4)2 + 2H2SO4 = Ca(H2PO4)2
+ 2CaSO4.
Более ценный "двойной
суперфосфат" получают по реакции
Ca3(PO4)2 + 4H3PO4
= 3Ca(H2PO4)3.
Основным веществом этого минерального
удобрения является дигидрофосфат кальция.
 1.Составьте
молекулярные уравнения реакций, для которых в
тексте параграфа приведены ионные уравнения.
1.Составьте
молекулярные уравнения реакций, для которых в
тексте параграфа приведены ионные уравнения.
2.Составьте уравнения реакций, данных в тексте
параграфа описательно.
3.Составьте уравнения реакций, характеризующих
химические свойства а) фосфора, б) оксида
фосфора(V), в) ортофосфорной кислоты, г)
дигидрофосфата натрия.
 Химические свойства фосфорной кислоты.
Химические свойства фосфорной кислоты.
16.4. Углерод
Углерод – основная составная часть всех
организмов. В природе встречаются как простые
вещества, образованные углеродом (алмаз, графит),
так и соединения (углекислый газ, различные
карбонаты, метан и другие углеводороды в составе
природного газа и нефти). Массовая доля углерода
в каменных углях доходит до 97 %.
Атом углерода в основном состоянии может
образовать две ковалентных связи по обменному
механизму, но в обычных условиях такие
соединения не образуются. Атом углерода,
переходя в возбужденное состояние, использует
все четыре валентных электрона.
Углерод образует довольно много аллотропных
модификаций (см. рис. 16.2). Это алмаз, графит,
карбин, различные фуллерены.
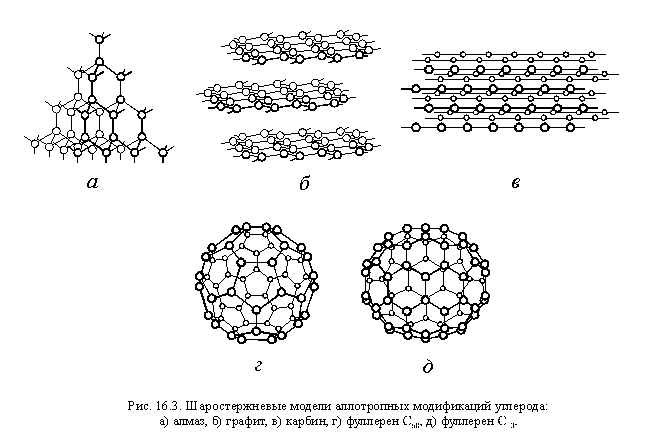
Алмаз – очень твердое бесцветное
прозрачное кристаллическое вещество. Кристаллы
алмаза состоят из атомов углерода в sp3-гибридизованном
состоянии, образующих пространственный каркас.
Графит – довольно мягкое кристаллическое
вещество серо-черного цвета. Кристаллы графита
состоят из плоских слоев, в которых атомы
углерода находятся в sp2-гибридном
состоянии и образуют сетки с шестигранными
ячейками.
Карбин – бесцветное вещество волокнистого
строения, состоящее из линейных молекул, в
которых атомы углерода находятся в sp-гибридном
состоянии (=С=С=С=С= или –С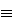 С–С
С–С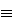 С–).
С–).
Фуллерены – молекулярные аллотропные
модификации углерода с молекулами C60, C80
и др. Молекулы этих веществ представляют собой
полые сетчатые сферы.
Все модификации углерода проявляют
восстановительные свойства в большей степени,
чем окислительные, например, кокс (продукт
переработки каменного угля; содержит до 98 %
углерода) используется для восстановления
железа из оксидных руд и ряда других металлов из
их оксидов:
Fe2O3 + 3C = 2Fe + 3CO (при высокой
температуре).
Большую часть соединений углерода
изучает органическая химия, с которой вы
познакомитесь в 10-м и 11-м классах.
В неорганических веществах степень окисления
углерода +II и +IV. С такими степенями окисления
углерода существуют два оксида.
Оксид углерода(II) – бесцветный ядовитый газ, без
запаха. Тривиальное название – угарный газ.
Образуется при неполном сгорании
углеродсодержащего горючего. Электронное
строение его молекулы см. на стр. 121. По химическим
свойствам CO несолеобразующий оксид, при
нагревании проявляет восстановительные
свойства (восстанавливает до металла многие
оксиды не очень активных металлов).
Оксид углерода(IV) – бесцветный газ без запаха.
Тривиальное название – углекислый газ.
Кислотный оксид. В воде малорастворим
(физически), частично реагирует с ней, образуя
угольную кислоту H2CO3 (молекулы
этого вещества существуют только в очень
разбавленных водных растворах).
Угольная кислота – кислота очень слабая (см.
приложение 13), двухосновная, образует два ряда солей
(карбонаты и гидрокарбонаты). Большинство
карбонатов нерастворимо в воде. Из
гидрокарбонатов как индивидуальные вещества
существуют только гидрокарбонаты щелочных
металлов и аммония. И карбонат-ион, и
гидрокарбонат-ион – частицы основания, поэтому и
карбонаты, и гидрокарбонаты в водных растворах
подвергаются гидролизу по аниону.
Из карбонатов наибольшее значение имеют
карбонат натрия Na2CO3 (сода,
кальцинированная сода, стиральная сода),
гидрокарбонат натрия NaHCO3 (питьевая сода,
пищевая сода), карбонат калия K2CO3
(поташ) и карбонат кальция CaCO3 (мел, мрамор,
известняк).
Качественная реакция на присутствие в
газовой смеси углекислого газа: образование
осадка карбоната кальция при пропускании
исследуемого газа через известковую воду
(насыщенный раствор гидроксида кальция) и
последующее растворение осадка при дальнейшем
пропускании газа. Протекающие реакции:
Ca2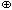 + 2OH
+ 2OH 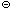 +CO2 = CaCO3
+CO2 = CaCO3 + H2O;
+ H2O;
CaCO3 + CO2 + H2O = Ca2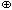 +2HCO3
+2HCO3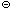 .
.
 1.
Составьте молекулярные уравнения реакций, для
которых в тексте параграфа приведены ионные
уравнения. 2.Составьте уравнения реакций, данных
в тексте параграфа описательно. Составьте
уравнения реакций, характеризующих химические
свойства а) диоксида углерода, б) карбоната калия,
в) карбоната кальция, г) гидрокарбоната натрия.
1.
Составьте молекулярные уравнения реакций, для
которых в тексте параграфа приведены ионные
уравнения. 2.Составьте уравнения реакций, данных
в тексте параграфа описательно. Составьте
уравнения реакций, характеризующих химические
свойства а) диоксида углерода, б) карбоната калия,
в) карбоната кальция, г) гидрокарбоната натрия.
 Получение и свойства углекислого газа.
Получение и свойства углекислого газа.
16.5. Кремний
Кремний входит в состав большинства
горных пород литосферы нашей планеты. Он
образует множество минералов, из которых
простейший по составу – кварц (SiO2). Кварц
входит в состав гранитов и других горных пород.
Элемент кремний образует одно простое вещество
с тем же названием. Это немолекулярное вещество
со структурой алмаза, которому кремний лишь
немного уступает по твердости. За последние
полвека кремний стал абсолютно необходимым
материалом для нашей цивилизации, так как его
монокристаллы используются практически во всей
электронной аппаратуре.
Кремний – довольно инертное вещество. при
комнатной температуре он практически ни с чем
кроме фтора и фтороводорода не реагирует:
Si + 2F2 = SiF4;
Si + 4HF = SiF4 + 2H2.
При нагревании в виде тонко измельченного
порошка сгорает в кислороде, образуя диоксид (SiO2).
При сплавлении со щелочью или при кипячении с
концентрированными растворами щелочей образует
силикаты:
Si + 4NaOH = Na4SiO4 + 2H2;
Si + 2NaOH + H2O = Na2SiO3 + 2H2.
Монооксид кремния SiO –
несолеобразующий оксид; легко окисляется до
диоксида.
Диоксид кремния SiO2 – немолекулярное
вещество каркасного строения. С водой не
реагирует. кислотный оксид – при сплавлении со
щелочами образует силикаты, например:
SiO2 + 2NaOH = Na2SiO3 + H2O .
Кремниевая кислота (точнее метакремниевая) –
немолекулярное вещество с простейшей формулой H2SiO3.
Структурная формула:
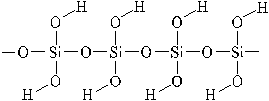
Это очень слабая нерастворимая в воде
кислота. Ее соли образуются при реакции этой
кислоты с растворами щелочей. Они очень сильно
гидролизованы. Большинство силикатов
нерастворимо в воде.
 1.Составьте
уравнения реакций, данных в тексте параграфа
описательно.
1.Составьте
уравнения реакций, данных в тексте параграфа
описательно.
2.Составьте уравнения реакций, характеризующих
химические свойства а) диоксида кремния, б)
силиката натрия.
 Химические свойства силиката натрия
Химические свойства силиката натрия
16.6. Алюминий
Атом алюминия существенно больше по
размерам, чем атомы других разобранных в этой
главе элементов. Он не склонен принимать
электроны, но и затраты энергии на превращение
его в трехзарядный катион очень велики.
Алюминий – следующий по распространенности в
литосфере Земли элемент после кремния.
Самостоятельно и вместе с кремнием он образует
множество минералов: полевые шпаты, слюды, корунд
Al2O3 и его драгоценные разновидности
(бесцветный лейкосапфир, содержащий примеси
хрома рубин, содержащий примеси титана сапфир).
Простое вещество алюминий – серебристо-белый
блестящий легкий металл. Чистый алюминий очень
мягкий, его можно прокатывать в тонкую фольгу,
вытягивать из него проволоку. У алюминия хорошая
электропроводность. Он стоек к атмосферным
воздействиям. Сплавы алюминия достаточно
твердые, но хорошо обрабатываются. Алюминий не
ядовит. Все это позволяет использовать алюминий
в самых разнообразных отраслях промышленности: в
авиационной, электротехнической, пищевой
промышленности, в строительстве. Широко
используется алюминий и в быту. Получают
алюминий путем электролиза расплава его
соединений.
Химическая инертность алюминия вызвана наличием
на его поверхности плотной оксидной пленки,
препятствующей контакту металла с реагентом. При
удалении этой пленки химическим или
механическим путем алюминий становится весьма
активным. Так, лишенный оксидной пленки, алюминий
самовоспламеняется и сгорает на воздухе без
дополнительного нагревания.
Восстановительные свойства алюминия особенно
хорошо проявляются при нагревании. В этих
условиях он восстанавливает из оксидов многие
металлы: не только железо, титан, цирконий, но
даже кальций и барий.
Оксид алюминия Al2O3 (тривиальные
названия – глинозем, корунд) – немолекулярное
вещество, связь в котором плохо описывается и как
ионная, и как ковалентная. Как всегда в этих
случаях это амфотерный оксид. Получают его при
прокаливании гидроксида алюминия, который также
обладает амфотерными свойствами.
Гидратированный ион алюминия – катионная
кислота, поэтому растворимые соли алюминия
довольно сильно гидролизованы.
Из солей алюминия наиболее употребмы
алюмокалиевые квасцы KAl(SO4)2·12H2O
– додекагидрат сульфата калия-алюминия. Это
негигроскопичное прекрасно кристаллизующееся
вещество. Его раствор ведет себя как смесь
растворов двух разных сульфатов: сульфата калия
и сульфата алюминия. Строение квасцов может быть
выражено формулой: [K(H2O)6][Al(H2O)6](SO4)2.
 1.Составьте уравнения реакций,
данных в тексте параграфа описательно.
1.Составьте уравнения реакций,
данных в тексте параграфа описательно.
2.Составьте уравнения реакций, характеризующих
химические свойства а) алюминия, б) гидроксида
алюминия, и) алюмокалиевых квасцов..
 Химические свойства солей алюминия
Химические свойства солей алюминия