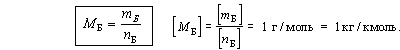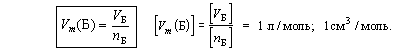С. Т. Жуков Химия 8-9 класс
Глава 5.Важнейшие физические величины ,
соотношения и расчеты в химии
5.1. Характеристики, свойства и
физические величины
В предыдущих главах вы неоднократно
сталкивались с характеристиками. Мы говорили о
характеристиках химических веществ и реакций, о
характеристиках атомов и атомных ядер, о
характеристиках элементов и изотопов, а также
других объектов или явлений.
Среди множества характеристик мы выделили
характеристики, называемые свойствами объектов,
выяснили, что свойства могут быть физическими и
химическими, и познакомились с некоторыми из них.
Из курса физики вам известна еще одна группа
характеристик. Это – физические величины. С
ними мы сталкиваемся, как только хотим
количественно описать какой-нибудь объект (или
явление). Например, сравнивая атомы, мы говорим об
их массе и о числе частиц, их составляющих.
Сравнивая частицы, мы приводим их массу и
электрический заряд. Описывая химическую
реакцию, мы говорим о ее скорости, а характеризуя
условия протекания реакции, используем
физическую величину, называемую температурой. И
так далее.
Таким образом, среди великого множества самых
разнообразных характеристик объектов или
явлений мы выделяем две большие группы: а)
свойства – часть чисто качественных
характеристик и б) физические величины –
качественные и одновременно количественные
характеристики этих объектов или явлений.
Следует четко различать сами объекты и явления
(реально существуют или происходят в Природе), их
характеристики и, в частности, свойства
(проявляются объектами и явлениями) и физические
величины (качественно и количественно
характеризуют объекты или явления). Например:
вещество свинец – объект, способность свинца
плавиться – его свойство, а температура
плавления свинца – физическая величина (в том
числе говорящая нам, что свинец способен
плавиться). Физические величины не являются
свойствами, а свойства, в свою очередь, не могут
быть физическими величинами. Перечисляя
свойства и характеристики объекта, можно описать
его только качественно, а, используя физические
величины, можно охарактеризовать объект и
качественно, и количественно.
Каждый объект (тело, вещество или частица), как
правило, обладает несколькими свойствами и
характеристиками и может характеризоваться
несколькими разными физическими величинами.
 ХАРАКТЕРИСТИКИ,
СВОЙСТВА, ФИЗИЧЕСКИЕ ВЕЛИЧИНЫ.
ХАРАКТЕРИСТИКИ,
СВОЙСТВА, ФИЗИЧЕСКИЕ ВЕЛИЧИНЫ.
 1)Используя
известные вам качественные характеристики (в том
числе и свойства) опишите следующие объекты:
1)Используя
известные вам качественные характеристики (в том
числе и свойства) опишите следующие объекты:
а) ядро атома гелия-4,
б) атом углерода-12,
в) лёд.
Используйте известные вам физические величины
для характеристики этих объектов.
2)Проиллюстрируйте ряд объект — свойство —
физическая величина тремя примерами.
5.2. Основные сведения о физических
величинах
| Физическая величина (величина) –
характеристика материального объекта (или
явления), одинаковая в качественном отношении
для многих объектов, но в количественном
отношении индивидуальная для каждого объекта. |
В качественном отношении физическая величина
показывает, что все объекты какой-либо группы
обладают определенным свойством. В
количественном отношении она показывает,
насколько интенсивно конкретный объект
проявляет это свойство.
Каждая физическая величина имеет название
и обозначение, например: длина – l, масса
– т, количество теплоты – Q, удельная
теплота плавления –  , сила
света – Iv. Так как физическая величина
характеризует конкретный объект или явление, то
в обозначении величины указывается этот объект
(или явление) в виде индекса, например: масса
первого тела – m1, масса второго тела – m2,
масса раствора – mр, масса серебра – mAg
и т. п. Если обозначение величины само содержит
индекс или индексы содержатся в обозначении
объекта, то обозначение объекта приводится в
скобках, например: масса атома серебра – mo(Ag),
объем раствора поваренной соли – Vp(NaCl),
плотность сульфата натрия –
, сила
света – Iv. Так как физическая величина
характеризует конкретный объект или явление, то
в обозначении величины указывается этот объект
(или явление) в виде индекса, например: масса
первого тела – m1, масса второго тела – m2,
масса раствора – mр, масса серебра – mAg
и т. п. Если обозначение величины само содержит
индекс или индексы содержатся в обозначении
объекта, то обозначение объекта приводится в
скобках, например: масса атома серебра – mo(Ag),
объем раствора поваренной соли – Vp(NaCl),
плотность сульфата натрия –  (Na2SO4).
Если речь идет о единственном (или о любом)
объекте, то обозначение объекта не приводится
(так вы обычно поступаете, решая задачи по
физике).
(Na2SO4).
Если речь идет о единственном (или о любом)
объекте, то обозначение объекта не приводится
(так вы обычно поступаете, решая задачи по
физике).
Рассмотрим подробно физическую величину,
называемую "длина" . Эта величина
характеризует протяженность объекта, системы
или ее части. Возьмем карандаш и указку – каждый
из этих объектов обладает протяженностью,
следовательно, может быть охарактеризован
длиной. Мы можем сравнить карандаш и указку по
длине – указка длиннее карандаша, следовательно,
длина карандаша и длина указки разная. Мы можем
сравнивать протяженность и других объектов;
линейки, коридора, Останкинской башни (см.,
например, рис. 1.5). Но мы не можем с длиной линейки
сравнивать вес яблока, а с длиной коридора –
продолжительность урока. С другой стороны, тот же
коридор имеет длину, ширину, высоту и их тоже
можно сравнивать между собой. Характеристики
протяженности имеют и многие материальные
системы: расстояние между фонарными столбами,
городами, планетами; межатомные расстояния в
молекулах и кристаллах. Все эти характеристики
(длина, ширина, высота, расстояние) при всем их
различии отражают одну и ту же качественную
особенность объекта, системы или части системы –
протяженность. Таким образом, физическая
величина " длина" для разных объектов и
систем имеет общую качественную особенность – род
величины, и совершенно разную количественную
особенность – размер величины.
| Род величины – качественная сторона этой
величины, показывающая, какую особенность
объекта данная величина характеризует. |
| Размер величины – количественная сторона
этой величины, показывающая, насколько
интенсивно данная особенность проявляется
объектом. |
| Однородные величины – величины,
одинаковые в качественном отношении
(характеризующие одну и ту же особенность
объектов). |
Следовательно, длина, ширина, высота,
расстояние – однородные величины. Однородные
величины можно сравнивать между собой по
размеру. Так, мы можем сравнивать радиус атома с
расстоянием между молекулами, массу атома с
массой слитка металла, длительность урока с
периодом обращения Земли вокруг Солнца. Но мы не
можем сравнивать температуру воздуха в комнате с
теплотой плавления льда или удельную
теплоемкость меди с массой слитка этого металла
– это пары величин разного рода (характеризуют
разные свойства).

Размер величины для каждого объекта существует
независимо от того, определяем мы его или нет.
Очевидно, что и указка, и Останкинская башня
имеют каждая вполне определенную длину, причем
разную. Как же определить размер величины?
Величину необходимо измерить, то есть сравнить с
другой однородной величиной, служащей неким
эталоном данной физической величины. В
результате измерения мы получаем значение
величины. Таким образом, значение физической
величины возникает только в результате ее
измерения.
Значение величины включает в себя числовое
значение величины и единицу измерений.
| Числовое значение величины – отвлеченное
число, входящее в значение величины. |
Числовое значение величины показывает, во
сколько раз размер измеряемой величины больше
размера единицы измерений. Следовательно,
числовое значение величины зависит от размера
выбранной единицы измерений.
| Единица измерений физической величины –
физическая величина фиксированного размера,
однородная измеряемой, которой условно
присвоено числовое значение, равное единице. |
В общем случае для обозначения числового
значения величины, например l , используют
фигурные скобки: {l}, а для
обозначения единицы измерений – квадратные: [l].
Значение величины есть произведение числового
значения величины на размер выбранной единицы
измерений. В случае длины l = {l}.[l].
Значение величины не зависит от выбора единицы
ее измерений. Действительно, высота Останкинской
телебашни (значение величины) не зависит от того,
какой единицей измерений мы будем пользоваться
– метром, футом, аршином или чем-нибудь другим. Но
числовые значения при этом будут получаться
разные. Или вспомните, как герои известного
мультфильма измеряли длину удава: в "
попугаях" у них получалось одно числовое
значение, а в " мартышках" – другое. Но
удав-то оставался тем же самым, и той же самой
оставалась его длина.
Разные величины связаны между собой уравнениями
связи, например: F = m.a, W =
F.s, 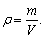
| Уравнения связи между величинами –
уравнения, отражающие законы Природы, в которых
под буквенными обозначениями понимаются
величины. |
Изучение связей между величинами показало, что,
если произвольно выбрать определенное число
физических величин в качестве основных, то
остальные величины (производные) могут быть
выражены через основные величины с помощью
уравнений связи. Все величины, вместе взятые,
образуют систему физических величин.
| Основные физические величины – величины,
входящие в систему величин и условно принятые
независимыми от других величин системы. |
| Производные физические величины – величины,
входящие в систему величин и определяемые через
основные величины этой системы. |
В принятой сейчас в науке и технике системе
величин за основные выбраны следующие семь
величин: длина – l, масса – т, время – t,
сила электрического тока – I,
термодинамическая температура – Т,
количество вещества – п, сила света – Iv.
Системе физических величин соответствует
система единиц измерений этих величин. Система
единиц измерений строится так: для каждой
основной величины произвольно (из соображений
удобства) выбирают одну единицу измерений и из
этих основных единиц в соответствии с
уравнениями связи получают единицы измерений
производных величин – производные единицы.
Размеры основных единиц измерений утверждаются
международными научными организациями. В
настоящее время наиболее распространенной (но
далеко не оптимальной) является Международная
система единиц (СИ).
Для удобства измерения величин, размер которых
намного больше или намного меньше размера
единицы измерений, используются кратные или дольные
единицы измерений (километр, миллиметр и
т. п.). Но и они не всегда удобны, поэтому в ряде
случаев допускается применение внесистемных
единиц. Так, давление удобно измерять в
атмосферах, размеры атомов и молекул – в
ангстремах, а заряды ядер – в элементарных
электрических зарядах.
Складывать и вычитать можно только однородные
величины, да и то не все (например, массы разных
веществ – можно, а их плотности – нельзя, так как
получится абсурд), а умножать и делить друг на
друга можно любые величины, помня только, что при
этом получаются совсем новые величины.
В химии наименование и обозначение физических
величин, применение единиц измерений, вопросы
терминологии и многие другие регламентируются
" Номенклатурными правилами ИЮПАК по химии"
.
| ИЮПАК – Международный союз теоретической
и прикладной химии (IUPAC – International Union of Pure and Applied
Chemistry) – неправительственная научная
организация, входящая в Международный совет
научных союзов. Создана в 1919 году для координации
исследований в области химии и химической
промышленности, требующих международного
согласования, контроля и стандартизации. Членами
ИЮПАК являются научные учреждения и
промышленные фирмы более чем из 50 стран мира, и,
кроме того, международные объединения по
отдельным областям химии. В ведении ИЮПАК
находится разработка общих принципов и правил
химической номенклатуры, терминологии,
символики; стандартизация методов измерений в
области химии; создание баз данных по различным
химическим направлениям, а также другие вопросы,
требующие международных договоренностей. |
 ФИЗИЧЕСКАЯ
ВЕЛИЧИНА,РОД ВЕЛИЧИНЫ,РАЗМЕР ВЕЛИЧИНЫ,
ОДНОРОДНЫЕ ВЕЛИЧИНЫ, ЧИСЛОВОЕ ЗНАЧЕНИЕ ВЕЛИЧИНЫ,
ЕДИНИЦА ИЗМЕРЕНИЙ, УРАВНЕНИЯ СВЯЗИ МЕЖДУ
ВЕЛИЧИНАМИ,ОСНОВНЫЕ ФИЗИЧЕСКИЕ ВЕЛИЧИНЫ,
ПРОИЗВОДНЫЕ ФИЗИЧЕСКИЕ ВЕЛИЧИНЫ
ФИЗИЧЕСКАЯ
ВЕЛИЧИНА,РОД ВЕЛИЧИНЫ,РАЗМЕР ВЕЛИЧИНЫ,
ОДНОРОДНЫЕ ВЕЛИЧИНЫ, ЧИСЛОВОЕ ЗНАЧЕНИЕ ВЕЛИЧИНЫ,
ЕДИНИЦА ИЗМЕРЕНИЙ, УРАВНЕНИЯ СВЯЗИ МЕЖДУ
ВЕЛИЧИНАМИ,ОСНОВНЫЕ ФИЗИЧЕСКИЕ ВЕЛИЧИНЫ,
ПРОИЗВОДНЫЕ ФИЗИЧЕСКИЕ ВЕЛИЧИНЫ
 1.Распределите
величины по семействам однородных величин:
работа, температура, потенциальная энергия,
удельная теплоемкость, количество теплоты,
температура плавления, кинетическая энергия,
температура кипения. Как доказать, что собранные
в семейства величины – однородные?
1.Распределите
величины по семействам однородных величин:
работа, температура, потенциальная энергия,
удельная теплоемкость, количество теплоты,
температура плавления, кинетическая энергия,
температура кипения. Как доказать, что собранные
в семейства величины – однородные?
2.Как значения величины, выраженные в одних
единицах измерений, выразить в других единицах?
Приведите любые известные вам примеры.
5.3. Важнейшие физические величины,
характеризующие атомы и молекулы
С основными количественными характеристиками
атомов вы познакомились в главе 4. Кроме числа
протонов в ядре (Z), числа нейтронов в ядре (N)
и массового числа (A) это
а) масса атома (нуклида), mо(AЭ), [mо(AЭ)]
= 1 г или 1 кг;
б) атомная масса нуклида, Аr(AЭ), [Аr(AЭ)]
=1 Дн;
в) средняя масса атомов элемента, 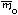 (Э), [
(Э), [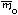 (Э)] = 1 г или 1кг;
(Э)] = 1 г или 1кг;
г) атомная масса элемента, Аr(Э), [Аr(Э)]
= 1 Дн.
Проанализируем эти величины.
Так как масса атома и атомная масса нуклида –
одна и та же величина, но измеренная разными
единицами измерений, то
{m0(AЭ)}.1 г = { Аr(AЭ)}.1
Дн.
Примеры:
для нуклида 1Н
1,67.10– 24.1 г = 1.1 Дн
или
1,67.10– 24 г = 1 Дн |
для нуклида 16О
2,66.10– 23.1 г = 16.1 Дн
или
2,66.10– 23 г = 16.1 Дн |
Совершенно аналогично, средняя масса атомов
элемента и атомная масса элемента – также одна и
та же величина, и в этом случае мы можем записать:
{ 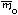 (Э)}.1
г = { Аr(Э)}.1 Дн.
(Э)}.1
г = { Аr(Э)}.1 Дн.
Примеры:
для элемента "
кислород"
2,66.10– 23.l г = 16.1 Дн
или
2,66.10– 23 г = 16 Дн |
для элемента "
золото"
3,29.10– 22.1 г = 197.1 Дн
или
3,29.10– 22г = 197 Дн |
Химические вещества могут состоять из молекул
(молекулярные вещества), а могут и не содержать
таких обособленных незаряженных частиц
(немолекулярные вещества).
Молекулы, как и атомы, естественно, обладают
массой. Масса молекулы равна сумме масс
составляющих ее атомов. Молекулы разных веществ
имеют, как правило, разную массу. Молекулы одного
вещества могут несколько отличаться друг от
друга по массе, ведь в их состав могут входить
атомы разных изотопов. Обычная вода, например,
содержит молекулы 1H216O, 1H2H16O,
2H216O, 1H217O, 1H2H17O,
2H217O, 1H218O, 1H2H18O
и 2H218O.
В ядерной технике получают и используют
вещества, состоящие из совершенно одинаковых
молекул, например 2H216O или 1H218O,
но с такими веществами, а их называют
изотопно-чистыми, химики имеют дело крайне
редко. Обычно чистое молекулярное вещество
содержит молекулы, разные по изотопному составу
и, соответственно, по массе.
Как посчитать среднюю массу молекулы такого
обычного вещества, например H2O? Можно,
конечно, посчитать массу молекулы каждого из
изотопно-чистых веществ, экспериментально
определить доли этих молекул в обычном веществе
и, так же, как мы рассчитывали среднюю массу атома
элемента в природной смеси изотопов, рассчитать
среднюю массу молекулы. Но можно воспользоваться
атомными массами элементов, ведь это уже средние
массы, и в них учтены доли изотопов в природной
смеси:
Mr(H2O) = 2Ar(H) + Ar(O).
Здесь Mr(H2O) – молекулярная
масса воды.
| Молекулярная масса вещества – средняя
масса молекулы этого вещества, выраженная в
дальтонах. |
Молекулярная масса вещества рассчитывается по
молекулярной формуле.
Как и для атомов, для молекул (например, молекул
воды) справедливы соотношения
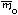 (H2O)
= Mr(H2O) и m0(1H216O)
= Mr(1H216O).
(H2O)
= Mr(H2O) и m0(1H216O)
= Mr(1H216O).
Для характеристики немолекулярных веществ (а
иногда и молекулярных) используется формульная
масса.
| Формульная масса вещества – средняя масса
формульной единицы этого вещества, выраженная в
дальтонах. |
Формульная масса рассчитывается по простейшей
формуле, но обозначается так же, как и
молекулярная масса – Mr, а масса
формульной единицы – так же, как и масса молекулы
– 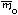 .
.
Для простого немолекулярного вещества
формульная масса равна атомной массе элемента,
например: Mr(К) = Аr(К), Мr(Fe)
= Аr(Fe).
Для международной системы единиц (СИ) дальтон –
внесистемная единица (то есть его в системе нет),
поэтому, измеряя атомную, формульную или
молекулярную массу, приходится массу
соответствующей структурной единицы (то есть
атома, молекулы или формульной единицы)
сравнивать не с дальтоном (как единицей
измерений), а с 1/12 частью массы
нуклида 12С. Получающаяся величина
(отношение) – величина безразмерная, она
называется " относительная атомная
(молекулярная, формульная) масса" и численно
равна атомной (молекулярной, формульной) массе,
выраженной в дальтонах. В химии использовать
относительные массы очень неудобно!
 МОЛЕКУЛЯРНАЯ
МАССА ВЕЩЕСТВА, ФОРМУЛЬНАЯ МАССА ВЕЩЕСТВА
МОЛЕКУЛЯРНАЯ
МАССА ВЕЩЕСТВА, ФОРМУЛЬНАЯ МАССА ВЕЩЕСТВА
 1.Принимая атомную массу нуклида численно равной
массовому числу, определите массы нуклидов а) 14N,
б) 35Cl, в) 65Cu, г) 202Hg.
1.Принимая атомную массу нуклида численно равной
массовому числу, определите массы нуклидов а) 14N,
б) 35Cl, в) 65Cu, г) 202Hg.
2.Используя значения атомных масс (приложение 2),
определите среднюю массу атомов а) азота, б)
хлора, в) меди, г) ртути. Почему средняя масса
атомов элемента отличается от массы отдельного
атома этого элемента?
3.Средняя масса атомов элемента равна а) 1,794.10–
23 г, б) 3,349.10– 23 г, в) 5,324.10– 23
г, г) 6,653.10– 23 г.
4.Определите, какие это элементы. В каком случае
вы можете сомневаться в точности определения
элемента? Выпишите из приложения 2 точные
значения атомных масс следующих элементов: Na, N, О,
Pb, Fe, Ag, U. Округлите эти значения до целого числа
дальтонов.
5.Выпишите точные значения атомных масс для
элементов Cl, Cu и Rb. Округлите их до целого числа
дальтонов и посчитайте относительную ошибку,
вызванную таким округлением. Объясните, почему
атомную массу хлора принято округлять до
значения 35,5 Дн, а атомные массы меди и рубидия –
до целых чисел.
6.Используя округленные до целых чисел значения
атомных масс, определите молекулярные массы
следующих веществ: N2, O2, S8, H2S,
CO2, N2O5, P4O10, CCl2O,
H2SO4, H3PO4.
7.Используя округленные значения атомных масс,
определите формульные массы следующих веществ:
Al, Fe, Na, NaCl, BaO, Al2O3, (CuOH)2CO3, Ca3(PO4)2,
CuSO4.5H2O (точка между формулами
веществ означает, что это единое химическое
вещество; коэффициенты перед составными частями
таких формул имеют тот же смысл, что и индексы в
простейших или молекулярных формулах и
относятся ко всей формуле составной части
вещества, перед которой они поставлены).
8.Определите точное значение формульной массы Ca3(PO4)2,
сравните его с округленным и посчитайте
относительную ошибку, вызванную округлением
атомных масс.
9.Определите молекулярные массы всех
изотопно-чистых веществ, входящих в состав воды.
Посчитайте, во сколько раз и на сколько процентов
масса самой тяжелой молекулы воды больше массы
самой легкой.
10.Смесью скольких изотопно-чистых веществ
является тетрахлорид кремния SiCl4, если для
его получения использовался кремний 28Si и 30Si,
а также хлор 35Сl и 37Сl. Напишите
молекулярные формулы всех этих веществ.
11.Вычислите среднюю массу молекулы воды и
определите, сколько молекул содержится в 100 мл
воды (плотность воды равна 1 г/мл).
5.4. Количество вещества. Моль
Проведем химическую реакцию, протекающую при
взаимодействии алюминия с йодом: 2Аl + 3I2 = 2АlI3.
Из уравнения реакции следует, что
1) алюминий и йод реагируют между собой, образуя
новое вещество – йодид алюминия;
2) в реакцию вступают атомы алюминия и молекулы
йода;
3) отношение числа вступивших в реакцию
формульных единиц (в данном случае - атомов)
алюминия к числу вступивших в реакцию молекул
йода равно 2 к 3, то есть
N(Al) : N(I2) = 2 : 3.
Если для проведения реакции мы возьмем,
например, 1.1020 атомов алюминия, то, для
того, чтобы все они прореагировали, потребуется
1,5.1020 молекул йода. И наоборот, если у
нас есть 90000 молекул йода, то в этом случае, чтобы
все они прореагировали, нужно взять 60000 атомов
алюминия. Если мы возьмем исходные вещества в
другом соотношении, то одно из них останется
непрореагировавшим. В таком случае говорят, что
это вещество было взято в избытке.
Как отмерять взятые для реакции вещества, чтобы
они прореагировали без остатка?
Очевидно, что отмерять вещества следует по числу
атомов, молекул (для молекулярных веществ) или
формульных единиц (для немолекулярных веществ).
Обобщенно атомы, молекулы (реальные частицы),
формульные единицы (выделенные нами "
частицы" ) и другие составные части вещества
называют структурными элементами. Число
таких структурных элементов в порции вещества
является физической величиной, называемой количество
вещества. В нашем случае роль структурных
элементов выполняют частицы – атомы алюминия и
молекулы йода.
Количество вещества –
физическая величина, равная числу структурных
элементов, составляющих систему. |
Роль систем в нашем случае выполняют порции
реагирующих веществ – алюминия и йода.
Количество вещества как физическая величина
обычно характеризует только такие системы,
структурные элементы которых в той или иной
степени одинаковые. Примеры таких структурных
элементов: атомы одного химического элемента,
молекулы или формульные единицы одного вещества,
а также заведомо неразличимые частицы –
электроны, протоны, нейтроны и другие подобные им
микрочастицы.
Обозначается количество вещества латинской
буквой n, а если эта буква уже " занята" ,
то греческой буквой  .
.
Количество вещества – одна из основных
физических величин, поэтому ее единица измерений
выбирается произвольно – только из соображений
удобства.
Что же удобно выбрать за единицу измерений этой
величины? Естественно, штуку. Но поштучно
пересчитать молекулы в химической практике
невозможно, зато вещество можно взвесить, то есть
определить его массу. Следовательно, за единицу
измерений количества вещества следует принять
порцию из определенного и всегда одинакового
числа частиц, достаточно большую, чтобы ее легко
можно было взвесить на обычных весах.
Такая единица измерений получила название моль,
а величина, показывающая массу одного моля
вещества – молярная масса. Молярная масса
вещества Б обозначается МБ, или М(Б).
Таким образом, единица измерений количества
вещества [n] = 1 моль, а единица измерений
молярной массы [МБ] = 1 г/моль.
Физическая величина, показывающая, сколько
частиц содержится в одном моле вещества,
называется постоянной Авогадро и
обозначается NA. Единица измерений этой
величины – " штуки в моле" , но, так как
физики штуку единицей измерений не считают, то
получается
[NA] = 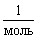 , или [NA] = моль– 1.
, или [NA] = моль– 1.
Значение постоянной Авогадро выбрано таким
образом, чтобы числовое значение молярной массы
любого вещества было равно числовому значению
молекулярной массы, то есть
{M(Б)} = {Mr(Б)}
NA = 6,02.1023 моль– 1
Числовое значение постоянной Авогадро {NA}
называется числом Авогадро.
Таким образом
| Моль – порция из {NA} частиц. |
В Международной системе единиц определение
моля формулируется несколько иначе.
| Моль – единица измерений количества
вещества, равная количеству вещества системы,
содержащей столько же структурных элементов,
сколько содержится атомов в 12 граммах углерода-12. |
Но так как в 12 г углерода-12 содержится {NA}
штук атомов углерода, оба эти определения не
противоречат друг другу.
Применяются кратные и дольные единицы,
производные от моля: 1 кмоль = 1000 моль, 1 ммоль = 0,001
моль и так далее.
Слово " моль" как обозначение единицы
измерений не склоняется (5 моль; 0,25 моль), а в
качестве названия единицы измерений (в тексте и
устной речи) склоняется как существительное
мужского рода (четверть моля, пятью молями, двух
молей и тому подобное).
Число частиц в моле вещества (число Авогадро)
очень велико, поэтому количество макрообъектов в
молях обычно не измеряют, ведь даже звезд в
Метагалактике всего лишь порядка одного моля.
Теперь запишем формально не строгое, но понятное
определение количества вещества:
| Количество вещества – то же, что и число
частиц, но измеряется не в штуках, а в молях (то
есть, порциями по 6,02.1023 штук). |
| Алюминий – Al – легкий пластичный металл.
Как и все металлы – немолекулярное вещество.
Алюминий сравнительно дешев и широко
используется. Самая близкая любому человеку
область его применения – многочисленные бытовые
предметы: от кастрюль до фольги. Из измельченного
до состояния пудры алюминия изготавливают "
серебряную" краску. В некоторых странах,
например в Венгрии, из алюминиевых сплавов
делают монеты. Крупнейшими потребителями
алюминия являются авиационная промышленность,
машиностроение и строительство, не говоря уже о
том, что большая часть электрических проводов (от
линий электропередач до проводов в вашей
квартире) делается из алюминия. Но так было не
всегда. В течение некоторого времени после
открытия (середина XIX века), алюминий был очень
дорогим металлом, т. к. способы получения чистого
алюминия были в то время слишком сложны. В те годы
алюминиевые столовые приборы считались
предметом роскоши. Йод – I2. В быту с
йодом в чистом виде вам сталкиваться не
приходится. Это черно-фиолетовые кристаллы с
металлическим блеском, очень мало растворимые в
воде, зато хорошо растворимые в спирте. Именно
спиртовой раствор йода, используемый в медицине,
в быту и называют просто " йодом" . Йод
извлекают из морской воды, его накапливают
некоторые морские водоросли. В микроколичествах
это вещество необходимо человеку для
правильного функционирования щитовидной и
паращитовидной желез. Он используется в медицине
и быту как дезинфицирующее средство. Йод и его
пары ядовиты. Пары йода раздражают слизистые
оболочки, поэтому при частом воздействии
возможны воспаления слизистых и кожные
дерматиты. |
 ЧИСЛО
ЧАСТИЦ, КОЛИЧЕСТВО ВЕЩЕСТВА, МОЛЬ, СТРУКТУРНЫЙ
ЭЛЕМЕНТ, ИЗБЫТОК ВЕЩЕСТВА В РЕАКЦИИ.
ЧИСЛО
ЧАСТИЦ, КОЛИЧЕСТВО ВЕЩЕСТВА, МОЛЬ, СТРУКТУРНЫЙ
ЭЛЕМЕНТ, ИЗБЫТОК ВЕЩЕСТВА В РЕАКЦИИ.
 1.Используя округленные значения атомных масс
элементов, определите молярные массы следующих
веществ: O2, O3, Cl2, HCl, CO2, H3PO4,
NaCl, Ba(OH)2, Fe2(SO4)3, Ca3(PO4)2.
1.Используя округленные значения атомных масс
элементов, определите молярные массы следующих
веществ: O2, O3, Cl2, HCl, CO2, H3PO4,
NaCl, Ba(OH)2, Fe2(SO4)3, Ca3(PO4)2.
2.Сколько молекул содержится в а) 1 г водорода H2,
б) 1 г кислорода O2, в) 76,8 кг серы S8, г) 9,8
мг серной кислоты H2SO4? 3.Определите
массу а) 6,02.1022 атомов железа; б) 2,107.1025
молекул диоксида углерода СО2; в) 9,03.1022
формульных единиц CuSO4; г) 1,204.1024
электронов.
4.Каково количество вещества атомов кислорода в
3,5 моль газообразного кислорода?
5.Каково количество вещества атомов а) кальция, б)
фосфора, в) кислорода в 1,5 моль Са3(РО4)2?
6.Определите массу водорода, содержащегося в 3,01.1024
молекул метана СН4.
7.Определите количество вещества атомов хлора,
содержащегося в 1,204.1023 молекул
пентахлорида фосфора PCl5.
5.5. Удельные и молярные величины
Из физики вам уже знакомы удельная
теплоемкость, удельная теплота плавления,
удельная теплота парообразования. Все это – удельные
величины.
Удельная величина –
отношение величины, характеризующей порцию
вещества, к массе этой порции. |
Удельная величина показывает значение
соответствующей ей обычной величины для порции
вещества массой 1 килограмм.
Но 1 кг меди содержит одно число атомов меди, а 1 кг
свинца – совсем другое (где больше?). Очень часто,
особенно при химических расчетах, использовать
удельные величины бывает неудобно (почему?). В
этом случае значение величины относят к
стандартному числу частиц – к одному молю, то
есть используют не удельные, а молярные
величины.
Молярная величина – отношение
величины, характеризующей порцию вещества, к
количеству вещества этой порции. |
Молярная величина показывает значение
соответствующей обычной величины для 1 моля
вещества.
С одной из молярных величин вы уже знакомы – это
молярная масса.
Молярная масса вещества Б – отношение
массы порции вещества Б к количеству вещества
этой порции. |
Молярная масса вещества соответствует
массе 1 моля этого вещества.
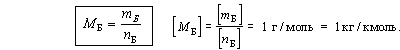
Молярная масса вещества не зависит от внешних
условий и агрегатного состояния вещества.
Молярная масса характеризует не только
химические вещества, но и элементы, изотопы и
любые другие совокупности более или менее
одинаковых частиц (ионов, электронов и т. п.).
Другая часто используемая молярная величина – молярный
объем.
| Молярный объем вещества Б – отношение
объема порции вещества Б к количеству вещества
этой порции. |
Молярный объем вещества соответствует объему 1
моля этого вещества.
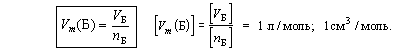
Молярный объем зависит от температуры и
давления и может быть определен для любого
агрегатного состояния вещества.
К молярным величинам относится и постоянная
Авогадро.
| Постоянная Авогадро (" молярное число
частиц" ) – отношение числа частиц в порции
вещества к количеству вещества этой порции. |
Постоянная Авогадро соответствует числу
частиц в одном моле химического вещества,
элемента, изотопа, или любой другой совокупности
более или менее одинаковых частиц.
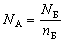 [NA] = 1 моль– 1.
[NA] = 1 моль– 1.
Три приведенные выше уравнения связи дают нам
формулы для вычисления количества вещества,
исходя из других данных:
В дальнейшем мы познакомимся и с другими
молярными величинами.
 УДЕЛЬНАЯ
ВЕЛИЧИНА, МОЛЯРНАЯ ВЕЛИЧИНА, МОЛЯРНАЯ МАССА
ВЕЩЕСТВА, МОЛЯРНЫЙ ОБЪЕМ ВЕЩЕСТВА, ПОСТОЯННАЯ
АВОГАДРО
УДЕЛЬНАЯ
ВЕЛИЧИНА, МОЛЯРНАЯ ВЕЛИЧИНА, МОЛЯРНАЯ МАССА
ВЕЩЕСТВА, МОЛЯРНЫЙ ОБЪЕМ ВЕЩЕСТВА, ПОСТОЯННАЯ
АВОГАДРО
 1)Определите
молярные теплоемкости алюминия и кремния при 25oС,
если их удельные теплоемкости при той же
температуре равны 902,6 и 618,4 Дж/(кг.К),
соответственно.
1)Определите
молярные теплоемкости алюминия и кремния при 25oС,
если их удельные теплоемкости при той же
температуре равны 902,6 и 618,4 Дж/(кг.К),
соответственно.
2)Определите удельные теплоемкости при 25oС
воды, этилового спирта С2Н5ОН и
сульфата бария BaSO4, если их молярные
теплоемкости при той же температуре
соответственно равны 75,3; 111,4 и 102,1 Дж/(моль.К).
3)Молярная теплоемкость при 25oС ацетона C3H6O
равна 125 Дж/(моль.К), а оксида фосфора Р4О10
– 215,6 Дж/(моль.К). Порции обоих веществ
равной массы необходимо нагреть на 10o. Для
какого из веществ потребуется затратить больше
энергии?
4)Определите молярные теплоты плавления (при
температуре плавления) воды, алюминия и кремния,
если их удельные теплоты плавления
соответственно равны 890 кДж/кг (при ОoС), 400
кДж/кг (при 660oС) и 1780 кДж/кг (при 1415oС).
5)Молярные теплоты плавления при температуре
плавления у железа – 13,8 кДж/моль, а у оксида
железа Fe3O4 – 138 кДж/моль. Во сколько
раз больше энергии нужно затратить для плавления
образца Fe3O4, чем для плавления такого
же по массе образца железа?
6)Молярные теплоты кипения некоторых веществ (Lm,
в кДж/моль) приведены в таблице.
Вещество |
Lm |
Вещество |
Lm |
Вещество |
Lm |
Вещество |
Lm |
H2 |
0,9 |
Fe |
360,0 |
SiO2 |
573,6 |
Этанол |
38,7 |
O2 |
6,8 |
Ba |
139,0 |
Al2O3 |
485,7 |
Метан |
8,2 |
Cl2 |
20,4 |
Н2О |
40,7 |
FeO |
230,3 |
Ацетон |
29,1 |
Si |
356,0 |
СО |
6,0 |
BaO |
259,6 |
NaOH |
144,3 |
Al |
293,0 |
SO2 |
25,0 |
CaCl2 |
225,0 |
NaCl |
138,0 |
В каких из этих веществ при кипении рвутся
химические связи, а в каких межмолекулярные?
Определите тип строения этих веществ.
7)Расположите молекулярные вещества, найденные
вами в таблице (задача 6), в порядке возрастания
прочности межмолекулярных связей.
8)Пользуясь данными той же таблицы, определите
удельные теплоты кипения водорода, кислорода,
воды, оксида бария и железа. Можно ли по
полученным значениям сказать что-либо о типе
структуры этих веществ?
9)Определите количество вещества хлорида натрия
в образце этой соли массой 5,85 г.
10)Определите количества вещества в продажных
(килограммовых) пачках поваренной соли и сахара
(С12Н22О11). Почему эти количества
вещества так сильно отличаются друг от друга?
11)Для проведения реакции необходимо взять 2,5 моля
оксида кальция СаО. Сколько нужно отвесить этого
вещества на весах?
12)Известно, что в результате реакции
термического разложения гидроксида железа Fe(OH)2
образовалось 0,125 моль оксида железа FеО.
Определите массу образовавшегося оксида железа.
13)В результате реакции было получено 6,4 г
диоксида серы. Какова масса серы, содержащейся в
этом диоксиде? Что в данном случае означает слово
" сера" в вопросе задачи?
14)Оксид алюминия Al2O3 массой 306 г
получили из алюминия массой 162 г. Докажите, что
алюминий прореагировал полностью.
15)Из 268,8 г железа было получено 650 г трихлорида
железа. Полностью ли прореагировало железо? Если
нет, то какова масса непрореагировавшего железа?
16)В образце немолекулярного вещества массой 320 г
содержится 4 моль этого вещества. Определите
формульную массу вещества.
17)Установлено, что в образце желтого металла
массой 1,97 г количество вещества составляет 0,01
моль. Какой это металл?
18)3,5 моля вещества с простейшей формулой СН2
имеют массу 196 г. Определите молекулярную формулу
этого вещества.
19)Определите молекулярную формулу одной из
аллотропных модификаций серы, если 0,02 моль этого
вещества имеет массу 5,12 г.
20)При исследовании 6 г вещества с простейшей
формулой HPO3 было установлено, что
количество вещества в этой порции составляет 0,025
моль. Определите молекулярную формулу
исследуемого вещества.
5.6. Закон Авогадро
Уравнение связи Vm = V/n не дает
нам возможности вычислить молярный объем
конкретного вещества, так как непосредственное
измерение количества вещества практически
невозможно, а измерение объема особенно для
твердых веществ часто бывает довольно сложным и
трудоемким.
Преобразуем это уравнение. Вспомним, что
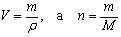 ,
,
тогда 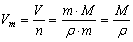 ; следовательно
; следовательно 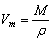
Молярную массу легко определить, плотность
тоже (ее значения приводятся во многих
справочниках).
Теперь мы легко можем посчитать молярный объем
любого вещества, например, воды (плотность воды - 1
г/см3):
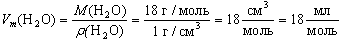 .
.
Аналогично определим молярные объемы
некоторых других веществ и внесем их в таблицу:
Вещество |
Формула |
Агрегатное
состояние |
Плотность,г/см3 |
Молярный
объем,см3/моль |
Примечание |
| Железо |
Fe |
твердое |
7,87 |
|
|
| Сера |
S8 |
твердая |
2,07 |
|
|
| Хлорид натрия |
NaCl |
твердый |
2,17 |
|
|
| Этиловый спирт |
C2H5OH |
жидкость |
0,79 |
|
|
| Кислород |
O2 |
газ |
0,00143 |
|
t = 0oC; P
 105 Па 105 Па |
| Хлор |
Cl2 |
газ |
0,00317 |
|
" |
| Диоксид углерода |
CO2 |
газ |
0,00196 |
|
" |
Мы с вами убедились, что для твердых и жидких
веществ молярные объемы имеют разные значения, а
для газов при одинаковых условиях эти значения
очень близки. Совершенно одинаковы молярные
объемы идеальных газов, то есть газов, в
которых кроме упругих соударений между
молекулами нет других видов взаимодействия.
Подробнее идеальные газы вы будете изучать в
курсе физики.
Под одинаковыми условиями понимается
одинаковая температура и одинаковое давление. Мы
с вами рассчитывали молярные объемы различных
газов в условиях, обозначенных в примечании.
Именно это сочетание давления и температуры
получило название " нормальные условия" (сокращенное
обозначение – н. у.).
Нормальные условия (для газов)
t = 0 oС, или Т = 273,15 К  273
К 273
К
P = 1 атм = 760 мм рт. ст. = 101325 Па |
При нормальных условиях
Для двух различных газов (1 и 2) количества
вещества
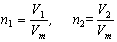 .
.
Если V1 = V2, то и n1 = n2,
а так как n = N/NA, то и N1 = N2.
Мы с вами вывели один из важнейших законов,
которым подчиняются идеальные газы (или близкие
к ним по свойствам реальные). Закон этот
называется " закон Авогадро" .
В равных объемах различных газов при
одинаковых условиях содержится одинаковое число
молекул.
Сера (ромбическая сера) – S8 ( -S8). Одно из простых
веществ, образуемых химическим элементом "
сера" . Ромбическая сера – твердое, хрупкое
негигроскопичное вещество лимонно-желтого
цвета. В воде нерастворима, но хорошо
растворяется в дисульфиде углерода и некоторых
других растворителях. При комнатной температуре
сера довольно инертна, но при нагревании активно
реагирует со многими веществами. В природе сера
встречается довольно часто. -S8). Одно из простых
веществ, образуемых химическим элементом "
сера" . Ромбическая сера – твердое, хрупкое
негигроскопичное вещество лимонно-желтого
цвета. В воде нерастворима, но хорошо
растворяется в дисульфиде углерода и некоторых
других растворителях. При комнатной температуре
сера довольно инертна, но при нагревании активно
реагирует со многими веществами. В природе сера
встречается довольно часто.
В России месторождения самородной серы имеются в
Самарской области. В промышленности более
половины добытой серы расходуется на
производство серной кислоты. Используют ее и для
производства многих других веществ, а также в
резиновой промышленности для вулканизации
каучука, в производстве красителей, в
фармацевтической промышленности, при
изготовлении спичек и средств борьбы с
вредителями сельскохозяйственных растений.
Тщательно очищенная сера применяется и в
медицине при некоторых кожных и
желудочно-кишечных заболеваниях. |
 МОЛЯРНЫЕ
ОБЪЕМЫ ТВЕРДЫХ ВЕЩЕСТВ, ЖИДКОСТЕЙ И ГАЗОВ; ЗАКОН
АВОГАДРО .
МОЛЯРНЫЕ
ОБЪЕМЫ ТВЕРДЫХ ВЕЩЕСТВ, ЖИДКОСТЕЙ И ГАЗОВ; ЗАКОН
АВОГАДРО .
 1.Какое количество вещества углекислого газа (при
н. у.) занимает объем 2,8 л?
1.Какое количество вещества углекислого газа (при
н. у.) занимает объем 2,8 л?
2.Какой объем (при н. у.) занимает а) 0,5 моль, б) 0,1
моль, в) 10 моль, г) 0,01 моль любого газа?
3.Определите массу углекислого газа, занимающего
при н. у. объем 2,8 л.
4.Определите массы следующих газов (объем газов
при н. у. указан в скобках): а) H2 (4,48 л), б) N2
(134,4 л), в) СО (6,72 л), г) Аr (336 л).
5.Определите объемы при н. у. следующих газов
(массы газов указаны в скобках): a) NH3 (40,8 г), б)
СО2 (11 г), в) SO2 (80 г), г) C2H6 (180
г).
6.Сколько молекул метана СН4 содержится в
0,112 л этого газа при н. у.?
7.Сколько атомов водорода содержится в 1 мл
водорода (при н. у.)?
8.Сколько всего атомов содержится в 1 мл метана?
Сколько из них атомов водорода? Какой объем при
нормальных условиях займет 1,26.1025
молекул аммиака NH3? Какова его масса?
9.Каково в нем количество вещества водорода? А
азота? Определите массу всего водорода,
входящего в состав этой порции аммиака.
10.В каком значении употребляется слово "
водород" в задачах 7 – 9 (в каждом из случаев)?