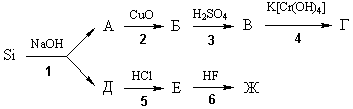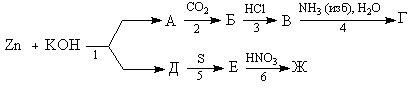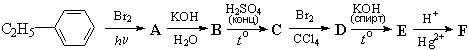Варианты экзаменационных задач по химии на вступительных экзаменах 2002 года
Химический факультет
Вариант 1
1.Сколько электронов и протонов
содержат молекула СО2 и ион [Ag(NH3)2]+?
2.Даны вещества: фенол, толуол,
фенилэтилен и 2,2,3–триметилбутан. Какие из них
будут реагировать с бромной водой? Напишите
соответствующие уравнения реакций.
3. Даны соли: (NH4)2CO3,
NaBr, KMnO4, Fe(NO3)2. Какие из них
разлагаются при прокаливании? Напишите
уравнения реакций.
4. При сгорании 5.6 г оксида углерода
выделяется 56.58 кДж теплоты, а при взаимодействии
10.8 г FeO с оксидом углерода (II) выделяется 2.13 кДж
теплоты. Рассчитайте теплоту образования оксида
железа (II).
5. Напишите уравнения реакций,
соответствующие следующей схеме превращений:
PH3  X X  Ca3(PO4)2 Ca3(PO4)2  Y Y  KH2PO2 KH2PO2
Определите неизвестные вещества.
6. В 300 г 10.8%-ного раствора хромата
натрия растворили 10 г оксида хрома (VI).
Рассчитайте массовые доли веществ в
образовавшемся растворе.
7. При взаимодействии сульфида
мышьяка (III) с избытком азотной кислоты
выделилось 7.46 л газа с плотностью 1.21 г/л (при 30° С
и давлении 1 атм) и образовался раствор массой 90 г,
в котором массовые доли азотной и серной кислот
равны. Вычислите массовую долю азотной кислоты в
исходном растворе.
8. Напишите уравнения реакций,
соответствующие следующей схеме превращений:
С10H12O2  X X  C7H8 C7H8  Y Y 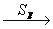 C7H5NO4 C7H5NO4 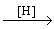 Z Z  C7H6NO2K C7H6NO2K
(Знак SEобозначает реакцию
электрофильного замещения).
В уравнениях укажите структурные
формулы веществ и условия реакций.
9. Электролиз 400 г раствора сульфата
меди (II) продолжали до тех пор, пока масса
раствора не уменьшилась на 20.5 г. Выделившийся на
аноде кислород может полностью окислить 16.8 г
металлического железа. Вычислите массовые доли
соединений в исходном растворе и в растворе,
полученном после окончания электролиза, а также
массы веществ, выделившихся на инертном катоде.
10. Ароматический углеводород с одним
бензольным кольцом содержит 90.91% углерода по
массе. При окислении 2.64 г этого углеводорода
подкисленным раствором перманганата калия
выделяется 962 мл газа (при 20° С и нормальном
давлении), а при нитровании образуется смесь,
содержащая два мононитропроизводных. Установите
возможную структуру исходного углеводорода и
напишите схемы упомянутых реакций. Сколько
мононитропроизводных образуется при нитровании
продукта окисления углеводорода?
Вариант 2
1. Напишите уравнения электролиза
водного раствора и расплава CaBr2.
2. Смесь меди и нитрата меди (II)
прокалили на воздухе. Масса смеси при этом не
изменилась. Определите массовые доли
компонентов в исходной смеси.
3. Напишите уравнения реакций (с
указанием структурных формул), соответствующие
следующей схеме превращений:
А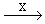 С8H4O4K2
+ 2CO3K2 + … С8H4O4K2
+ 2CO3K2 + … 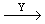 Mn Mn
Определите возможные вещества А, Х
и Y.
4. В 500 мл насыщенного раствора Zn3(PO4)2
содержится 2.47* 10–7 моль фосфат-ионов.
Вычислите растворимость соли в моль/л и
произведение растворимости Zn3(PO4)2
.
5. В разбавленной азотной кислоте
растворена навеска цинка. При нагревании
полученного раствора с избытком щелочи
выделился газ, который был использован для
полного восстановления 24 г оксида меди (II).
Определите массу цинка, растворенного в азотной
кислоте.
6. Константа скорости реакции А  В при 22°
С равна 2.4 мин–1, а при 27° С – 3.3 мин–1.
При какой температуре константа скорости
реакции будет равна 4.0 мин–1? В при 22°
С равна 2.4 мин–1, а при 27° С – 3.3 мин–1.
При какой температуре константа скорости
реакции будет равна 4.0 мин–1?
7. Напишите уравнения реакций,
соответствующие следующей схеме превращений:
Cr2O3  X X  K2CrO4 K2CrO4  Y Y  CrCl3 CrCl3  Z Z  Cr2O3 Cr2O3
Определите неизвестные вещества.
8. Напишите уравнения реакций,
соответствующие следующей схеме превращений:
С4H4O3 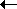 С4H6O4 С4H6O4
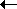 С4H8O2 С4H8O2
 С4H11O3N С4H11O3N
 С4H7O2Br С4H7O2Br
 С4H7O3Na С4H7O3Na
 С5H10O3 С5H10O3
В уравнениях укажите структурные
формулы веществ и условия реакций.
9. Известно, что 40 мл раствора,
содержащего нитрат меди (II) и серную кислоту,
могут прореагировать с 25.4 мл 16.02%-ного раствора
гидроксида натрия (плотность раствора 1.18), а
прокаливание выпавшего при этом осадка дает 1.60 г
твердого вещества. Вычислите концентрации (в
моль/л) нитрата меди (II) и серной кислоты в
исходном растворе, а также объем газа (при н.у.),
который выделяется при внесении 2.5 г
порошкообразной меди в 40 мл этого раствора.
10. Смесь двух эфиров, образованных
метиловым спиртом и одноосновными карбоновыми
кислотами, массой 53.6 г нагрели с 367 мл 8%-ного
раствора гидроксида натрия (плотность 1.09 г/мл), а
затем через полученный раствор пропустили ток
углекислого газа до прекращения увеличения
массы раствора. Объем поглощенного углекислого
газа, измеренный при 25° С и давлении 101.325 кПа,
составил 7.34 л. Назовите исходные сложные эфиры,
если мольные доли элементов в них составляют: С –
28.6%, Н – 57.1%, О – 14.3% и С – 44.4%, Н – 44.4%, О – 11.1%.
Определите массовые доли солей в образовавшемся
растворе.
Биологический факультет
Вариант 1
1. Напишите структурные формулы двух
изомерных пептидов и назовите их.
2. Константы равновесий A 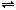 B и A B и A 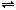 C равны, соответственно, K1
и K2. Найдите константу равновесия B C равны, соответственно, K1
и K2. Найдите константу равновесия B 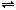 C. C.
3. В трех пробирках находятся водные
растворы хлорида аммония, сульфида натрия и
хлорида меди (II). Как можно распознать, где какое
вещество находится? Опишите процедуру
идентификации и напишите уравнения используемых
реакций.
4. Установите формулу газа, который
тяжелее газовой смеси, полученной при разложении
нитрата серебра, но легче смеси, полученной при
разложении нитрата меди (II). Ответ подтвердите
расчетом.
5. Напишите уравнения химических
реакций, соответствующие следующей схеме
превращений:
глюкоза  X X  Y. Y.
Молекула вещества Y имеет такой же
массовый элементный состав, что и молекула
глюкозы, но содержит на 4 атома кислорода меньше.
6. Напишите уравнения следующих
реакций:
а) FeCl2 + Br2 + KOH  ... ...
б) FeCl3 + KCN(изб, р-р)  … …
в) S + KOH (конц)  … …
7. Известны тепловые эффекты
следующих реакций:
C2H2(г)  2C(графит) + H2(г), Q
= 226.7 кДж; 2C(графит) + H2(г), Q
= 226.7 кДж;
3C2H2(г)  C6H6(ж), Q = 631.1
кДж; C6H6(ж), Q = 631.1
кДж;
C6H6(ж)  C6H6(г), Q = –33.9
кДж/моль. C6H6(г), Q = –33.9
кДж/моль.
Рассчитайте теплоту образования
газообразного бензола из графита и водорода.
8. Напишите уравнения химических
реакций, соответствующие следующей схеме
превращений:
C9H12  C3H6O C3H6O C3H6Cl2 C3H6Cl2  C3H4 C3H4 C9H12 C9H12 C9H6O6 C9H6O6 C9H15N3O6 C9H15N3O6
В уравнениях укажите структурные
формулы веществ и условия протекания реакций.
9. Порошок железа массой 12.6 г
растворили в 200 мл 4 М соляной кислоты, и
полученный раствор оставили на воздухе. Через
некоторое время к раствору добавили 10%-ный
раствор гидроксида калия до полного выпадения
осадка, который отфильтровали и нагревали до
постоянной массы в инертной атмосфере. Масса
сухого остатка оказалась равной 17.2 г. Определите
состав сухого остатка (в мольных %). Напишите
уравнения проведенных реакций.
10. При полном гидролизе смеси двух
изомерных нуклеозидов получен образец смеси
углеводов, который при сжигании образует 224 мл
углекислого газа (н.у.). Такой же образец смеси
углеводов способен прореагировать с 0.910 г
пропионового ангидрида. Установите структурные
формулы нуклеозидов и их молярное соотношение в
смеси.
Вариант 2
1. Напишите структурные формулы
двух изомерных углеводов и назовите их.
2. Константы равновесий A 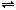 B и B B и B 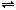 C равны, соответственно, K1
и K2. Найдите константу равновесия C C равны, соответственно, K1
и K2. Найдите константу равновесия C 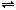 A. A.
3. В трех пробирках находятся водные
растворы нитрата серебра, гидрокарбоната натрия
и хлорида железа (III). Как можно распознать, где
какое вещество находится? Опишите процедуру
идентификации и напишите уравнения используемых
реакций.
4. Установите формулу газа, который
тяжелее газовой смеси, полученной при разложении
бромида аммония, но легче смеси, полученной при
окислении углерода концентрированной серной
кислотой. Ответ подтвердите расчетом.
5. Напишите уравнения химических
реакций, соответствующие следующей схеме
превращений:
диметилкетон  X X  Y. Y.
Молекула вещества Y имеет такой же
массовый элементный состав, что и молекула
диметилкетона, но содержит на 6 атомов водорода
больше.
6. Напишите уравнения следующих
реакций:
а) FeSO4 + Cl2 + KOH  … …
б) FeSO4 + KCN(изб, р-р)  … …
|
to |
в) Cl2 + Ba(OH)2
|
 ... ...
|
7. Известны тепловые эффекты
следующих реакций:
6C(графит) + 3H2(г)  C6H6(г), Q
= –82.9 кДж; C6H6(г), Q
= –82.9 кДж;
3C2H2(г)  C6H6(ж), Q = 631.1
кДж; C6H6(ж), Q = 631.1
кДж;
C6H6(ж)  C6H6(г), Q = –33.9
кДж/моль. C6H6(г), Q = –33.9
кДж/моль.
Рассчитайте теплоту образования
ацетилена из графита и водорода.
8. Напишите уравнения химических
реакций, соответствующие следующей схеме
превращений:
C7H6OCl2  C7H6O2 C7H6O2
 C7H8O2 C7H8O2
 C9H10O3 C9H10O3
 C9H8O3Br2 C9H8O3Br2
 C7H5O2Br2Na C7H5O2Br2Na
 C7H5OBr3 C7H5OBr3
В уравнениях укажите структурные
формулы веществ и условия протекания реакций.
9. Порошок железа массой 19.6 г
растворили в 400 мл 2 М серной кислоты, и полученный
раствор оставили на воздухе. Через некоторое
время к раствору добавили 10%-ный раствор
гидроксида калия до полного выпадения осадка,
который отфильтровали и нагревали до постоянной
массы в инертной атмосфере. Масса сухого остатка
оказалась равной 26.8 г. Определите состав сухого
остатка (в мольных %). Напишите уравнения
проведенных реакций.
10. При полном гидролизе смеси двух
изомерных нуклеозидов получен образец смеси
углеводов, который при сжигании образует 336 мл
(н.у.) углекислого газа. Такой же образец смеси
углеводов способен прореагировать с 1.30 г
пропионового ангидрида. Установите структурные
формулы нуклеозидов и их молярное соотношение в
смеси.
Вариант 3
1. Напишите структурные формулы двух
изомерных карбонильных соединений и назовите их.
2. При столкновении ядер никеля-62 и
свинца-208 выделяется нейтрон и образуется ядро
нового элемента. Определите массовое число и
заряд этого ядра.
3. Напишите уравнения полуреакций и
суммарное уравнение электролиза водного
раствора: а) сульфата меди; б) хлорида кальция.
4. Константа скорости реакции изомеризации A
 B равна 20 с–1, а константа скорости
обратной реакции B B равна 20 с–1, а константа скорости
обратной реакции B  A равна 12 с–1. Рассчитайте состав равновесной
смеси (в граммах), полученной из 10 г вещества A.
A равна 12 с–1. Рассчитайте состав равновесной
смеси (в граммах), полученной из 10 г вещества A.
5. Какой объем углекислого газа (н.у.)
надо пропустить через 200 г 0.74%-ного раствора
гидроксида кальция, чтобы масса выпавшего осадка
составила 1.5 г, а раствор над осадком не давал
окраски с фенолфталеином?
6. Какие два вещества вступили в
реакцию и при каких условиях, если в результате
образовались следующие вещества (указаны все
продукты реакции без стехиометрических
коэффициентов):
а) AgBr + C2H2;
б) C2H5OH + Mg(OH)Cl;
в) C2H5SO4Na ?
Напишите полные уравнения реакций.
7. Напишите уравнения химических
реакций, соответствующие следующей схеме
превращений. Определите неизвестные вещества А
– Ж.
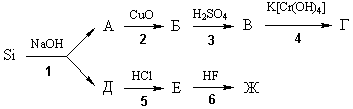
8. Дана схема превращений:
C7H16  C7H8 C7H8  C7H7O2N C7H7O2N  C7H5O4N C7H5O4N
 C6H5O2N C6H5O2N
 C6H7N C6H7N
 C6H9O4NS. C6H9O4NS.
Напишите структурные формулы
указанных веществ и уравнения соответствующих
реакций. Укажите условия проведения реакций.
9. Смесь гидроксидов хрома (II) и (III)
общей массой 2.92 г растворили в избытке соляной
кислоты. К полученному раствору добавили избыток
щелочи и получили осадок массой 0.86 г. Через
фильтрат пропускали углекислый газ до
прекращения выделения осадка. Найдите массу
второго осадка. Напишите уравнения реакций (все
опыты проводили в инертной атмосфере).
10. При полном гидролизе 49.50 г
олигосахарида образовался только один продукт –
глюкоза, при спиртовом брожении которой получено
22.08 г этанола. Установите число остатков глюкозы
в молекуле олигосахарида и рассчитайте массу
воды, необходимой для гидролиза, если выход
реакции брожения – 80%.
Факультет фундаментальной
медицины
Вариант 1
1. Укажите число протонов, электронов и
электронную конфигурацию атома циркония.
2. Напишите уравнения полуреакций и
суммарное уравнение электролиза водного
раствора: а) серной кислоты, б) ацетата лития.
3. Две реакции протекают с одинаковой
скоростью (w1 = w2) при 20 оС,
температурный коэффициент скорости первой
реакции равен 6, второй – 3. Как будут относиться
скорости реакций w2 / w1, если
реакции проводить при 60 оС?
4. Лекарственный препарат норадреналин
имеет следующее строение:
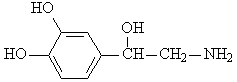
Приведите три уравнения реакций,
характеризующие свойства норадреналина, и
структурную формулу одного межклассового
изомера этого вещества.
5. Допишите в уравнения реакций
формулы соединений Х и Y (коэффициенты при
реагентах и продуктах реакции уже указаны).
а) CH3COOH + X1 = H2O + Y1;
б) CH3Cl + X2 = NaCl + Y2;
в) KOH + X3 = C2H6 + Y3;
г) C2H5OH + X4 = HCl + Y4.
6. Константа диссоциации уксусной
кислоты равна 1.75? 10–5. Вычислите: а) рН 0.1 М
раствора этой кислоты; б) рН раствора,
содержащего 0.1 моль/л этой кислоты и 0.1 моль/л
ацетата натрия.
7. Напишите уравнения химических
реакций, соответствующих следующей схеме
превращений. Определите неизвестные вещества А
– Ж. Укажите условия реакций.
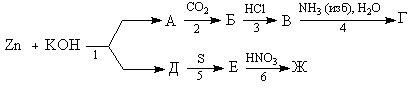
8. При сгорании 11.0 г пропана
выделилось 555 кДж теплоты. При сгорании 11.5 г смеси
пентана и гексана выделилось 564 кДж теплоты.
Каково молярное соотношение пентана и гексана в
смеси, если известно, что в гомологическом ряду
алканов теплота сгорания увеличивается на 660 кДж
на каждый моль СН2-групп?
9. Сплавили 22.4 г смеси натриевой соли
карбоновой кислоты и гидроксида натрия,
содержащей избыток щелочи. Полученное твердое
вещество снова подвергли плавлению с 20.4 г оксида
алюминия. Объем выделившегося при этом газа
составил
2.4 л (при 20 оС). Твердый остаток промыли
избытком воды. Масса нерастворившегося вещества
составила 5.1 г. Установите молекулярную формулу и
массу полученного в первой реакции
органического соединения.
10. При полном гидролизе пентапептида
Met-энкефалина были получены следующие
аминокислоты: Gly – H2NCH2COOH, Phe – H2NCH(CH2C6H5)COOH,
Tyr – H2NCH(CH2C6H4OH)COOH, Met – H2NCH(CH2CH2SCH3)COOH.
Из продуктов частичного гидролиза этого же
пептида были выделены вещества с молекулярными
массами 295, 279 и 296. Установите две возможные
последовательности аминокислот в данном пептиде
(в сокращенных обозначениях) и рассчитайте его
молярную массу.
Факультет биоинженерии и
биоинформатики
Вариант 1
1. От каких факторов зависит
положение химического равновесия? Приведите по
одному конкретному примеру для каждого фактора.
2. Во сколько раз уменьшается масса
твердого вещества при полном разложении
дихромата аммония?
3. Приведите примеры молекул, в
которых в состоянии sp-гибридизации
находятся: а) два атома углерода; б) три атома
углерода; в) один атом углерода.
4. В вашем распоряжении имеются
водные растворы сульфита калия, перманганата
калия и бромоводорода. Напишите уравнения всех
возможных реакций, протекающих попарно между
указанными веществами.
5. Определите формулу
кристаллогидрата перхлората магния, содержащего
67.67% кислорода по массе.
6. При некоторой температуре
молярная масса дихлоруксусной кислоты в парах
составляет 220 г/моль. Сколько молекул димера
кислоты приходится на одну молекулу мономера в
этих условиях?
7. Напишите уравнения реакций,
соответствующие следующей последовательности
превращений:
|
HCl |
|
HNO3 |
|
Na2CO3*H2O |
|
| Cr |
 |
X1 |
 |
X2
|

| X3
|
Определите неизвестные вещества.
8. Напишите уравнения реакций,
соответствующие следующей схеме:
|
KMnO4, H+
|
|
Al, NaOH
|
|
2C2H5Br
|
|
C9H11NO2
|

|
C8H5NO6
|

|
C8H5Na2NO4
|

|
C12H15NO4
|
В уравнениях укажите структурные
формулы веществ и условия реакций.
9. При действии избытка углекислого
газа на 19.8 г неизвестного соединения металла с
кислородом образовалось твердое вещество А и
выделился газ B. Вещество А растворили в
воде и добавили избыток раствора нитрата бария,
при этом выпало 11.82 г осадка. Газ В пропустили
через трубку с раскаленной медью, и масса трубки
увеличилась на 2.88 г. Установите формулы
исходного соединения и веществ А и В.
10. Фермент рибонуклеаза
катализирует гидролиз РНК по фосфодиэфирным
связям. Его полипетидная цепь состоит из 124
аминокислотных остатков. Из продуктов полного
гидролиза 100.0 г этого фермента было выделено 1.642 г
глицина NH2CH2COOH, 7.066 г цистеина HSCH2CH(NH2)COOH
и 4.350 г метионина СH3S(CH2)2CH(NH2)COOH.
Определите молярную массу рибонуклеазы и
рассчитайте массовую долю серы в этом ферменте.
Факультет почвоведения
Вариант 1
1. Определите относительную
молекулярную массу простого вещества Х, одна
молекула которого весит 6.64 · 10-23 г.
2. Каким ионам могут соответствовать
электронные конфигурации а) элемента Не и
б) иона Са2+?
3. Две различные реакции протекают с
выделением углекислого газа. За одну минуту в
реакции А образуется 3.36 л СО2 (н.у.), а в
реакции Б 66 г СО2. Найдите соотношение
скоростей реакций Б : A.
4. При прохождении воздуха через
озонатор 50% кислорода превратилось в озон.
Определите плотность полученной газовой смеси
по азоту. Состав воздуха:
N2 – 79%, O2 – 21% (по объему).
5. Напишите уравнения химических
реакций, соответствующие следующей схеме
превращений:
HCl  Cl2 Cl2  KClO3 KClO3  KCl KCl  K2SO4 K2SO4  KNO3 KNO3  O2. O2.
Укажите условия проведения реакций.
6. Напишите уравнения следующих
реакций и укажите условия их протекания:
MnO2 + KI + H2SO4 
(NH4)2HPO4 + Ca(OH)2 
7. Продукты сгорания смеси серы и
фосфора массой 7.15 г в избытке кислорода
растворили в 100 мл воды. На полную нейтрализацию
полученного раствора пошло 81.63 мл раствора
гидроксида натрия с массовой долей щелочи 20% и
плотностью 1.225 г/мл. Определите массовые доли
веществ в исходной смеси.
8. Напишите уравнения химических
реакций, соответствующие следующей цепочке
превращений:
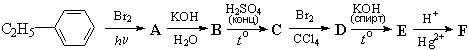
9. После пропускания над раскаленным
углем без доступа воздуха смеси оксида углерода
(II) и оксида углерода (IV) с плотностью по водороду
18.8 объем газовой смеси увеличился на 20% и
составил 26.88 л (н.у.). Полученную газовую смесь
пропустили через раствор гидроксида кальция, при
этом выпало 40 г осадка. Определите объемное
соотношение газов в исходной смеси и объем
оставшегося газа.
10. При полном сгорании раствора
нитробензола и анилина в этиловом спирте с
массовой долей нитробензола 37.16 % выделилось
2.24 л азота (н.у.). Тепловой эффект реакции составил
991.2 кДж. Определите массу исходного раствора,
если известно, что теплоты сгорания
нитробензола, анилина и этанола равны
соответственно 3094.88, 3392.15 и 1370 кДж/моль.
|