|
Школьные олимпиады по химии
Всероссийская олимпиада школьников по химии - 2004 года
Всероссийская олимпиада школьников по химии - 2004 г.
ОДИННАДЦАТЫЙ КЛАСС
Задача 11-1.
Ниже приведена схема превращения некоторых
органических соединений:
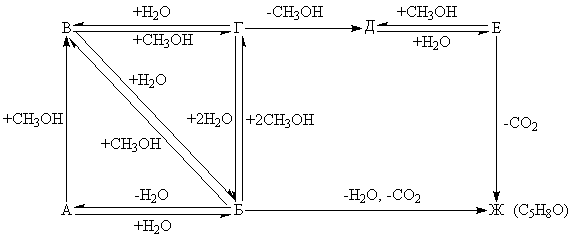
Известно, что в спектре протонного магнитного
резонанса (ПМР) соединения Ж имеются три
мультиплетных сигнала, обусловленных
расщеплением сигнала на атомах водорода у
соседних атомов углерода. Кроме того, известно,
что соединение А имеет похожий спектр ПМР, в
котором также три сигнала такой же
мультиплетности, отличающиеся лишь по величинам
химических сдвигов.
- Приведите структурные формулы соединений А
- Ж и их названия в соответствии с
номенклатурой IUPAC. Ответ мотивируйте.
- Какие из соединений А - Г могут
существовать в виде двух изомеров?
- Приведите механизм превращения соединения Г
в соединение Д.
- Нарисуйте наиболее вероятную пространственную
структуру соединения Д. Ответ мотивируйте.
Задача 11-2.
Восстановление нафталина в зависимости от
используемых реагентов и условий реакции
приводит к образованию различных продуктов. В
лабораторных условиях широкое распространение
получило восстановление металлами в аммиаке или
органических аминах. При восстановлении натрием
или литием в смеси жидкий аммиак - диэтиловый
эфир при -78оС с выходом 98% образуется
соединение А, содержащее до 1% соединения В и
следы соединения С. Если восстановление
проводить в присутствии избытка натрия или лития
также в смеси жидкий аммиак - диэтиловый эфир, но
затем добавить к реакционной смеси хлорид железа
(III) и температуру повысить до -330С, то почти
с количественным выходом образуется только
соединение В; в этих же условиях, но в
отсутствии хлорида железа (III) также с
количественным выходом образуется только
соединение С. При кипячении с этилатом натрия
в этаноле А изомеризуется в В.
При восстановлении нафталина или соединения С литием
в низших алифатических аминах (этиламин,
диаминоэтан) образуется смесь двух изомерных
веществ D и Е. При добавлении натрия к
раствору нафталина в смеси аммиак - спирт -
диэтиловый эфир при
-78оС получается соединение F, являющееся
изомером С.
Известно, что А, В и С при кипячении с
перманганатом калия в кислой среде образуют одну
и ту же ароматическую кислоту. При окислении D
в тех же условиях образуется циклический дикетон
G, а при окислении E - кетокислота Н. В
ПМР-спектре соединения F имеется всего 2
сигнала.
- Изобразите структурные формулы веществ А-Н.
- Для характеристики жидких ненасыщенных
углеводородов часто используют их реакцию с
нитрозилхлоридом, приводящую к образованию
кристаллических аддуктов. Иногда эти аддукты
могут существовать в двух таутомерных формах.
Напишите реакцию смеси изомеров D и Е с
нитрозилхлоридом. Если продукты реакции могут
существовать в таутомерной форме, напишите обе
формы; если не могут, объясните - почему
существует только одна форма.
- В отличие от А, соединение В может далее
восстанавливаться натрием в спирте. Почему это
возможно?
Задача 11-3.
Основным методом промышленного производства
соединения А является его получение в
процессе комплексной переработки нефелинов.
Однако, существует еще несколько промышленных
способов:
а) Магнезиальный способ основывается на
процессе карбонизации под давлением 0,5-1,8 МПа
суспензии активной магнезии (Б) в водном
растворе хлорида калия (1). Осаждаемую двойную
соль Энгеля (В) отделяют от раствора хлорида
магния и разлагают водой (2) или суспензией
гидроксида магния (3) при нагревании. Полученная
суспензия фильтруется. Активная магнезия
возвращается в процесс, а раствор упаривается и
из концентрированных растворов выделяют
кристаллы, которые после сушки упаковывают в
виде товарного продукта.
б) В триметиламиновом методе карбонизации под
давлением подвергается смесь растворов хлорида
калия и триметиламина (4). В процессе охлаждения
полученного раствора выделяются кристаллы (Г),
которые легко могут быть переведены в целевой
продукт (5). Остающееся при этом в растворе
соединение (Д) после соответствующей
обработки (6) возвращается в голову процесса.
в) Формиатный способ сводится к обработке
сульфата калия суспензией гидроксида кальция
под давлением окиси углерода (7). Отфильтрованный
раствор упаривают, а остаток прогревают при 800 оС
во вращающейся барабанной печи (8), после чего
перекристаллизовывают из воды или предыдущих
маточных растворов.
г) Известен процесс, в котором смесь сульфата
калия нагревают с углем и известняком (9), а из
образующегося плава маточными растворами
выщелачивают продукт.
1. О производстве какого продукта идет речь?
Рассчитайте точный состав самого продукта,
активной магнезии и двойной соли Энгеля. В Вашем
распоряжении имеются следующие данные по их
термолизу: при нагревании соединений А и В
до 200 оС они теряют 16,36 и 40,19 % массы
соответственно, причем 10,00 г В выделяют 7561 мл
газообразных продуктов (t=200 oC, p=1 атм). При
нагревании Б и В от 20 до 700 оС потеря
массы составляет, соответственно, 70,88 и 57,36 %.
2. Напишите уравнения реакций 1-4. Предложите
рациональные способы переработки Г и Д
(процессы 5 и 6).
3. Напишите уравнения реакций 7-9. С какой целью
процесс 8 проводят во вращающейся барабанной
печи? Что произойдет, если ее заменить обычной
печью?
4. Способы б) и г) имеют прототипами известные с 1860
и 1790 гг процессы Сольве и Леблана. Чем они
отличаются от описанных способов?
5. При комплексной переработке нефелинов, после
их спекания с известняком, получают, кроме А,
еще 3 ценных промышленных продукта. Какие
химические элементы составляют основу нефелинов
и какие товарные продукты получают в финале их
переработки?
Задача 11-4.
Полимеры, содержащие аминогруппы в боковых
цепях, часто находят практическое применение в
качестве ионообменных смол, препаратов для
очистки воды, отбеливателей в
целлюлозно-бумажной промышленности. В 2003 году
группа американских ученых сообщила о синтезе
«супераминированного» полимера -
полиметиленамина. В качестве исходного сырья для
получения полимера был использован 1,3-дигидро-2H-имидазол-2-он,
подвергавшийся следующим химическим
превращениям:
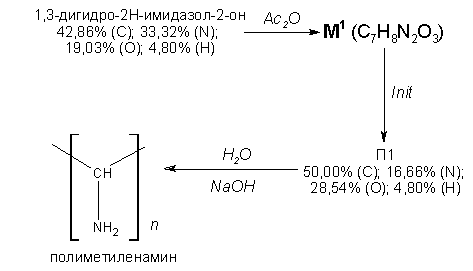
На схеме использованы следующие обозначения: Ас2О
- уксусный ангидрид, Init - инициатор реакции -
[1,1’-азобис(1-цианоциклогексан)], М1 -
мономер, получающийся при ацилировании
1,3-дигидро-2H-имидазол-2-она, П1 - полимер,
модификация которого приводит к образованию
полиметиленамина.
- Запишите структурные формулы 1,3-дигидро-2H-имидазол-2-она,
уксусного ангидрида, 1,1’-азобис(1-цианоциклогексана), мономера М1,
и полимера П1.
- Запишите уравнения процессов, протекающих при
получении полиметиленамина, включая стадию
распада инициатора - 1,1’-азобис(1-цианоциклогексана).
- Какой процесс инициируется в результате
распада 1,1’-азобис(1-цианоциклогексана)?
- Определите среднюю степень полимеризации
полимера П1 и среднюю молекулярную массу
полиметиленамина, полученного в описываемом
эксперименте, учитывая нижеследующие данные.
Авторы методики получения полиметиленамина
определили среднюю молекулярную массу полимера
П1. Она равна 104000. Провести прямое измерение
средней молекулярной массы полиметиленамина не
удалось, однако, авторы считают, что в процессе
гидролиза полимера П1 деструкция главной
цепи не происходит.
Задача 11-5.
Пиролиз гексафторацетона в зависимости от
температуры протекает по одному из двух
направлений (JournalChemicalSociety, 1961, p. 1388). Ниже 800К в
результате реакции образуются преимущественно
продукты A и B, а при температуре выше 900К
механизм реакции меняется, и основным продуктом
разложения CF3C(O)CF3 являются вещества С
и D.
Ниже приведены значения константы скорости
пиролиза k двух индивидуальных реакций,
соответствующих двум температурным интервалам.
| T, K |
750 |
775 |
800 |
925 |
950 |
975 |
| k, c-1 |
6,3*10-6 |
1,8*10-5 |
5,0*10-5 |
7,9*10-3 |
2,5*10-2 |
7,9*10-2 |
Известно, что Aвосстанавливает I2O5,
B и C имеют одинаковый качественный
состав, однако Dвозд(B) в 1,38 раз превышает Dвозд(С),
а D легко гидролизуется, образуя при этом
кислый раствор.
- Какой порядок имеет реакция разложения (CF3)2CO?
- Используя зависимость k(T) в форме уравнения
Аррениуса, рассчитайте энергию активации Еа и
значение предэкспоненциального множителя Ао
для Т<850К и Т>900К
k=Aоe-Ea/RT
- Определите вещества A-D и напишите
уравнения обоих процессов разложения.
- Приведите пример одного соединения F,
которое при термическом разложении образует
продукт С. Напишите уравнение реакции.
Задача 11-6.
Энергетика гликолиза
Один из биохимических путей переноса энергии в
живых организмах включает гликолиз - расщепление
глюкозы до более простых веществ. Этот процесс
начинается с фосфорилирования глюкозы
аденозинтрифосфатом (АТФ) и изомеризации
образующегося сложного эфира:
| |
|
DG°,кДж/моль |
| 1 |
Глюкоза + АТФ4-®
глюкозо-6-Ф2- + АДФ3- + Н+ |
+ 16.3 |
| 2 |
глюкозо-6-Ф2-®
фруктозо-6-Ф2- |
+ 1.7 |
1. Изобразите структуру иона глюкозо-6-Ф2- в проекции Хеуорса для b-формы.
2. В биохимии используют стандартное значение
энергии Гиббса (обозначается DG°'), которое соответствует pH = 7 и
стандартной концентрации 1 моль/л для остальных
участников реакции. Рассчитайте DG°' для приведенных выше двух реакций.
Энергетика биохимических реакций сильно
зависит от концентрации реагентов и продуктов.
Предположим, что в клетке созданы следующие
концентрации веществ: с(АДФ3-) = с(АТФ4-)
= 100 мкмоль/л, с(глюкоза) = 500 мкмоль/л, с(глюкозо-6-Ф2-)
= 5000 мкмоль/л.
3.При каком минимальном значении pH реакция
фосфорилирования глюкозы станет
термодинамически возможной?
4. Определите константу равновесия между
фосфатами глюкозы и фруктозы и найдите
процентное содержание фруктозо-6-фосфата в
равновесной смеси. Объясните, зависит ли это
содержание от исходной концентрации фосфатов.
5. При молочнокислом брожении суммарное
уравнение гликолиза имеет вид:
C6H12O6 + 2АДФ3- + 2HPO42-
+ 2H+ = 2CH3CH(OH)COOH + 2АТФ4- + 2H2O
Используя закон Гесса, рассчитайте изменение
энергии Гиббса в этой реакции при стандартных
концентрациях глюкозы и молочной кислоты, pH =7 и
концентрации остальных ионов 100 мкмоль/л.
Известно, что для гидролиза АТФ
АТФ4- + H2O ®
АДФ3- + HPO42- + H+
стандартная биохимическая энергия Гиббса: DG°' = -30.5 кДж/моль.
Необходимая информация.
1) Температура 298 К.
2) Зависимость энергии Гиббса вещества или иона
от концентрации:
G = Gо + RT ln c
где G0 - стандартное значение при концентрации 1 моль/л.
3) Связь между константой равновесия и
стандартным изменением энергии Гиббса в реакции:
DGо = -RT ln K .
4) Стандартные энергии Гиббса образования в
растворе:
DGо(C6H12O6)
= -910 кДж/моль,
DGо(C3H6O3)
= -518 кДж/моль.
|


