 |

|
|
LXII Московская городская олимпиада школьников по химии
Задания 11 класса
11-1. На
нейтрализацию водного раствора, образовавшегося при гидролизе 1,000 г
некоторого ангидрида А, было израсходовано 20,41 мл одномолярного раствора NaOH. Определите брутто-формулу
органического соединения А и предложите его возможное строение.
11-2. Сплав нейзильбер применяется для изготовления
деталей приборов и медицинских инструментов. Он состоит из трех металлов: Cu
(65%), Zn (20%) и металла Х(15%).
Образец сплава 1,000 г растворили в избытке разбавленной азотной кислоты и
получили ярко окрашенный раствор. Добавление избытка NaOH к полученному
раствору привело к образованию осадка, который после прокаливания имел массу
1,005 г. Установите металл Х; ответ
подтвердите расчетами. Напишите уравнения упомянутых в задаче реакций.
11-3. Разбирая реактивы на полках лаборант наткнулся на большую
банку с белыми кристаллами. Фирменная этикетка почти стерлась и можно было
прочесть только молярную массу 181,09 г/моль и часть названия вещества: "L-2-ам::3-(пара-:)-про:..овая:.". Помимо этикетки,
на банке также красовалась трехбуквенная надпись фломастером. Проведенный
элементный анализ показал, что кроме углерода и водорода вещество содержит 7,73
% азота и 26,52% кислорода. Попробуйте по имеющимся данным восстановить
брутто-формулу, а затем и структуру этого соединения. Обоснуйте свой выбор.
Какое тривиальное название имеет это соединение? Какие три буквы были написаны
на банке и что они означают?
11-4. Реакция тетрамеризации M в М4 протекает через три последовательные стадии:
M + MRM2
M2 + MRM3
M3 + MRM4
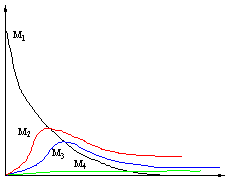
Не производя расчетов, постройте на одном графике зависимость количества M, M2, M3 и M4 от времени. Дайте краткое
объяснение предложенным вами временным зависимостям. При построении графика
считайте, что скорости всех трех реакций линейно зависят от концентрации
реагентов, а константы скоростей - одинаковы.
11-5. В лаборатории имелся водный раствор нитрата ртути (II), концентрация которого
равна 3% или 7% по массе. Для уточнения концентрации, к 325 г этого раствора
добавили 2,43 г магниевой стружки. После окончания реакции раствор отделили, а
осадок прокалили в токе инертного газа (до полного удаления паров ртути) и
взвесили. Его масса оказалась вдвое меньше первоначальной массы магния.
Рассчитайте концентрацию исходного раствора нитрата ртути и напишите уравнения
реакций.
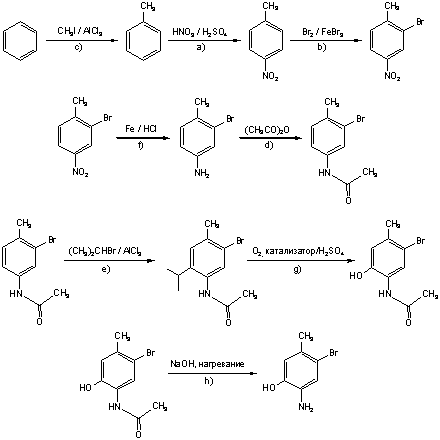
11-6. Для получения 2-амино-4-бром-5-метилфенола из бензола
могут быть использованы следующие реагенты:
а) HNO3/H2SO4; b) Br2/FeBr3; c) CH3I/AlCl3; d) (CH3CO)2O; e) (CH3)2CHBr/AlCl3; f) Fe/HCl; g) O2, катализатор/H2SO4; h) NaOH, нагревание.
Учитывая правила ориентации электрофильного замещения, расставьте реагенты в
порядке необходимом для успешного осуществления синтеза. Можно ли используя те
же реагенты в другом порядке получить 4-амино-2-бром-5-метилфенол? Напишите
уравнения реакций. В каждом из синтезов нельзя дважды использовать один и тот
же реагент.
Решения
Любая
сложная задача
имеет
простое, красивое, очевидное,
неправильное
решение.
"Cites from Gaussian 98"
- Нейтрализация органического ангидрида протекает по следующему
уравнению:
R-COOOC-R’ + 2NaOH
= R-COONa + R’-COONa + H2O
Отметим, что в
большинстве случаев (в школьной программе и на практике) R= R’, но это не
обязательно. Из уравнения найдем молярную массу ангидрида A:
M(А) =
1,000/(0,02041/2) = 98 г/моль.
После вычитания молярной массы фрагмента COOOC остается:
M(R+ R’) = 26, что
может соответствовать либо R= H
и R’ =
CCH, либо
фрагменту 1,2-замещенного этилена (R, R’) = CH=CH. Таким образом, А – либо смешанный
ангидрид муравьиной и ацетиленкарбоновой кислоты, либо ангидрид малеиновой
кислоты.
- После
добавления NaOH к
раствору сплава в избытке азотной кислоты происходит выпадение гидрооксида
Cu(OH)2
и, возможно, X(OH)2n, в то время как Zn(OH)2 в избытке щелочи растворяется
образуя Na2[Zn(OH)4].
После прокаливания в остатке присутствуют CuOи XOn. Произведем расчет массы XOn:
m(XOn) = 1,005
– (1,000*0,6500/63,55)*(63,55+16,00) = 0,1913 г
Поскольку мы знаем, что в образце исходного сплава содержалось 0,1500 г
металла X (15,00%),
можно составить уравнение для нахождения молярной массы металла M(X) при
фиксированных значениях n
(валентности):
(0,1500/M(X))*(M(X)+n*16,00) =
0,1913
Откуда:
0,01721*M(X) = n
и перебором n, находим
при n = 1, M(X) = 58,11 г/моль. Наиболее близко подходит
металл Ni. В
качестве ответа принимался также Co. В этой
задаче было важно учитывать количество значащих цифр в исходном условии и
промежуточных расчетах.
- Сначала найдем брутто-формулу
исследуемого вещества. По молярной массе и данным элементного анализа
можно установить, что вещество содержит:
181,09*0,7730/14,00 = 1 атом азота, и
181,09*0,2652/16,00 = 3 атома кислорода
Оставшаяся молекулярная масса 181,09 – 1*14,00 – 3*16,00 = 119,09 г/моль
приходится, по-видимому, на углерод и водород в формуле CxHyNO3. Составляя уравнение:
12,01*x
+ 1,00*y
= 119,09
находим единственное возможное при целых x и у решение: x = 9, y = 11 (другие решения противоречат
также химическому смыслу). Таким образом формула брутто-вещества C9H11NO3. По остаткам названия разумно
предположить, что исследуемое соединение содержит в структуре: амино-группу
("ам.."), карбоновую кислоту (причем, вероятно, пропионовую –
"про...овая"), пара-замещенное
бензольное ядро ("пара-..") и
ассиметрический атом углерода ("L-.."). Комбинируя эти фрагменты мы получаем формулу L-2-амино-3-(пара-гидроксифенил)-пропионовой кислоты. Тривиальное название
этой аминокислоты – тирозин. Сокращенное обозначение по стандартной
биохимической номенклатуре Tyr – было написано на банке
фломастером (в качестве ответа принималась также надпись "чда").
- Общее
уравнение скорости реакции, линейно зависящей от концентрации реагентов:
v = k*[A]*[B]
Вещество М расходуется во всех реакциях, но скорость его исчезновения
падает с уменьшением его концентрации, поэтому убывание М происходит по
кривой близкой к гиперболе. Концентрация вещества М2 вначале
быстро возрастает, но затем падает из-за дальнейшего превращения в M3.
Аналогично ведет себя концентрация М3, однако ее максимум
смещен относительно М2. Вещество М4 медленно накапливается в
реакционной смеси. В переделе, концентрация веществ M2, M3 и М4
выходит на плато, в тот момент когда заканчивается вещество М1.Суммарный
график схематично выглядит так:
- Реакция
нитрата ртути (II) с
магнием протекает по уравнению:
Hg(NO3)2
+ Mg = Mg(NO3)2
+ Hg
Таким образом после удаления раствора и паров ртути в остатке должен был
находиться избыток магния. Рассчитаем концентрацию исходного раствора по
этим данным:
с(Hg(NO3)2)
= ((2,43 – 2,43/2)/24,3)*(200,6 + (14,0+3*16,0)*2)/325 = 0,05 = 5%
Это не согласуется с исходными данными, и следовательно в смеси происходит
еще одна реакция. Эта реакция и является ключом к ответу на задачу. В
результате взаимодействия избытка магния в выделившейся ртути, образуется
амальгама магния, которая реагирует с водой. Следовательно в осадке
остается не магний, а его оксид. Концентрация исходного раствора в этом
случае будет равна:
с(Hg(NO3)2)
= ((2,43/24,3 – ((2,43/(24,3 + 16,0))/2)*(200,6 + (14,0+3*16,0)*2)/325 =
0,07 = 7%
- Возможный порядок реагентов приведен
ниже. Следует отметить, что он достаточно условен и построен в рамках формальных
законов ориентации электрофильного замещения в бензольном кольце,
излагаемых в образовательных программах. В качестве ответа принимался
также любой другой разумный порядок не противоречащий этим правилам.
|
|
 |
 |
Для того, чтобы мы могли качественно предоставить Вам информацию, мы используем cookies, которые сохраняются на Вашем компьютере (сведения о местоположении; ip-адрес; тип, язык, версия ОС и браузера; тип устройства и разрешение его экрана; источник, откуда пришел на сайт пользователь; какие страницы открывает и на какие кнопки нажимает пользователь; эта же информация используется для обработки статистических данных использования сайта посредством интернет-сервисов Google Analytics и Яндекс.Метрика). Нажимая кнопку «СОГЛАСЕН», Вы подтверждаете то, что Вы проинформированы об использовании cookies на нашем сайте. Отключить cookies Вы можете в настройках своего браузера.
Сервер создается при поддержке Российского фонда фундаментальных исследований
Не разрешается копирование
материалов и размещение на других Web-сайтах
Вебдизайн: Copyright (C) И. Миняйлова и В. Миняйлов
Copyright (C) Химический факультет МГУ
Написать письмо редактору
|



