Структура
Название
Структура
Название
А
диэтиловый эфир
![]()
метилэтиловый эфир
![]()
метиловый спирт
В
дипропиламин
![]()
пропиловый спирт
Г
триметилфосфин
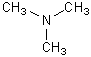
триметиламин
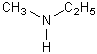
Д
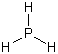
Фосфин
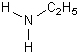
Е
Б
этиловый спирт
![]()
Ж
LXI Московская городская олимпиада школьников по химии
8-1. Старлей Кибулькин сидел, обхватив голову руками. Он не знал, что делать. В его родном городе N появился фальшивомонетчик! Он чеканил фальшивые пятирублевые монеты из железа, которые по виду никак не отличались от настоящих. Полковник Бульбулькин дал ему задание: разработать методы, которыми можно отличить фальшивки от настоящих монет. При этом фальшивки нельзя было уничтожать - они были вещдоками!!! Помогите старлею стать капитаном. Предложите как можно больше методов, которыми можно отличить железные монеты от настоящих.
8-2. Когда 9 января 1769 года Екатерина II подписала манифест о введении в России бумажных денег, за 1000 рублей ассигнациями давали 62,5 пуда (1 пуд = 16,38 кг) медной монеты. На конец 2004 года 1 т меди стола около 3100$, курс доллара – 27,8 руб/$. Сколько граммов весила монета в 10 копеек?
1). Посчитайте курс современного рубля к екатерининскому если считать медь за твердый эквивалент. 2). Какую массу малахита (CuOH)2CO3 нужно было переработать, чтобы выплавить монет на 1000 рублей 1769 года? 3). Предложите цепочку химических реакций, по которой могли получать медь из малахита?
8-3. Вас пригласили в некий регион на берегу моря для налаживания там химической промышленности. В регионе есть уголь, песок и морская вода. Какие полезные вещества можно получить, используя только это сырье и солнечную энергию (напишите, где возможно, уравнения реакций). Не более, чем одним предложением опишите условия его получения.
8-4. Ниже приведена таблица соответствий структур и названий органических соединений. заполните пропуски в ней, обозначенные буквами.
|
Структура |
Название |
Структура |
Название |
|
А |
диэтиловый эфир |
|
метилэтиловый эфир |
|
|
метиловый спирт |
В |
дипропиламин |
|
|
пропиловый спирт |
Г |
триметилфосфин |
|
|
триметиламин |
|
Д |
|
|
Фосфин |
|
Е |
|
Б |
этиловый спирт |
|
Ж |
8-5. Майор Кибулькин ликовал: операция завершилась удачно. Перед ним стояла ничем не примечательная склянка с твердым легкоплавким веществом, которое противник планировал использовать как ракетное топливо. Майор сжег 1 г вещества в кислороде и получил 810 мг воды, 340 мл (н.у.) азота и не получил вообще углекислого газа и других соединений.
1). Что представляло собой это вещество? Напишите его молекулярную и структурную формулу.
2). Напишите уравнение реакции горения неизвестного вещества с кислородом.
3). Чтобы определить массу воды и углекислого газа, майор поглощал их некими поглотителями – оксидами. Какой оксид мог служить в этом опыте поглотителем воды, а какой – углекислого газа? Напишите уравнения реакций. В каком порядке следует располагать поглотители и почему?
8-6. При некоторых заболеваниях у человека наблюдаются резкие скачки температуры тела. Можно считать, что энергия для повышения температуры выделяется при реакции глюкозы С6H12O6 с О2. При этом образуется вода и CO2. Снижение температуры тела достигается за счет испарения воды, выделяющейся в виде пота.
1). Какую массу глюкозы нужно израсходовать на разогревание тела человека массой 60 кг с 36.6°С до 38°С, если при окислении 1 моль глюкозы образуется 2565 кДж энергии? Теплоемкость тела принять за 3000 Дж/(кг×°С). 2). Какую массу воды нужно испарить для обратного снижения температуры, если при испарении 1 моль воды при этой температуре поглощается 43 кДж.
3). Напишите уравнение реакции глюкозы с кислородом воздуха.
8-1. 1) Поднести магнит (настоящая монета не магнитна!)
2) Проверить способность к ржавлению (не очень удачно) - частично разрушается фальшивая монета.
3) Померить тепло- и электропроводность фальшивки и сравнить ее с характеристиками заведомо настоящей монеты.
8-2.
1. 1000 рублей - это 10000 десятикопеечных монет. Они весили 62,5×16,38 = 1023.75 кг. Так что десятикопеечная монета весила 102 г.
2. 1000 рублей соответствуют примерно 1 т меди, которая стоит 3100$. Эта сумма сейчас эквивалентна 3100$×28 руб/$ = 86800 руб. То есть курс современный рубль/екатерининский рубль составит 86,8.
3. Монет на 1000 рублей - это 1023.75 кг меди, что соответствует 16250 моль (Ar(Cu)=63) Значит, количество малахита равно 16250/2 = 8125 моль, что имеет массу 8125моль*220(г/моль) = 1787.5 кг.
4. (CuOH)2CO3 t° 2CuO + H2O + CO2
CuO + C t° CO + Cu
8-3. Любые разумные реакции: электролиз воды (получение кислорода и водорода), получение углекислого газа (сжигание угля), электролиз морской воды (содержащей хлорид натрия) позволит получить газообразный хлор, из него - хлороводород. И т.д.
8-4.
|
Структура |
Название |
Структура |
Название |
|
С2H5-O-C2H5 |
диэтиловый эфир |
|
метилэтиловый эфир |
|
|
метиловый спирт |
(C3H7)2N-H |
дипропиламин |
|
|
пропиловый спирт |
(CH3)3P |
триметилфосфин |
|
|
триметиламин |
|
Метиэтиламин |
|
|
фосфин |
|
этиламин |
|
С2H5-OH |
этиловый спирт |
|
Дипропиловый эфир |
8-5. 1. Найдем количество углерода и азота.
n(N) = 0.340/22.4*2 = 0.030 моль.
n(H) = 810/18*2 = 0.090 моль.
Соотношение N:H = 1:3.
Это мог бы быть аммиак, но аммиак газ. Значит, в веществе еще есть кислород. Найдем его массу в 1 г.
m(O) = 1 - 0.03*14-0.09*1 = 0.49 (г) = 0.03 моль.
Формула NH2OH (NH3O).
2. 2NH2OH + 0.5O2 = N2 + 3H2O
3. P2O5 и CaO:
P2O5 + H2O = 2HPO3 (или H3PO4)
CaO + CO2 = CaCO3
Сначала P2O5, потом CaO, иначе CaO поглотитводу
8-6. 1. Нужно нагреть 60 кг тела на 1.4С.
Для нагревания 1 кг на 1С требуется 3000 Дж. Значит, на все нагревание нужно 252000 Дж = 252 кДж.
Для этого нужно окислить 252/2565*180 = 17.7 г глюкозы.
3. Чтобы остыть, нужно испарить 252/43 = 5,9 моль воды, что соответствует 106 г.
4. C6H12O6 + 6O2 = 6CO2 + 6H2O.