 |

|
|
[ На предыдущий раздел]
4. Наиболее распространенные процессы
мембранного разделения
Из баромембранных процессов наиболее распространены: газовая эффузия, микро-, ультра- и нанофильтрация и обратный осмос. Эти процессы применяют для газо- и жидкофазного разделения на пористых мембранах.
Газовая эффузия – течение газа через пористую перегородку под действием разности давлений. Эффузия в условиях вакуума называется кнудсеновским течением или молекулярной эффузией. Понятие вакуума, как известно, относительное. Вакуум представляет собой такое разрежение газа, при котором средняя длина свободного пробега молекул больше размера содержащего газ сосуда. Поэтому, чем меньше размеры сосуда, в котором находится газ, тем при больших давлениях в нем создаются условия вакуума. Так, для газа, находящегося в пористых средах с размерами пор 10 2ё103 нм, атмосферное давление является вакуумом. Скорость преодоления молекулами пористой перегородки зависит от скорости их движения, а более легкие молекулы всегда обладают большей скоростью, что и приводит к разделению.
Если условие вакуума нарушено, то есть молекулы могут сталкиваться не только со стенкой, но и друг с другом, то такое течение называется пуазейлевским или вязкостным. В реальных мембранах, имеющих определенное распределение пор по размерам, как правило, реализуются оба типа течения. Для чистого газа суммарный поток имеет вид
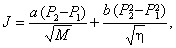 (20) (20)
где a и b – характеристики геометрии порового пространства мембраны, DP = P2 – P1 – перепад давлений, M – молекулярная масса, h – динамическая вязкость. Первый член суммы представляет собой кнудсеновский поток, а второй – пуазейлевский. Кнудсеновский поток зависит от индивидуальных свойств молекул, а пуазейлевский не зависит, поэтому он не сопровождается эффектами разделения. Преобразуя уравнение (20) в
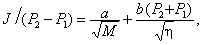 (21) (21)
по линейной зависимости левой части от переменной ( P2 + P1) можно определить параметры a и b.
В смеси газов
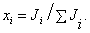 (22) (22)
Отсюда для бинарной смеси в случае так называемого идеального разделения, когда P1 ® 0, то есть полностью удаляется газ, прошедший через мембрану,
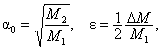 (23) (23)
где M1 – молекулярная масса более легкого компонента. С учетом противодавления (P1 № 0)
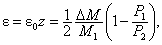
где z = 1 – P1 / P2 – коэффициент полезного действия мембраны.
Микрофильтрацию применяют для отделения растворителя от коллоидных или взвешенных микрочастиц размерами 0,1ё10 мкм.
Ультрафильтрацию используют для разделения растворов, в которых молекулярная масса растворенных компонентов намного больше молекулярной массы растворителя. Обычно при ультрафильтрации коллоидные и высокомолекулярные вещества отделяются от низкомолекулярных.
Нанофильтрацию или низконапорный обратный осмос применяют для задержки частиц с размерами порядка нанометра.
Обратный осмос – баромембранный процесс разделения истинных растворов. Движущая сила процесса
где P – давление над исходным раствором, DП = П1 – П2 – разность между осмотическими давлениями исходного раствора и фильтрата. Для полупроницаемых мембран П2 = 0, так как в фильтрате отсутствуют растворенные вещества. Если P = DП, то потоки растворителя слева и справа через мембрану одинаковы, и два раствора различной концентрации, разделенные мембраной, находятся в равновесии. При P < DП растворитель преимущественно переходит в более концентрированный раствор. Это явление называется осмосом.
Важнейшим параметром, влияющим на производительность баромембранных процессов, является рабочее давление. В микрофильтрации оно составляет 0,03 ё0,1 МПа, в ультрафильтрации – 0,3ё1 МПа, в нанофильтрации – 1ё3 МПа, в обратном осмосе – 3ё10 МПа.
Размер частиц, проникновение которых через мембрану необходимо предотвратить, тесно связан с размером пор. В микрофильтрационных мембранах он более 50 нм, в ультра- и нанофильтрационных – 5 ё50 нм, в обратноосмотических – 3ё5 нм. Но не только средний размер пор определяет селективность. Высокую селективность при увеличении размера пор можно сохранить за счет придания мембране электрического заряда и увеличения ее гидрофильности. Следует отметить, что размер пор обратноосмотических мембран много больше размеров молекул и ионов. Следовательно, селективность обратного осмоса вообще не связана с ситовым эффектом. Ее причиной является изменение концентрации молекул и ионов под влиянием силового поля поверхности пор.
Мощным рычагом управления селективностью баромембранных методов является их сочетание с другими процессами. Например, электроосмофильтрация – обратный осмос в постоянном электрическом поле. Такой гибридный метод позволяет извлекать целевые вещества из многокомпонентных растворов, в том числе, из природных и сточных вод. Известен также метод КОУФ, сочетающий комплексообразование и ультрафильтрацию. В нем используется вспомогательное вещество, образующее комплексы с компонентом, который нужно извлечь. Комплексы легко отфильтровываются, а затем разрушаются, освобождая целевое вещество, и комплексообразователь используется вновь.
Основными концентрационномембранными процессами являются диффузионное газоразделение, первапорация, диализ. Их используют для разделения газов и жидкостей с помощью непористых мембран из полимеров, стекол, металлических сплавов .
Диффузионное газоразделение – процесс селективного трансмембранного газопереноса под влиянием градиента концентрации разделяемых компонентов по толщине мембраны, который задают различные парциальные давления газа на противоположных сторонах мембраны. Для бинарной смеси в простейшем случае, когда сорбция равновесна и подчиняется закону Генри, коэффициент диффузии постоянен, десорбция происходит в вакуум и не лимитирует скорость процесса, коэффициент разделения равен отношению коэффициентов проницаемости a = Q1 / Q2, а сама величина Qi представляет собой произведение коэффициента диффузии на коэффициент растворимости (константу Генри) Qi = si ∙ Di. Таким образом, эффект разделения определяется как термодинамическими (s), так и кинетическими (D) свойствами системы мембрана–газ.
Коэффициенты диффузии газов в полимерных мембранах различаются на 3ё7 десятичных порядков. Область изменения коэффициентов растворимости значительно меньше. Значение коэффициента диффузии определяется, главным образом, свободным объемом в полимерах, а коэффициента растворимости – межмолекулярным взаимодействием. Они могут заметно измениться при наличии специфических взаимодействий полимер–диффузант, к которым относятся донорно-акцепторное взаимодействие, обратимое связывание в комплекс, образование водородных связей и т.д.
Термин “первапорация” образован из слов “проницание” и “испарение” (permeation + evaporation = pervaporation) и означает испарение жидкостей через мембрану. Процесс состоит в том, что на поверхности жидкости находится мембрана, а пермеат в виде пара отводится током инертного газа, либо конденсируется, попадая в охлаждаемую вакуумированную ловушку. В первапорации используют лиофильные непористые полимерные мембраны. Для них характерна анизотропия набухания, существенно нелинейный профиль концентрации, сильная концентрационная зависимость коэффициента диффузии, неравномерность развития релаксационных процессов по толщине мембраны. Наличие на поверхности жидкости полимерной мембраны полностью подавляет специфику испарения со свободной поверхности. Поэтому во многих случаях селективность разделения очень высокая, а пермеат может быть обогащен как более, так и менее летучим компонентом.
Диализ основан на различных скоростях диффузии растворенных веществ, отличающихся молекулярной массой, через мембрану, разделяющую концентрированный и разбавленный растворы. С течением времени скорость процесса снижается вследствие диффузии растворителя в обратном направлении.
К термомембранным процессам относится мембранная дистилляция. Систематическое экспериментальное и теоретическое изучение этого метода началось с 1995 г. Мембранная дистилляция состоит в селективном переносе паров воды через микропористую гидрофобную мембрану, разделяющую два водных раствора, находящихся при различных температурах. Обычно температура концентрированного раствора составляет 50 ё80°C, а дистиллята 20ё25°C. Для проведения процесса не требуется избыточное рабочее давление и может быть использована низкопотенциальная теплота. Движущей силой мембранной дистилляции является разность давлений насыщенных паров растворителя, обусловленная разностью температур, которая является регулируемым и управляющим параметром процесса. Диффузионный механизм мембранной дистилляции подтверждается линейной зависимостью потока пермеата от обратной толщины мембраны, что характерно для фиковской диффузии. Кроме того, высокая селективность (f = 0,99) указывает на отсутствие конвективного потока. Гидрофобность мембраны обеспечивает пространственное разделение и стабилизацию поверхностей испарения и конденсации. Поэтому практически невозможно использовать мембранную дистилляцию для растворов, содержащих поверхностно-активные вещества (ПАВ), улучшающие смачиваемость поверхности микропор.
В примембранных слоях не только концентрация, но и температура, вследствие теплопереноса через мембрану, отличается от своего значения в объеме. Это явление получило название температурной поляризации. Температурная поляризация оказывает отрицательное влияние на производительность мембранной дистилляции, поскольку температура поверхности испарения снижается, а поверхности конденсации – повышается.
Наиболее распространенным электромембранным процессом является электродиализ – метод разделения растворов электролитов под действием разности электрических потенциалов, которая создается по обе стороны чередующихся анионо- и катионообменных мембран ( рис. 2). Электродиализаторы состоят из ряда камер, через которые прокачивают растворы электролитов. В крайних камерах расположены электроды. Поскольку анионообменные мембраны пропускают только анионы, а катионообменные – только катионы, то камеры поочередно обогащаются и обедняются электролитом. В результате поток исходного раствора разделяется на два потока: разбавленный (обессоленный) и концентрированный. Элементарным звеном электродиализатора является так называемая парная камера, состоящая из одной катионо- и одной анионообменной мембран, а также из растворов в каналах обессоливания и концентрирования. Эффективность использования электроэнергии в электродиализаторе составляет 80ё95%. Если учесть, что этот процесс не требует дополнительных химических реагентов, в нем не создаются вещества, отравляющие окружающую среду (как правило, из растворов удаляются микрокомпоненты), то становится понятным, почему электродиализ так же, как и остальные мембранные процессы, относят к экологически целесообразным, ресурсо- и энергосберегающим.
[ На следующий раздел] [На Содержание]
Copyright ©
|
|
 |
 |
Для того, чтобы мы могли качественно предоставить Вам информацию, мы используем cookies, которые сохраняются на Вашем компьютере (сведения о местоположении; ip-адрес; тип, язык, версия ОС и браузера; тип устройства и разрешение его экрана; источник, откуда пришел на сайт пользователь; какие страницы открывает и на какие кнопки нажимает пользователь; эта же информация используется для обработки статистических данных использования сайта посредством интернет-сервисов Google Analytics и Яндекс.Метрика). Нажимая кнопку «СОГЛАСЕН», Вы подтверждаете то, что Вы проинформированы об использовании cookies на нашем сайте. Отключить cookies Вы можете в настройках своего браузера.
Сервер создается при поддержке Российского фонда фундаментальных исследований
Не разрешается копирование
материалов и размещение на других Web-сайтах
Вебдизайн: Copyright (C) И. Миняйлова и В. Миняйлов
Copyright (C) Химический факультет МГУ
Написать письмо редактору
|


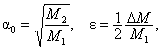 (23)
(23)