|
[На
предыдущую главу]
3. Транспорт
аминокислот в ионообменных мембранах
Сложный характер
процессов, происходящих в ЭМС, содержащих
аминокислоты, и невозможность его теоретического
описания приводят к необходимости получения
эмпирической зависимости удельной электропроводности
мембран от аналитической концентрации
компонентов в объеме раствора.
В мембранной системе
происходит сорбция компонентов фазой мембраны,
определяющая величины концентраций, а
затем миграция их в соответствии с подвижностями.
Для смесей, содержащих аминокислоты, возможны
химические взаимодействия компонентов,
изменяющие ионный состав, как в равновесном
растворе, так и в фазе мембраны. При этом
экспериментально с наибольшей точностью
и достоверностью мы можем определить лишь
исходные (аналитические) концентрации
аминокислот и минеральных компонентов.
Поэтому наибольший интерес представляют
функциональные зависимости электропроводности
ионообменных мембран в сложных аминокислотных
смесях от таких параметров системы, как
аналитические концентрации компонентов.
В [12]
решение этой задачи было проведено с использованием
многомерного регрессионного анализа и
методов математического планирования
эксперимента. Полученные регрессионные
уравнения представлены в табл.
4 для кодированных концентраций компонентов
(Х) [12]. В регрессионных
моделях 1 и 2 содержатся только статистически
значимые коэффициенты регрессии при уровне
значимости Р = 0,95. Модели 2 получены из моделей
1 путем экстраполяции на нулевую концентрацию
минерального компонента в смеси.
Кроме формально-математического
смысла, коэффициенты регрессии позволяют
ранжировать термы уравнения по степени
их влияния. Так большему по абсолютной
величине коэффициенту регрессии соответствует
больший эффект влияния фактора.
Наиболее сильно
на электропроводности мембраны МК-40 сказывается
изменение концентрации соляной кислоты
в равновесном растворе. При увеличении
концентрации HCl возрастает и электропроводность
МК-40, соответственно при снижении концентрации
HCl электропроводность МК-40 уменьшается.
В целом этот эффект был бы тривиальным,
если бы в равновесном растворе не присутствовала
“нейтральная”
аминокислота.
В зависимости
от концентрации соляной кислоты большая
или меньшая часть цвиттер-ионов аминокислот
становится катионами. С математической
точки зрения это выражается наличием в
регрессионных моделях (табл.
4) членов, отражающих влияние концентрации
аминокислот и эффектов двойных взаимодействий
типа Х1Х2.
При концентрациях
аминокислот 0,1 М удельная электропроводность
мембраны МК-40 становится малочувствительной
к изменению концентрации соляной кислоты,
тогда как при концентрациях аминокислот
0,01 М, зависимость (ХHCl)
линейна и близка к электропроводности
мембраны в чистой HCl. Наиболее ярко эти
тенденции проявляются для смеси соляная
кислота–лейцин.
Миграционное
число переноса компонента i можно оценить
по данным кондуктометрических измерений:
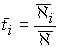 , (1) , (1)
где 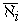 – доля электропроводности
мембраны, обеспечиваемая только ионами
i-го сорта,
– доля электропроводности
мембраны, обеспечиваемая только ионами
i-го сорта, 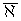 – общая удельная электропроводность мембраны
в смешанном растворе.
– общая удельная электропроводность мембраны
в смешанном растворе.
Используя формулу
(1) можно рассчитать числа переноса катионов
аминокислот в мембране МК-40 при конкурирующем
переносе ионов водорода [13].
Для этого необходимо разложить общую удельную
электропроводность мембраны в смешанном
растворе на две составляющие – аминокислотную
и водородную.
На рис.
5 и 6
в виде трехмерных диаграмм представлены
результаты расчетов чисел переноса катионов
глицина и аланина в мембране МК-40 в зависимости
от аналитических концентраций аминокислоты
и соляной кислоты в равновесном растворе.
При малых концентрациях
глицина и аланина (0,01 М) в смешанном равновесном
растворе числа переноса катионов аминокислот
в мембране МК-40 составляют 0,05–0,1 и практически
не зависят от концентрации HCl в изучаемом
диапазоне. Это означает, что основным переносчиком
электричества в мембране являются ионы
водорода.
Увеличение концентрации
аминокислоты до 0,05 М при постоянстве концентрации
HCl (0,05 М) приводит к возрастанию чисел переноса
катионов глицина до 0,15, а аланина – до 0,3.
Максимальное число переноса катионов глицина
равно 0,2 и соответствует случаю, когда аналитическая
концентрация глицина в пять раз выше, чем
концентрация соляной кислоты. В подобной
ситуации число переноса катионов аланина
составляет 0,45. Этот факт показывает существенное
различие в электрохимическом поведении
нейтральных аминокислот – глицина и аланина
– с близкими изоэлектрическими точками
и создает предпосылки к их электроионитному
разделению.
[На
следующую главу] [На
Содержание]
Copyright ©
|

