МАТРИЧНАЯ ИЗОЛЯЦИЯ И ИК-ХЕМИЛЮМИНИСЦЕНЦИЯ ПРОДУКТОВ РЕАКЦИИ С2 О2Н2 И С2О2Cl2 C ПЕРОКСИДОМ ВОДОРОДА.
Серебренников Л.В., Головкин А.В.,
Уваров Н.А., Шевельков В.Ф.
Кафедра физической химии
Реакции глиоксаля и некоторых его
производных с пероксидом водорода, если
проводить их в жидкой фазе, приводят к
образованию двух- и трехатомных газофазных
молекул: (СНО)2+ (ОН)2 ![]() 2СО2 + 2Н2 (-
2СО2 + 2Н2 (-![]() H=384.1 кдж/
моль, lgKp=217.2 при 100К), и (СНО)2 + (ОН)2
H=384.1 кдж/
моль, lgKp=217.2 при 100К), и (СНО)2 + (ОН)2
![]() 2СО +
2Н2 О (-
2СО +
2Н2 О (-![]() H=303.2 кдж/ моль, lgKp=178.8 при
100К); (CClO)2 + (OH)2
H=303.2 кдж/ моль, lgKp=178.8 при
100К); (CClO)2 + (OH)2 ![]() 2CO2 + 2HCl, (CClO)2 + (OH)2
2CO2 + 2HCl, (CClO)2 + (OH)2
![]() 2CO +
2HOCl и т.д. Особенностью этих реакций является то,
что теплоты основных каналов, значительные сами
по себе, недостаточно велики для электронного
возбуждения продуктов. Это дает основание
предполагать возможность получения в газовой
фазе больших количеств
колебательно-возбужденных простых молекул для
приведенных примеров CO2, CO, HCl, H2O, HOCl).
Механизмы обсуждаемых реакций достаточно сложны
и могут включать ряд промежуточных продуктов,
экспериментальное определение некоторых из них
и являлось целью работы.
2CO +
2HOCl и т.д. Особенностью этих реакций является то,
что теплоты основных каналов, значительные сами
по себе, недостаточно велики для электронного
возбуждения продуктов. Это дает основание
предполагать возможность получения в газовой
фазе больших количеств
колебательно-возбужденных простых молекул для
приведенных примеров CO2, CO, HCl, H2O, HOCl).
Механизмы обсуждаемых реакций достаточно сложны
и могут включать ряд промежуточных продуктов,
экспериментальное определение некоторых из них
и являлось целью работы.
Метод матричной изоляции идеально
подходит для изучения продуктов первой стадии
химического процесса, и с его помощью нам удалось
измерить ИК-спектры поглощения двух различных
комплексов состава (C2O2H2*H2O2)
[1] в системе глиоксаль - пероксид водорода (1) и
интермедиата [HC2O4Cl] , образовавшегося
после отщепления одной молекулы HCl, в системе
оксалилхлорид - пероксид водорода (2). При
изучении ИК-спектров хемилюминесценции
газофазных продуктов [2] в (1) были
зарегистрированы и отнесены полосы различных
колебательных переходов СО2 , СО и Н2О,
причем сопоставление энергии заселяемых в
реакции состояний продуктов с ![]() H процесса привело к
заключению о реализации каналов с асимметричным
распределении энергии. Суммарные механизмы
могут быть, например, такими: (а) (COH)2 + H2O2
= CO(v=12) + CO(v=0) + 2H2O(000) + ~ 1500 см-1, (б) (COH)2
+ H2O2 = CO(v=14) + CO2(000) + H2O(000) + H2(0)
+ ~ 1270 см-1, (в) (COH)2 + H2O2 = 2CO2(G
» 12700 см-1) + H2(v=1) + H2(v=2) - ~ 335 см-1.
Таким образом, косвенно подтвердился вывод о
существования в реакции (1) по меньшей мере двух
интермедиатов, каждый из которых приводит в
результате к образованию своих продуктов. При
изучении хемилюминисценции системы (2), помимо
полос CO2, CO и HCl наблюдались полосы молекул
OH, HOCl и, с меньшей достоверностью, COCl. В сочетании
с данными матричных исследований этой системы (а
также системы (COCl)2 + H2O) это
позволило сделать некоторые заключения о
механизме процесса. Показано, что первой стадией
является отщепление HCl и образование
интермедиата: (COCl)2 + H2O2 => HCl + [C2ClO4H].
Распад интермедиата в газовой фазе происходит по
разным маршрутам [C2ClO4H] (5) => ([?] + ?)
=> CO2 + OH + COCl и [C2ClO4H] (5) => ([?]
+ ?) => CO2 + CO + HOCl, причем в рамках одного
образование всех зарегистрированных продуктов
невозможно, маршрутов должно быть не менее двух.
Обозначения ([?] + ?) поставлены с целью подчеркнуть
сложность механизма, приводящего к двум наборам
продуктов: HCl*, CO2*, OH*, COCl*
и HCl*, CO*, CO2*, HOCl. На ряде
переходов OH, HCl и CO наблюдалось испускание
аномально высокой интенсивности, связанное, по
всей вероятности, с эффектом усиления в области
адиабатического расширения газообразных
продуктов реакции.
H процесса привело к
заключению о реализации каналов с асимметричным
распределении энергии. Суммарные механизмы
могут быть, например, такими: (а) (COH)2 + H2O2
= CO(v=12) + CO(v=0) + 2H2O(000) + ~ 1500 см-1, (б) (COH)2
+ H2O2 = CO(v=14) + CO2(000) + H2O(000) + H2(0)
+ ~ 1270 см-1, (в) (COH)2 + H2O2 = 2CO2(G
» 12700 см-1) + H2(v=1) + H2(v=2) - ~ 335 см-1.
Таким образом, косвенно подтвердился вывод о
существования в реакции (1) по меньшей мере двух
интермедиатов, каждый из которых приводит в
результате к образованию своих продуктов. При
изучении хемилюминисценции системы (2), помимо
полос CO2, CO и HCl наблюдались полосы молекул
OH, HOCl и, с меньшей достоверностью, COCl. В сочетании
с данными матричных исследований этой системы (а
также системы (COCl)2 + H2O) это
позволило сделать некоторые заключения о
механизме процесса. Показано, что первой стадией
является отщепление HCl и образование
интермедиата: (COCl)2 + H2O2 => HCl + [C2ClO4H].
Распад интермедиата в газовой фазе происходит по
разным маршрутам [C2ClO4H] (5) => ([?] + ?)
=> CO2 + OH + COCl и [C2ClO4H] (5) => ([?]
+ ?) => CO2 + CO + HOCl, причем в рамках одного
образование всех зарегистрированных продуктов
невозможно, маршрутов должно быть не менее двух.
Обозначения ([?] + ?) поставлены с целью подчеркнуть
сложность механизма, приводящего к двум наборам
продуктов: HCl*, CO2*, OH*, COCl*
и HCl*, CO*, CO2*, HOCl. На ряде
переходов OH, HCl и CO наблюдалось испускание
аномально высокой интенсивности, связанное, по
всей вероятности, с эффектом усиления в области
адиабатического расширения газообразных
продуктов реакции.
Литература
1.Головкин А.В., Серебренников Л.В., Уваров Н.А.,
Шевельков В.Ф.
Исследование реакции глиоксаля с перекисью
водорода методом ИК-спектроскопии в твердом
ксеноне.
ЖФХ, 1998, 72, №11, 1843.
2.Серебренников Л.В., Головкин А.В., Полякова М.В.,
Шевельков В.Ф. ИК-хемилюминесценция газофазных
продуктов реакции мономерного глиоксаля с
пероксидом водорода,
ЖФХ, 2001, 75. № 4 (в печати).
ВОЗМОЖНОСТИ ТЕРМОЛИНЗОВОЙ
СПЕКТРОМЕТРИИ
ПРИ ИЗУЧЕНИИ ОСОБЕННОСТЕЙ ПРОТЕКАНИЯ РЕАКЦИЙ
НА УРОВНЕ МАЛЫХ СОДЕРЖАНИЙ
Проскурнин М.А., Черныш В.В.,
Кононец М.Ю., Бендрышева С.Н .
Кафедра аналитической химии
Показаны возможности термолинзовой спектрометрии (ТЛС) при исследовании термодинамики и кинетики реакций комплексообразования и окисления-восстановления, использующихся в аналитической химии, на уровне нанограммовых содержаний реагирующих компонентов. На примере систем медь(I)–2,9-диметил-1,10-фенантролин, медь(I), железо(II)–1,10-фенантролин, висмут(III ), медь(I), свинец(II)–йодид, никель(II)–диметилглиоксим, медь(II), кобальт(III), никель(II)–ДЭДТК показано, что условия ТЛС лучше соответствуют приближению идеальных растворов, что дает возможность повысить надежность и точность определения констант равновесия по сравнению с традиционной спектрофотометрией и потенциометрией. В частности, впервые определены ступенчатые константы в системе медь(I)–1,10-фенантролин. Продемонстрировано, что ТЛС также может быть использована для исследования равновесия осаждения–растворения; найдены значение констант растворимости в воде иодидов меди(I ), свинца(II) и олова(II).
Для систем медь(I)–2,9-диметил-1,10-фенантролин и железо(II)–1,10-фенантролин показаны изменения в скорости реакции образования хелатов при на уровне концентраций металлов n? 10–8 моль/л.В частности, исследована кинетика диссоциации диэтилдитиокарбаматных комплексов меди(II), кобальта(III) и никеля(II) в присутствии хлорид- и бромид- ионов. Найдены характеристические константы скорости, получены их зависимости от кислотности среды. Из данных термолинзовых измерений показано, что разложение комплексов включает в себя два процесса — обратимую диссоциацию комплексов и необратимое окисление диэтилдитиокарбамовой кислоты. Найдены условия, в которых преобладает каждый из процессов, и показано, что, в отличие от традиционной спектрофотометрии, в условиях термолинзового эксперимента возможно одновременное раздельное рассмотрение этих процессов.
Учет изменения условий проведения
рассмотренных аналитических реакций в новых
условиях позволил улучшить селективность, а
также чувствительность аналитического
определения. В целом, за счет использования в
аналитических методиках особенностей
химического взаимодействия на уровне
нанограммовых содержаний, а также минимизации
контрольного опыта с использованием
экстракционных и сорбционных методов достигнуты
пределы обнаружения кобальта
2-нитрозо-1-нафтолом, железа 1,10–фенантролином и
никеля диметилглиоксимом равные,
соответственно, 3 ![]() 10–12 моль/л, 4
10–12 моль/л, 4 ![]() 10–9
моль/л и 2
10–9
моль/л и 2 ![]() 10–10 моль/л; диапазоны
определяемых содержаний составляют 3–5 порядков.
10–10 моль/л; диапазоны
определяемых содержаний составляют 3–5 порядков.
Термолинзовая спектрометрия применена для исследования адсорбционного равновесия на уровне нанограммовых содержаний реагентов. Разработана методика исследования адсорбции с использованием ТЛС для определения равновесной концентрации адсорбата в растворе. Исследована кинетика адсорбции нанограммовых содержаний трис-(1,10-фенантролината) железа(II) и диэтилдитиокарбаматов меди(II), кобальта(III) и никеля(II) на силикагелях.
Показаны возможности ТЛС при изучении адсорбции ферроина на сорбентах с малой емкостью (стекло ХС и кварц). Получено хорошее совпадение экспериментальной поверхностной концентрации комплекса с моделью адсорбированного монослоя. Абсолютное детектируемое количество составляет 4.1 ? 10–15 моль. Показано, что ТЛС позволяет определять количества адсорбированного ферроина на поверхности кварца до уровня 0.01 монослоя. Оценены характеристики адсорбции трис-(1,10-фенантролината) железа(II) и диметилглиоксимата никеля(II ) из водных и водно-этанольных растворов на лабораторном стекле (ГОСТ 1770-74) на уровне нанограммовых содержаний адсорбата в растворе. В случае комплекса железа оценена поверхностная концентрация необратимых и обратимых центров сорбции.
ИЗОТОПНЫЕ СДВИГИ В СПЕКТРАХ ЯМР ВОДЫ : НОВЫЙ МЕТОД ИЗУЧЕНИЯ КЛАСТЕРНОЙ СТРУКТУРЫ И ПРОТОННОГО ОБМЕНА В ВОДЕ И ЕЕ СМЕСЯХ С ОРГАНИЧЕСКИМИ РАСТВОРИТЕЛЯМИ
Сергеев Н. М.
Кафедра органической химии
Общепринятая модель воды включает
кластерное описание структуры воды и протонный
обмен в воде. Однако детали этого описания
продолжают оставаться неизвестными. К числу пока
еще нерешенных проблем можно отнести равновесие
и динамику поведения кластеров в воде, механизм
протонного обмена в воде, а также характер
взаимодействий воды с другими растворителями
или растворенными веществами. Наши работы
последних лет [1-3] показали , что решение ряда этих
проблем достижимо при использовании метода
ядерного магнитного резонанса (ЯМР). Важным
инструментом наблюдения являются изотопные
эффекты (ИЭ) на параметры спектров ЯМР. Впервые
нам удалось наблюдать ИЭ дейтерия на химические
сдвиги протонов и ядер 17О в воде. Это
позволило наблюдать отдельные сигналы 1 Н
ЯМР для молекул Н2 О и HDO (или сигналы HDO и D2O
в спектрах ЯМР 2Н) Кроме того были
обнаружены три сигнала в спектрах ЯМР 17 О
от всех трех форм Н2 О, HDO и D2O. Это
позволило впервые определить константы
равновесия в классической реакции изотопного
обмена H2O + D2O ![]() 2 HDO без необходимости знания начальных
концентраций H2 O и D2O. Наконец, при
использовании препаратов 17 О обогащенной
воды (до 30 %) мы обнаружили ИЭ, вызванные 16 О, 17О
и 18 О изотопами. Наблюдение сигналов
отдельных изотопомеров позволило провести
эксперименты по наблюдению протонного обмена в
воде для растворов воды в органических
растворителях. Экспериментальные данные
показывают, что при низких концентрациях воды в
органических растворителях (до 6% в нитрометане и
до 60% в диоксане, см. рис. 1) обмен остается
медленным. Скорость обмена пропорциональна
концентрации воды с, и время жизни
протона в индивидуальной молекуле не менее 0.5 с
при указанных выше концентрациях. При повышении
концентрации воды в диоксане (до 100 %) скорость
начинает быстро возрастать (пропорциональна сn
где n - порядок реакции). По предварительным
оценкам
2 HDO без необходимости знания начальных
концентраций H2 O и D2O. Наконец, при
использовании препаратов 17 О обогащенной
воды (до 30 %) мы обнаружили ИЭ, вызванные 16 О, 17О
и 18 О изотопами. Наблюдение сигналов
отдельных изотопомеров позволило провести
эксперименты по наблюдению протонного обмена в
воде для растворов воды в органических
растворителях. Экспериментальные данные
показывают, что при низких концентрациях воды в
органических растворителях (до 6% в нитрометане и
до 60% в диоксане, см. рис. 1) обмен остается
медленным. Скорость обмена пропорциональна
концентрации воды с, и время жизни
протона в индивидуальной молекуле не менее 0.5 с
при указанных выше концентрациях. При повышении
концентрации воды в диоксане (до 100 %) скорость
начинает быстро возрастать (пропорциональна сn
где n - порядок реакции). По предварительным
оценкам
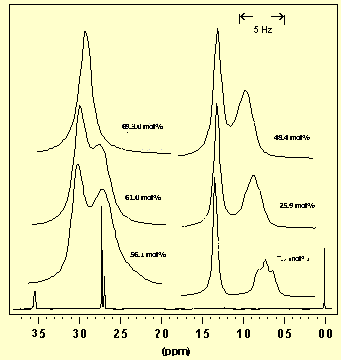 |
Рис. 1. Спектры ЯМР 1 Н растворов H2O/D2 O (1:1) в диоксане-d8 при различных концентрациях (Bruker AC-200). Обзорный спектр (внизу) показывает сигналы TMС (0 м.д.), диоксана-d7 (при 3.55 м.д.) и воды H2O и HDO около 2.7 ppm. Вставки показывают сигналы воды H2 O(синглет) и HDO (триплет из-за взаимодействия H-D , дейтерий спин 1) при различных концентрациях 7.7 (b), 25.9 (c), 48.4 (d), 56.1 (e), 61.0 (f) и 69.3 мол. % (g). Шкалы на вставках в Гц и они даются относительно произвольного нуля. |
порядок реакции составляет 10-11, что указывает на участие в промежуточных комплексах (оксониевых ионах) кластеров высокого порядка.
Литература
1. N.M. Sergeyev, N.D. Sergeyeva and W.T. Raynes,
J. Magn. Res., 1999, 137, 311.
2.N. M. Sergeyev. N. D. Sergeyeva, W.T. Raynes, and Yu. A.
Strelenko,
Chem Phys. Letters, 1997, 227, 142.
3. N. D. Sergeyeva, N. M. Sergeyev, and J. P. Jacobsen,
J. Chem. Soc. Chem. Comm., 1998, 1355.
Выражаем благодарность РФФИ за финансовую поддержку (грант РФФИ N 00-03-32314).
МАТРИЧНАЯ СТАБИЛИЗАЦИЯ ИНТЕРМЕДИАТОВ НА АКТИВИРОВАННОЙ ПОВЕРХНОСТИ ТВЕРДЫХ ТЕЛ
Мельников М.Я., Пергушов В.И.
Кафедра химической кинетики
Одно из основных достоинств метода матричной изоляции, заключающееся в существенном ограничении трансляционной подвижности активных интермедиатов, одновременно является и недостатком, ограничивая его возможности при исследовании механизмов бимолекулярных реакций, реакций диссоциации и т.п. Кроме того энергии активации реакций мономолекулярных превращений для многих типов радикалов лежат в диапазоне 15-25 ккал/моль и следовательно эти "активные" в реакциях рекомбинации, отрыва или замещения частицы могут быть стабильными в отсутствие реакционноспособного окружения при комнатной и более высоких температурах.
Идея использовать для исследований реакционной способности радикалов развитую поверхность минерального носителя, на которой в результате различных воздействий можно создавать разные по природе собственные дефекты, в т.ч. и парамагнитные, способные в реакциях присоединения и других процессах, приводить к образованию различных по структуре радикалов, "привитых" к поверхности оказалась весьма плодотворной. Основными требованиями к таким системам являются: высокие величины энергии связей в молекулах носителя, обеспечивающие его химическую инертность, и достаточная изолированность создаваемых дефектов, исключающая их взаимное влияние.
В настоящей работе на примере выполненных нами в последние годы исследований показаны уникальные возможности метода матричной стабилизации на поверхности диоксида кремния применительно к молекулярной сборке разных по структуре активных интермедиатов, изучению механизма и эффективности различных термических и фотохимических реакций с их (радикалов, силиленов) участием. Проанализирована молекулярная динамика радикалов (величины характеристических времен вращательной корреляции, коэффициенты вращательной диффузии и их температурные зависимости), "привитых" к поверхности диоксида кремния. Для ряда исследованных реакций выявлено влияние активированной поверхности, вызывающее инверсию селективности изучаемых процессов.
Авторы выражают благодарность ФЦП "Интеграция" (проект А0114), Российскому Фонду фундаментальных исследований (проект 00-03-32109) и программе "Университеты России" (проект 990399) за финансовую поддержку исследований.
НОВЫЙ МАРШРУТ САМООРГАНИЗАЦИИ ВЫСОКОДИСПЕРСНОГО ОКСИДА АЛЮМИНИЯ: ТЕКСТУРЫ В ВИДЕ ПОЛЫХ МАКРОТРУБОК
Бердоносов С.С., Баронов С.Б.,
Кузьмичева Ю.В., Бердоносова Д.Г., Мелихов И.В.
Кафедра радиохимии
При нагревании на воздухе или в атмосфере водорода до температуры 160-200oC и выше хлорида алюминия, полученного взаимодействием хлора и металла и затем частично гидролизованного с поверхности парами воды обнаружено образование Al2O3 в двух формах. Одна форма — это высокодисперсный порошок со средним размером частиц около 0,1 мкм (по массе эта форма доминирует). Вторая форма — это полые трубки диаметром 10-300 мкм и длиной от 100 мкм до 6 см (макротрубки). Толщина стенок трубок составляла около 1/20 - 1/4 от их диаметра. Скорость роста трубок была равна около 1 мм/с и зависела от скорости нагрева исходного материала, обычно формирование трубок происходило в течение 10-60 с. В ходе роста трубок наблюдалось выделение из их отверстий белого дыма (вероятно, состоящего из микрочастиц оксида алюминия, а также HCl, паров AlCl3 и воды). Когда выделение дыма прекращалось, рост трубок останавливался. Трубки механически устойчивы и сохраняются неделями на воздухе без видимых изменений. По данным рентгеновского излучения, материал трубок слабо кристалличен; его рентгенограмма содержит две слабые линии фазы корунда.
Согласно данным рентгенофлуоресцентного, макротрубки состоят из Al2O3 с небольшой (2-4%) примесью хлора. О том, что материал трубок — Al2O3, свидетельствуют также данные ИК микро-спектроскопии. Внутренняя и внешняя поверхность макротрубок охарактеризована методами электронной и атомно-силовой микроскопии. Из полученных снимков следует, что стенки макротрубок составлены из плотно пригнанных друг к другу нано- и микрочастиц. Предложен механизм формирования макротрубок и обсуждены перспективы их применения.
ЭФФЕКТ КАТАЛИТИЧЕСКОГО УПРОЧЕНИЯ ПОРИСТЫХ МАТЕРИАЛОВ
Л.Н.Буренкова 1,
Б.В.Романовский 1, Л.Н.Соколова 2,
Е.Д.Щукин 1,2
1 Химический факультет МГУ, 2 Институт
физической химии РАН
Механическая прочность макропористых тел, имеющих глобулярное строение, определяется как числом, так и общей площадью межчастичных контактов, и ее повышение при высокотемпературном спекании является результатом массопереноса поверхностных атомов в контактные зоны. Общая скорость этого процесса определяется двумя факторами - коэфициентом поверхностной диффузии и концентрацией мигрирующих частиц. Первый из них зависит от природы поверхности твердого тела и температуры; второй фактор также определяется температурой процесса, но в не меньшей степени и характером взаимодействия со средой. Такое взаимодействие всегда имеет место при протекании на поверхности каталитических реакций, и поэтому следовало ожидать, что в условиях катализа может происходить резкое повышение скорости поверхностной диффузии, приводящее к заметному увеличению механической прочности материала. Действительно, ранее было показано для металлических порошков [1,2], что в условиях протекания на них каталитических реакций происходит повышение интенсивности поверхностного массопереноса и увеличение механической прочности. Можно было полагать, что, если каталитическая реакция и возникновение поверхностных дефектов, являются сопряженными процессами, то повышение эффективности массопереноса в контактные зоны достигается за счет свободной гиббсовой энергии химического процесса.
Целью настоящей работы была проверка этого предположения на примере оксидной системы ZrO2+Y2O3 как катализатора окисления и дегидратации метанола и этанола. Эффект упрочения прессованных таблеток этого материала, который достагал в ряде случаев 80-90 %, наблюдается независимо от того, является ли протекающая каталитическая реакция экзотермической или эндотермической. Существенно, что упрочение достигается именно в результате протекания каталитической реакции, поскольку, эффект тем заметнее, чем выше температура процесса, т.е. чем выше скорость реакции.
Эти данные показывают, что ключевым фактором, определяющим эффект упрочения прессованных порошков при проведении на них каталитической реакции, является не экзотермичность реакции, которая могла бы привести к локальному нагреву поверхности материала, а значительное повышение концентрации дефектов по сравнению с равновесной при данной температуре. Хотя прочность материала, полученного после осуществления такого процесса на смеси ZrO2+Y2O3 , далека от прочностей, характерных для оксидно-циркониевых керамик, этот результат представляется принципиально важным.
Литература