Научные достижения химического факультета
26.01.2022
Химики МГУ выяснили механизм фотопереноса электрона флуоресцентного белка
Сотрудники кафедры физической
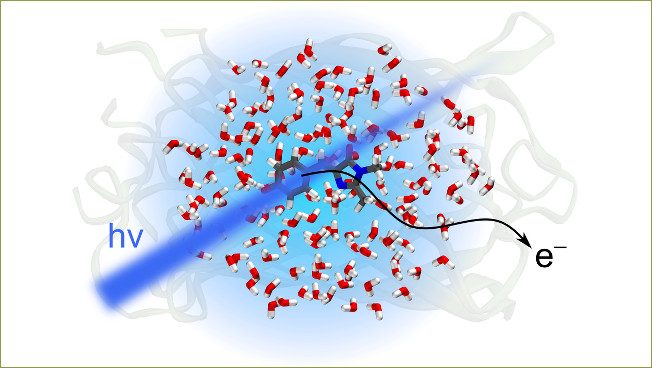
химии Химического факультета МГУ совместно с учеными из Университетского
колледжа Лондона исследовали процессы окисления хромофора зеленого
флуоресцентного белка в водном растворе. Результаты позволят значительно
расширить область применения одного из самых актуальных способов следить за
деятельностью белков и помогут создать индикатор на активные формы кислорода.
Работа, выполненная при поддержке
Российского научного фонда, опубликована
в журнале Nature Communications.
Зеленый флуоресцентный белок
активно используется биологами для наблюдения за процессами в живых организмах.
Его присоединение к другим молекулам в качестве светящейся зеленой метки
позволяет точно отследить их положение в клетке.
"Мы изучали хромофор – часть
белка, отвечающую за его способность светиться, – рассказала руководитель лаборатории
квантовой фотодинамики, соавтор работы, доцент, к.ф.-м.н. Анастасия Боченкова. –
Ведь именно при испускании поглощенного хромофором света мы и видим зеленое
свечение. Однако в некоторых случаях хромофор может подвергаться окислению, то
есть отдавать электрон другой молекуле. Окисленный белок меняет длину волны
излучения, становясь красным, что является перспективным для создания
светочувствительных редокс биосенсоров. Фотоокисление может также приводить к
необратимому обесцвечиванию, при котором белок больше не может светиться, что
значительно снижает область его практического применения".
До недавнего времени
окислительные свойства хромофора зеленого флуоресцентного белка были изучены
только для молекул в газовой фазе – относительно простого для проведения и
интерпретации результатов процесса. Но так как окружение сильно влияет на
свойства хромофора, окислительно-восстановительные характеристики для газовой
фазы и для белка должны заметно отличаться.
"Непосредственно в белке
окислительные свойства изучать очень сложно, но наши коллеги из Англии
попытались приблизиться к этому: они нашли способ исследовать окисление
хромофора в водном растворе, – пояснила Анастасия Боченкова. – С точки зрения
эксперимента это прорывная методика, но получаемые результаты очень сложны для
понимания. Для их правильной интерпретации нужно в деталях понимать механизм
фотоиндуцированного переноса электрона с хромофора. Поэтому наша часть работы
заключалась в разработке метода моделирования и анализа фотоэлектронных
спектров. Мы проводили масштабные квантовохимические расчеты с помощью
ресурсов суперкомпьютерного комплекса Ломоносов-2".
Комбинация многофотонной ультрафиолетовой
фотоэлектронной спектроскопии и расчетов квантовой химии высокого уровня
точности позволила получить значения энергии отрыва электрона и оценить влияние
окружения на электронную структуру хромофора, исследовать характер и роль его электронно-возбужденных
состояний в процессах фотопереноса электрона. Полученное экспериментальное
значение энергии отрыва электрона оказалось гораздо больше измеренного в
газовой фазе. Авторы также сравнили его со своими расчетами для белка. Полное
сходство двух значений указывает на то, что способность хромофора отдавать
электрон при поглощении фотона в белковом окружении и водной среде практически
одинаково.
"Помимо помощи экспериментаторам,
мы смогли верифицировать предложенную нами методику расчетов, – объяснил аспирант
лаборатории квантовой фотодинамики химического факультета МГУ и соавтор
исследования Антон Бойченко.
– Это поможет в дальнейшем распространить ее на другие подобные системы и
откроет возможность интерпретировать результаты сложных экспериментальных
исследований".
"В будущем мы хотим направить фотоокисление
во благо, – поделилась Анастасия Боченкова. – В клетке ведь тоже есть
окислители, например, активные формы кислорода. Появление красного свечения
вместо зеленого позволяет использовать белок как биосенсор, показывающий
наличие окислителей в клетке. Основная проблема, ограничивающая его применение –
маленький выход реакции. Сейчас мы активно работаем над ее устранением, с
помощью физических подходов пытаемся повысить эффективность процесса при лазерном облучении в линейном и нелинейном режиме".
Ссылка на статью:
Omri Tau, Alice Henley, Anton N. Boichenko, Nadezhda N. Kleshchina, River Riley, Bingxing Wang, Danielle Winning, Ross Lewin, Ivan P. Parkin, John M. Ward, Helen C. Hailes, Anastasia V. Bochenkova & Helen H. Fielding
Liquid-microjet photoelectron spectroscopy of the green fluorescent protein chromophore
Nature Communications volume 13, Article number: 507 (2022)
https://doi.org/10.1038/s41467-022-28155-5

